Σαριδάκη Αικατερίνη
Ενδοκρινολόγος, διευθύντρια Β΄ Ενδοκρινολογικού
τμήματος Ευρωκλινικής
Γουλή Αγγελική-Μαρία
Ενδοκρινολόγος
1. Εισαγωγή
Ο Υποθάλαμο-Υποφυσιο-Θυρεοειδικός Άξονας (ΥΥΘ) (Εικόνα 1), αποτελεί τμήμα του ενδοκρινικού συστήματος που είναι υπεύθυνο για την ρύθμιση του μεταβολισμού. Όπως προτείνει το όνομά του, αποτελείται από τον υποθάλαμο, την υπόφυση και τον θυρεοειδή αδένα.
Σε γενικές γραμμές, ο υποθάλαμος αντιλαμβάνεται τα χαμηλά επίπεδα των θυρεοειδικών ορμονών Τ3 (Τριιωδοθυρονίνη), Τ4 (θυροξίνη) και αντιδρά με την απελευθέρωση της TRH (Thyroid Releasing Hormone) από τον υποθάλαμο. Με την σειρά της η TRH διεγείρει την παραγωγή TSH (Thyroid Stimulating Hormone, θυρεοειδοτρόπος ορμόνη) από την υπόφυση, η οποία διεγείρει την παραγωγή των θυρεοειδικών ορμονών, μέχρι τα επίπεδά τους να φτάσουν τα φυσιολογικά. Οι θυρεοειδικές ορμόνες δρουν στον υποθάλαμο και την υπόφυση με αρνητική παλίνδρομη ρύθμιση (negative feedback), με αποτέλεσμα την ισορροπία στην έκκριση TRH και TSH αντίστοιχα1.
Η ομοιοστασία του θυρεοειδούς διατηρείται από πολλαπλά συστήματα αρνητικών παλίνδρομων αλληλεπιδράσεων στα περισσότερα σπονδυλωτά. Η άριστη λειτουργία του συστήματος αρνητικής παλίνδρομης ρύθμισης, είναι απολύτως απαραίτητη για την ανάπτυξη, την κατά φύλο διαφοροποίηση, την αναπαραγωγή και την ανάπτυξη της νοημοσύνης.
Η υπόφυση εκκρίνει την TSH, η οποία διεγείρει την έκκριση θυροξίνης (Τ4) και σε μικρότερο βαθμό τριιωδοθυρονίνης (T3). Το μεγαλύτερο ποσοστό της Τ3, ωστόσο, παράγεται στα περιφερικά όργανα από την Τ4 με αφαίρεση του ενός Ιωδίου. Η αποϊωδίωση ελέγχεται από πολλές ορμόνες και νευρικά ερεθίσματα συμπεριλαμβανομένων των TSH, βαζοπρεσσίνης και κατεχολαμινών.
Και οι δυο ιωδοθυρονίνες (θυρεοειδικές ορμόνες) αναστέλλουν την έκκριση της TSH από την υπόφυση. Έτσι επιτυγχάνεται η ισορροπία όλων των ορμονών. Η έκκριση της TSH, ωστόσο, δεν θα υπήρχε χωρίς την παραγωγή της TRH από τον υποθάλαμο, στην έκκριση του οποίου πάλι επιδρούν οι θυρεοειδικές ορμόνες του εγκεφαλονωτιαίου υγρού, μέσω αρνητικής παλίνδρομης ρύθμισης (μακρά καμπύλη παλίνδρομης ρύθμισης)2. Επιπροσθέτως η έκκριση της TSH υπόκειται σε έλεγχο και από το τοπικό (ultra-short)3 κύκλωμα αρνητικής παλίνδρομης ρύθμισης όπως επίσης και από τα γραμμικά κυκλώματα που ελέγχουν την σύνδεση των περιφερικών ορμονών με τις συνδετικές τους πρωτεΐνες (Εικόνα 1).
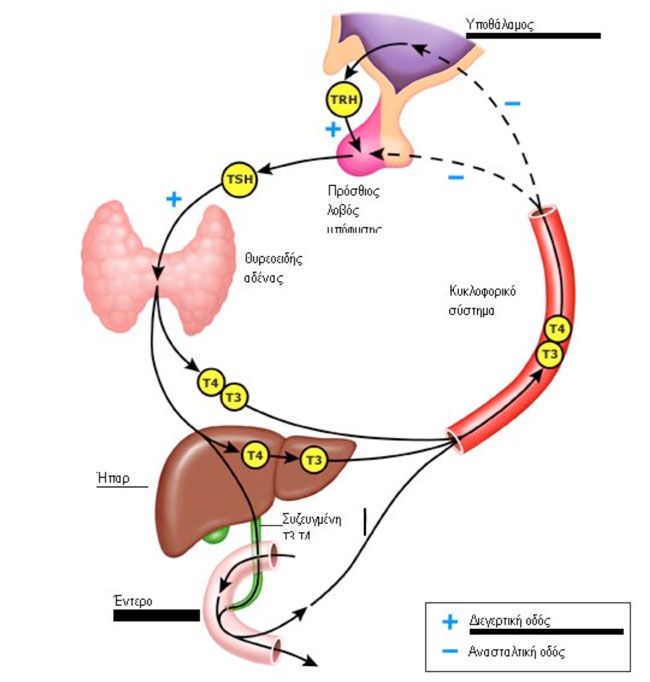
Εικόνα 1. Άξονας υποθάλαμος – υπόφυση – θυρεοειδής
2. Υποθάλαμος και άξονας θυρεοειδικών ορμονών
Ο Υποθάλαμος είναι μία δομή του εγκέφαλου που αποτελείται από διακριτούς πυρήνες αλλά και από λιγότερο διακριτές ανατομικές περιοχές. Ο ρόλος του είναι να συντονίζει ορμονικούς αλλά και συμπεριφεριολογικούς κιρκάδιους ρυθμούς, πολύπλοκες νευροενδοκρινικές λειτουργίες και ομοιοστατικούς μηχανισμούς, καθώς και εξαιρετικής σημασίας συμπεριφορές. Επομένως ο υποθάλαμος ανταποκρίνεται σε ποικίλα ερεθίσματα, τα οποία δημιουργούνται είτε μέσα σε αυτόν είτε προέρχονται από ανώτερα εγκεφαλικά κέντρα, όπως για παράδειγμα ο προμήκης.
Αποτελεί μέρος του μεταιχμιακού συστήματος και επομένως βρίσκεται σε άμεση σχέση με την αμυγδαλή και το διαφανές διάφραγμα, ενώ συνδέεται πολλαπλώς και με το αυτόνομο νευρικό σύστημα.
Τέλος, ο υποθάλαμος είναι ένα είδος θερμοστάτη για το σώμα. Δεδομένης της ιδιότητας του ΥΥΘ άξονα να ελέγχει τη θερμορρύθμιση, είναι σαφής η στενή σχέση του με τη λειτουργία του θυρεοειδικού συστήματος.
Η TRH απελευθερώνεται από τον παρακοιλιακό πυρήνα του υποθαλάμου (Paraventricular Nucleus, PVN) και δη από τα μικρότερου μεγέθους νευρικά κύτταρά του (parvocellular) που καταλήγουν στον πρόσθιο λοβό της υπόφυσης, μέσω του πυλαίου υποφυσιακού αγγειακού συστήματος (Εικόνες 2, 3).

Εικόνα 2. Πυρήνες υποθαλάμου

Εικόνα 3. Ανατομία υποθαλάμου – υπόφυσης
Έχει αποδειχτεί ότι η Τ4 προσλαμβάνεται από τα κύτταρα της γλοίας στην μέση εσοχή (median eminence), εκεί μετατρέπεται σε Τ3 μέσω 2-ιωδινάσης (D2) και έτσι μεταφέρεται στους νευρώνες παραγωγής TRH στον παρακοιλιακό πυρήνα.
Σε αυτούς τους νευρώνες εκφράζεται και ένας μεταφορέας θυρεοειδικών ορμονών, ο MCT8 πράγμα που αποδεικνύει την μεταφορά της Τ3, η οποία συνδέεται με τους εκεί υποδοχείς των θυρεοειδικών ορμονών, ώστε να επηρεάζεται η παραγωγή του TRH από την περιφέρεια.
3. ΤRH
3.1. Εισαγωγή
Ιστορία. Την αλληλουχία των αμινοξέων στην TRH ταυτοποίησαν κατά την ίδια εποχή ο Roger Guillemin και ο Andrew Schally το 19694,5. Παρά τον ανταγωνισμό που υπήρξε, το 1977 μοιράστηκαν το βραβείο Nobel της Ιατρικής για τις ανακαλύψεις τους γύρω από την παραγωγή πεπτιδικών ορμονών.
Xημεία. Πρόκειται για τριπεπτίδιο με ΜΒ 359,5 Da, αποτελούμενο από τα αμινοξέα: πυρογλουταμικό οξύ- ιστιδίνη-προλίνη. Είναι το κυριότερο μόριο που διεγείρει την σύνθεση και έκκριση της ΤSH.
Παραγωγή. Όπως έχει ήδη αναφερθεί, η TRH παράγεται στον υποθάλαμο στους μέσους μικροκυτταρικούς (parvocellular) νευρώνες του παρακοιλιακού πυρήνα. Αρχικά συντίθεται σε προμορφή, ως ένα πολυπεπτίδιο με 242 αμινοξέα (29kD), την προ-προ-ΤRH. Η διάσπασή της οδηγεί σε 5-κατ’ άλλους 6- τετραπεπτίδια προ-TRH και σε άλλα μόρια τα περισσότερα με δράση παρόμοια της TRH και πιθανή συμμετοχή σε άλλα μεταβολικά μονοπάτια.
Mετά από επεξεργασία με μια μεγάλη σειρά ενζύμων, κυρίως πεπτιδάσες, κάθε προμορφή καταλήγει σε 5 -κατ’ άλλους 6- αντίγραφα από ώριμη TRH6,7 στον άνθρωπο. Η TRH μεταβολίζεται ταχύτατα με χρόνο ημιζωής τα 3 min.
Η έκκρισή της TRH γίνεται κατά ώσεις, που αντιστοιχούν στην κατά ώσεις έκκριση και του TSH. Αυτά τα ώριμα μόρια κατεβαίνουν μέσω της μέσης εσοχής στην πρόσθια υπόφυση με το πυλαίο αγγειακό σύστημα της υπόφυσης, όπου και διεγείρουν την έκκριση TSH μετά από σύνδεση με τους μεμβρανικούς υποδοχείς στα θυρεοτρόπα κύτταρα της υπόφυσης. Αμέσως μετά την σύνδεση ενεργοποιούνται μηχανισμοί της ενδοκυτταρίου οδού της φωσφολιπάσης C και της φωσφατυδιλ-ινοσιτόλης 3 (PLC-PIP3), με αποτέλεσμα την αύξηση c-AMP και την απελευθέρωση Ca2+ από τις ενδοκυττάριες αποθήκες του.
Η TRH παράγεται επίσης σε άλλους ιστούς και κυρίως σε άλλα μέρη του ΚΝΣ, όπου δρα σαν νευρομεταβιβαστής (υπόφυση, παγκρεατικά νησίδια, γαστρεντερικός σωλήνας και στο αναπαραγωγικό σύστημα).
3.2. Φυσιολογικός ρόλος και κλινική σημασία TRH
Κατ αρχήν η TRH καθορίζει τον ουδό της αρνητικής παλίνδρομης ρύθμισης της έκκρισης του TSH από τις περιφερικές θυρεοειδικές ορμόνες. Εξωγενής χορήγηση TRH στα φυσιολογικά άτομα οδηγεί στην σταδιακή αύξηση των επιπέδων της TSH. Στον υποθυρεοειδισμό η απάντηση είναι εκσεσημασμένη ενώ στον υποθυρεοειδισμό μειωμένη. Η εξωγενής χορήγηση TRH ενδοφλεβίως χρησιμοποιείται για τον έλεγχο και την λειτουργία του προσθίου λοβού υπόφυσης. Προκαλεί αύξηση της προλακτίνης φυσιολογικά αλλά και στις πλείστες υπερπρολακτιναιμίες, παράδοξη αύξηση αυξητικής ορμόνης στην μεγαλακρία, στην ηπατική νόσο και στο σακχαρώδη διαβήτη, ενώ στην μεγάλη ηλικία η αύξηση της αυξητικής ορμόνης θεωρείται αναμενόμενη. Έχει αντικαταθλιπτικές και αντι-αυτοκτονικές ιδιότητες8. Το 2012, Ο Στρατός στις ΗΠΑ, χρηματοδότησε έρευνα για χορήγηση TRH σε ρινικό εκνέφωμα προκειμένου να μειώσουν τις αυτοκτονίες9. Στους επίμυες έχει φανεί ότι έχει αντιγηραντική δράση.
3.3. Ρύθμιση της έκκρισης της TRH και περιφερικές επιδράσεις
Σύμφωνα με την πληρέστερη ανασκόπηση του 2010 από τον E.A.Nillni10, είναι απολύτως απαραίτητο να κατανοηθούν οι κυτταρικοί και μοριακοί μηχανισμοί οι οποίοι ελέγχουν την έκφραση του γονιδίου της προ-προ-TRH (Pre-pro-TRH), την βιοσύνθεσή της και την αναδίπλωσή της, μέχρι την μετά- μεταφραστική διαδικασία προς τα ώριμα μόρια του TRH. Από την ανακάλυψη των PC’s δηλαδή των κονβερτασών των προ-ορμονών, στο τέλος του 1980, άλλαξε ο τρόπος θεώρησης της σύνθεσης των πεπτιδικών ορμονών. Μια ομάδα, άλλοτε άλλου μεγέθους ενζύμων, είναι απολύτως απαραίτητα για την μετά-μεταφραστική διαδικασία. Τα ενζυμα αυτά βρίσκονται μέσα στο εκκριτικό σύστημα. Στα ενζυμα αυτά, επιδρούν ορμόνες εξαιρετικά σημαντικές στην φυσιολογία του θυρεοειδούς, όπως η λεπτίνη και η Τ3.
Η λεπτίνη έχει κεντρικό φυσιολογικό ρόλο στο να δίνει πληροφορίες για τις αποθήκες ενέργειας και την ενεργειακή ισορροπία στα κέντρα του εγκεφάλου, τα οποία ρυθμίζουν την όρεξη, την αποβολή ενέργειας, και τις νευροενδοκρινικές λειτουργίες. Όταν διαταράζεται η μεταφορά σήματος από τους νευρώνες της λεπτίνης, είτε λόγω μεταλλάξεων, είτε λόγω βλάβης στον υποδοχέα της, παρατηρείται σοβαρή παχυσαρκία τόσο στους επίμυες όσο και στον άνθρωπο. Έχει άμεσες και έμμεσες επιδράσεις στους νευρώνες της TRH με αποτέλεσμα αύξηση της βιοσύνθεσής της. Μαζί με τη νορεπινεφρίνη και την Τ3, επιδρά άμεσα στη βιοσύνθεση, την επεξεργασία και την έκκριση της προTRH, και ταυτοχρόνως, έμμεσα, στα ένζυμα PC1/3, PC2, τα οποία είναι απαραίτητα για την ωρίμανση της προ-TRH. Αυτά συμβαίνουν υπό κανονικές συνθήκες και όχι επί παχυσαρκίας ή πείνας.
Η επίδραση της λεπτίνης στον υποθάλαμο αφορά στην προ-TRH, και χρησιμοποιεί ως διαμεσολαβητή το μελανοκορτικοτρόπο σύστημα του τοξοειδούς πυρήνα του υποθαλάμου, το οποίο έχει βασικό ρόλο στην λήψη τροφής. Η α-MSH μέσω του υποδοχέα ΜC4R, ενός υποδοχέα συζευγμένου με πρωτεΐνη Gs αυξάνει την TRH, ενώ το AgRP (Agouti-Related Peptide) την μειώνει, ανταγωνιζόμενο την α-MSH. Τελικό αποτέλεσμα της δράσης της λεπτίνης είναι η αύξηση της TRH.
Στην παχυσαρκία, κατάσταση με αυξημένες συγκεντρώσεις λεπτίνης, ο άξονας υποθαλάμου-υπόφυσης βρίσκεται να λειτουργεί σε υψηλότερα επίπεδα και τα άτομα με νοσογόνο παχυσαρκία έχουν υψηλότερα επίπεδα θυρεοειδικών ορμονών σε σύγκριση με τα αντίστοιχα νορμοβαρή. Παρά την αυξημένη λεπτίνη, ωστόσο, τα άτομα αυτά δεν φαίνεται να έχουν ελαττωμένη όρεξη ούτε αυξημένη ενεργειακή κατανάλωση. Αυτή η κατάσταση έχει χαρακτηριστεί αντίσταση στη λεπτίνη και παρουσιάζει δυνητικές εφαρμογές στην αντιμετώπιση της παχυσαρκίας.
Το ΝΡΥ, ορεξιογόνο πεπτίδιο, έχει αρνητική επίδραση στην παραγωγή TRH στον PVN, μέσω σύνδεσης του με τους υποδοχείς NPY στον TRH νευρώνα. Είναι γνωστό ότι το ΝΡΥ εκτός από το να διεγείρει τη λήψη τροφής, διακόπτει τη φυσιολογική αρνητική παλίνδρομη ρύθμιση του θυρεοειδούς κατά την στέρηση τροφής, με στόχο την οικονομία ενέργειας. Οι νευρώνες του ΝPY μαζί με τους κατεχολαμινεργικούς νευρώνες είναι μεικτής προέλευσης και αποτελούν δενδρίτες των νευρώνων TRH, οι οποίοι δέχονται αρνητική παλίνδρομη ρύθμιση από τον υποθάλαμο.
Οι ΝΡΥ νευρώνες του τοξοειδούς πυρήνα, αναστέλλουν τους νευρώνες της προοπιομελανοκορτίνης (POMC) στον ίδιο πυρήνα, άμεσα και μέσω γ-αμινοβουτυρικού οξέος (GABA), με αποτέλεσμα να μην παράγεται α-MSH. Έξι υποδοχείς NPY (Y1-6), είναι υπεύθυνοι για την αναστολή λήψης τροφής ανάλογα με τις συνθήκες και τον υποδοχέα που διεγείρεται. ΟΙ Υ1 και Υ5 προκαλούν διαφορετική επίδραση του ΝΡΥ στον άξονα υποθαλάμου-υποφύσεως-θυρεοειδούς, πιθανώς λόγω διαφορετικής ανατομικής θέσης στον παρακοιλιακό και στον τοξοειδή πυρήνα, αντίστοιχα. Επί παραδείγματι, μέσω Υ1 διεγείρεται η επιθυμία πρόσληψης τροφής, ενώ μέσω Υ5 καθορίζεται το μέγεθος του γεύματος.
Η νηστεία προκαλεί την αύξηση της αποϊωδινάσης D2 στα κύτταρα του παρακοιλιακού πυρήνα με αποτέλεσμα την αποϊωδίωση της Τ4 και αύξηση της Τ3 στην περιοχή, ώστε να αναστέλλεται η έκκριση TRH μέσω των προ-ορμονών, για οικονομία ενέργειας. Παράλληλα, σε συνθήκες παρατεταμένης νηστείας παρατηρείται ελάττωση της έκφρασης της προ-TRH με στόχο την ελάττωση του μεταβολικού ρυθμού και τη διατήρηση των ενεργειακών αποθεμάτων. Η έκθεση στο ψύχος έχει ως συνέπεια την αύξηση της έκφρασης της προ-TRH, μέσω κατεχολαμινικής διέγερσης.
Ο άξονας υποθαλάμου-υπόφυσης-θυρεοειδούς ανταποκρίνεται σε μια νόσο με απρόσφορη έκκριση TSH, όπως φαίνεται στο σύνδρομο της ευθυρεοειδικής νόσου. Η ανορεξία που παρατηρείται σε αυτό υποδηλώνει ότι ελέγχεται από τις οδούς της λεπτίνης και της μελανοκορτίνης.
Συμπερασματικά, οι υποφυσιοτρόποι νευρώνες της TRH στον παρακοιλιακό πυρήνα είναι ευαίσθητοι στα επίπεδα της Τ3, και άλλων ορμονών (λεπτίνης, α-MSH, AgRP, NPY) οι οποίες εμπλέκονται στην ενεργειακή ομοιοστασία. O TRH νευρώνας αντιλαμβάνεται και συντονίζει όλες αυτές τις δράσεις, ώστε να αποφασιστεί το σημείο έναρξης της έκφρασης του γονιδίου προ-προ-TRH με τελικό αποτέλεσμα την σύνθεση των ώριμων μορίων ΤRH, και την μεταφορά τους στην υπόφυση. Η ρύθμιση των γονιδίων αυτών ακολουθείται από κυριαρχικούς μηχανισμούς ρύθμισης του σταδίου έκλυσης των προμορφών της TRH από τις προκονβερτάσες PC1/3, PC2.
Βάσει των νέων αυτών γνώσεων μπορούμε να πούμε ότι η TRH είναι ένας μεταβολικός αισθητήρας που ρυθμίζεται σε διάφορα επίπεδα, ώστε να ελέγξει την θυρεοειδική λειτουργία και τον μεταβολισμό.
Εντοπίζεται σε πολλά διαφορετικά σημεία του εγκεφάλου και άλλων ιστών όπως για παράδειγμα στο γαστρεντερικό και γεννητικό, γεγονός που υποδηλώνει ότι η TRH λειτουργεί και ως νευρομεταβιβαστής.
3.4. Υποδοχείς TRH
Όλες οι δράσεις της TRH11 αρχίζουν με την σύνδεση της με τους υποδοχείς της (Εικόνα 4), οι οποίοι ανήκουν στην οικογένεια των συζευγμένων με πρωτεΐνη G υποδοχέων κατηγορίας Α (Class A G-protein-coupled receptors, GPCR). Το 1990 ο πρώτος υποδοχέας TRH1 κλωνοποιήθηκε σε επίμυες. Ο ανθρώπινος υποδοχέας είναι ομόλογος κατά 80.2% έως 90.3% σε επίμυες και αρουραίους, αντίστοιχα.

Εικόνα 4. Υποδοχέας TRH
Το 1998 ένας δεύτερος υποδοχέας TRH 2 ταυτοποιήθηκε σε επίμυες και σε άλλα είδη, όχι όμως στον άνθρωπο (Πίνακας 1). Ο ΤRH 1 υποδοχέας συνδέεται με τις Gq/11πρωτεΐνες με δεύτερο νευρομεταβιβαστή την φωσφοϊνοσιτόλη (ΙΡ3) και διακυλογλυκερόλη (DAG).
Μόνο η TRH συνδέεται με τον υποδοχέα TRH1. Mεγαλύτερη συγγένεια δείχνει με το ανάλογο N-methylHis-TRH (MeTRH). Διάφοροι άλλοι ανταγωνιστές έχουν συνδεθεί, αλλά με μικρή συγγένεια με τον υποδοχέα TRH.
Πίνακας 1. Κατανομή των υποδοχέων της TSH-R 1 και 2 στον εγκέφαλο του αρουραίου.
4. Θυρεοειδοτρόπος Ορμόνη (Thyroid Stimulating Hormone, TSH)
4.1. Εισαγωγή
Η TSH είναι ένα ετεροδιμερές γλυκοπρωτεϊνικό μόριο με ΜΒ 28kDa, το οποίο αποτελείται από δύο υπομονάδες, την άλφα και τη βήτα. H α -υπομονάδα έχει αλληλουχία 92 αμινοξέων. Έχει ακριβώς την ίδια σύνθεση με την α-υποομάδα της β-χοριακής γοναδοτροπίνης (β-HCG), της Ωχρινοποιητικής ορμόνης (LH) και της Ωοθυλακιοτρόπου ορμόνης (FSH). H υπομονάδα αυτή είναι υπεύθυνη για την διέγερση της αδενυλκυκλάσης (c-AMP).Το γονίδιο έκφρασης της α-υπομονάδας είναι στο χρωμόσωμα 6 και αποτελείται από 4 εξόνια και 4 ιντρόνια12.
Η β-υπομονάδα, έχει αλληλουχία 82 αμινοξέων, είναι μοναδική για την TSH και επομένως χαρακτηρίζει την ειδικότητα για τον TSH-υποδοχέα. Μόνη της δεν είναι δραστική και πρέπει να συνδεθεί με την α-υπομονάδα για να αποκτήσει ορμονική δραστηριότητα. Το γονίδιο έκφρασής της βρίσκεται στο χρωμόσωμα 1 και αποτελείται από 3 εξόνια και 3 ιντρόνια. Η αλληλουχία 27CAGYC31 των αμινοξέων της β-υπομονάδας (κυστεΐνη-αλανίνη-γλυκίνη-τυροσίνη- κυστεΐνη) ανευρίσκεται και στις β-υπομονάδες των γοναδοτροπινών και η παρουσία της είναι σημαντική για τον ετεροδιμερισμό της με την α-υπομονάδα σε δραστικό μόριο.
Η ωρίμανση του μορίου μετά-μεταφραστικά αποτελείται αρχικά από γλυκοζυλίωση, κυρίως με μαννόζη, με σταδιακή αντικατάστασή της από φρουκτόζη, γαλακτόζη και σιαλικό οξύ. Η διαδικασία της γλυκοζυλίωσης μέσα στην συσκευή Golgi του κυττάρου καθιστά δυνατή την αναδίπλωση των δύο υπομονάδων του μορίου, έτσι ώστε να γίνει η σύνδεση και να προκύψει το ετεροδιμερές σταθερό, βιολογικά δραστικό μόριο. Η πρόσδεση της TRH στον υποδοχέα του θυρεοειδοτρόπου κυττάρου είναι καθοριστικής σημασίας για την επίτευξη της γλυκοζυλίωσης.
Ο χρόνος ημιζωής της TSH είναι 1 ώρα. Η έκκρισή της γίνεται κατά ώσεις ανά δίωρο και σε ένταση 0,6 mU/L, με την συχνότητά τους να αυξάνει προ του ύπνου μέχρι και κατά 50%-100% και να σταματά με την έλευση του ύπνου. Υπάρχουν πολλές εικασίες, αλλά δεν έχει διευκρινιστεί η αιτία της βραδινής ανάγκης. Η ημερήσια παραγόμενη ποσότητα της TSH είναι συνολικά 75-150 mU, ενώ μπορεί να αυξηθεί δραματικά στον υποθυρεοειδισμό φθάνοντας και τις 4000 mU ημερησίως.
Αυξημένη παραγωγή TSH αναστέλλει την ντοπαμίνη, με αποτέλεσμα την αύξηση της προλακτίνης και μείωση του εκλυτικού παράγοντα των γοναδοτροπινών (Gonadotropin-Releasing Hormone, GnRH). Η ΤSH εκκρίνεται δια βίου με μεγαλύτερα φυσιολογικά επίπεδα στην ταχεία ανάπτυξη.
4.2. Κατανομή του υποδοχέα TSH
Το γονίδιο του υποδοχέα βρίσκεται στο χρωμόσωμα 14/31. Εκφράζεται κυρίως στον θυρεοειδή, αλλά και σε άλλους ιστούς όπως ο λιπώδης και ο μυϊκός ιστός. Βρίσκεται κυρίως στα θηλώδη κύτταρα του θυρεοειδούς, στην μεμβράνη και πρόκειται επίσης για έναν διαμεμβρανικό υποδοχέα συζευγμένο με G-πρωτεΐνη (GPCR). Έχει MB 85kDa, με εξωκυττάρια περιοχή αποτελούμενη από 400 αμινοξέα και μικρότερη ενδοκυττάρια, αποτελούμενη από 100 αμινοξέα. Ο ώριμος υποδοχέας έχει πολλές θέσεις γλυκοζυλίωσης. Διέγερση του υποδοχέα προκαλεί αυξημένη παραγωγή τόσο της Τ3 όσο και της Τ4.
4.3. Διαταραχές του υποδοχέα της TSH
Διαταραχές του υποδοχέα της TSH συμβαίνουν τόσο στο εξωκυττάριο τμήμα του όσο και στο ενδοκυττάριο διαμεμβρανικό. Οι ενεργοποιητικές μεταλλάξεις του υποδοχέα συχνότερα αφορούν το διαμεμβρανικό του τμήμα και προκαλούν σύνδρομα ανθεκτικού υπερθυρεοειδισμού, σε νεαρή ηλικία με αντίσταση στις κλασικές φαρμακευτικές θεραπείες. Το αυτόνομο αδένωμα του θυρεοειδούς, ο οικογενής μη αυτοάνοσος υπερθυρεοειδισμός (Familial Non-Autoimmune Hyperthyroidism, FNAH), όπως και ο σποραδικός συγγενής μη αυτοάνοσος υπερθυρεοειδισμός (Sporadic Congenital Non-Autoimmune Hyperthyroidism, SCNAH) είναι αποτέλεσμα αυτών των ενεργοποιητικών μεταλλάξεων με άλλοτε άλλη βαρύτητα7.
Οι μεταλλάξεις που αφορούν στο εξωκυττάριο τμήμα του υποδοχέα είναι αδρανοποιητικές μεταλλάξεις, δηλαδή δημιουργούν αντίσταση στην TSH7,13, κατάσταση κληρονομούμενη κατά τον υπολειπόμενο χαρακτήρα. Οι ετεροζυγώτες μπορεί να είναι άτομα ευθυρεοειδικά14, με φυσιολογικές περιφερικές τιμές θυρεοειδικών ορμονών και με οριακά υψηλή TSH, δηλαδή να έχουν εικόνα δυνητικού υποκλινικού υποθυρεοειδισμού, ενώ οι ομοζυγώτες έχουν βαρύ υποθυρεοειδισμό, από την νεογνική ακόμα ηλικία και έχουν υποπλαστικό ή απλαστικό θυρεοειδή αδένα. Συχνά παρατηρούνται ενδιάμεσες μορφές υποθυρεοειδισμού με άλλοτε άλλη αντίσταση του υποδοχέα στην TSH.
Άλλα αίτια αντίστασης στην TSH αποτελούν η μετάλλαξη στο γονίδιο του μεταγραφικού παράγοντα PAX8, απαραίτητου για την μεταγραφή του γονιδίου του υποδοχέα της TSH, όπως και κάποιες όχι σαφώς καθορισμένες μεταλλάξεις στο χρωμόσωμα 15.
Άλλες διαταραχές αφορούν σε αντισώματα που διεγείρουν τον υποδοχέα της και καταλήγουν στη νόσο Graves. Εξαιτίας της συγγένειας της χοριακής γοναδοτροπίνης (hCG) με τον υποδοχέα της TSH, μια αύξηση στις τιμές hCG, όπως συμβαίνει στην κύηση, μπορεί να μιμηθεί υπερθυρεοειδισμό.
Εικόνα παρόμοια με την αντίσταση στις θυρεοειδικές ορμόνες παρουσιάζουν τα αδενώματα της υπόφυσης, έχοντας ως τυπικές εκδηλώσεις, εκτός από την εικόνα του τυπικού υπερθυρεοειδισμού με διάχυτη βρογχοκήλη, διαταραχές οπτικών πεδίων και επίσης γαλακτόρροια και αραιομηνόρροια στις γυναίκες. Τα τυπικά εργαστηριακά ευρήματα είναι αυξημένη ή οριακά υψηλή TSH σε συνδυασμό με υψηλή ελεύθερη και ολική Τ3 και Τ4, καθώς και αυξημένα επίπεδα της α-υπομονάδας των γλυκοπρωτεϊνών.
4.4. Δράση της TSH
Η TSH διεγείρει την πρόσληψη του ιωδίου, τη σύνθεση της θυρεοειδικής υπεροξειδάσης (ΤΡΟ), της θυρεοσφαιρίνης και τη σύνθεση των θυρεοειδικών ορμονών στα θυλακιώδη κύτταρα των θυρεοειδικών κυστιδίων. Είναι επίσης αυξητικός παράγοντας όσον αφορά στο μέγεθος του αδένα και διεγείρει την αύξηση του μεγέθους και του αριθμού των θυρεοειδικών κυττάρων, μέσω ενεργοποίησης πολλαπλών γονιδίων. Η πρόσδεση της TSH στην εξωκυττάρια μοίρα του υποδοχέα διεγείρει τρία συστήματα ενδοκυττάριας επικοινωνίας: το cAMP, την αύξηση του ενδοκυττάριου Ca2+, και το σύστημα της πρωτεϊνικής κινάσης
4.5. Ρύθμιση της έκκρισης ΤSΗ
H TSH7 είναι εξαιρετικά ευαίσθητη σε μικρές αλλαγές των επιπέδων των κυκλοφορούντων περιφερικών θυρεοειδικών ορμονών, με αποτέλεσμα η TSH να μειώνεται με μικρές αυξήσεις και να αυξάνεται με μικρές μειώσεις αυτών. Χάρη στην ευαισθησία αυτή οι Τ4 και Τ3 διατηρούνται σε πολύ στενά φυσιολογικά όρια.
Η ενδοκυττάρια Τ3, συνδεόμενη με τον πυρηνικό υποδοχέα των θυρεοειδικών ορμονών στην υπόφυση, έχει τον κύριο ρόλο στην αναστολή της σύνθεσης της TSH. Μετά τη σύνδεση της Τ3 με τον υποδοχέα, αναστέλλεται η έκφραση του γονιδίου κυρίως της β υπομονάδας της TSH, που φαίνεται να έχει εξαμερή που μοιάζουν στις περιοχές ανταπόκρισης στην Τ3 (Τ3 Response Elements–TRE’s). Έτσι μειώνεται κατεξοχήν η παραγωγή της β-υπομονάδας, και εν μέρει της α-υπομονάδας.
Η αναστολή της σύνθεσης της β-υπομονάδας της TSH επιτυγχάνεται σε μικρότερο βαθμό και από την Τ4, μέσω της μετατροπής της σε Τ3 από την αποϊωδινάση 2.
Η Τ3 αναστέλλει την ενεργοποιητική δράση της TRH μέσω μείωσης του ενδοκυττάριου ασβεστίου στους TRH νευρώνες, πράγμα το οποίο ανεξάρτητα μπορεί να είναι η αιτία μείωσης της TSH.
Σύμφωνα με τα προαναφερθέντα, η διαδικασία αυτή είναι το σημαντικότερο βήμα για τη διατήρηση σταθερών επιπέδων των θυρεοειδικών ορμονών στην κυκλοφορία.
Βιβλιογραφία
1. Dietrich JW, Landgrafe G, Fotiadou EH: TSH and Thyrotropic agonists: key actors in thyroid homeostasis J Thyroid Res. 2012;2012:351864. Epub2012 Dec 30.
2. Lechan, Ronald M, Fekete C: Feedback regulation of thyrotropin-releasing hormone (TRH): mechanisms for the non-thyroidal illness syndrome J Endocrinol Invest 2004; 27(6 Suppl):105-19.
3. Dietrich JW, Tesche A, Pickardt CR, Mitzdorf U: Thyrotropic Feedback Control: Evidence for an additional ultrashort feedback loop from fractal analysis. Cybernetics and Systems 2004; 35 (4)S : 315-331.
4. Boler J, Enzmann F, Folkers K, Bowers CY, Schally AV: The identity of chemical and hormonal properties of the thyrotropin releasing hormone and pyroglutamyl-histidyl-proline amide. Biochem Biophys Res Commun 1969; 37(4):705-10.
5. Burgus R, Dunn TF, Desiderio D, Guillemin R: Molecular structure of the hypothalamic hypophysiotropic TRF factor of ovine origin: mass spectrometry demonstration of the PCA-His-Pro-NH2 sequence. C.R. Hebd Seances Acad Sci, Ser. D, Sci.Nat. 269 (19):1870-3.
6. Wikipedia, Thyrotropin-releasing hormone.
7. K.Τερζίδης, Μ. Αλεβιζάκη. Ρυθμιστικός ρόλος της TSH. Μετεκπαιδευτικά μαθήματα ΕΕΕ 2011: παθήσεις θυρεοειδή.
8. Marangell LB, George MS, Callahan AM, Ketter TA, Pazzaglia PJ, L’Herrou TA et al: Effects of intrathecal thyrotropin-releasing hormone (protirelin) in refractory depressed patients. Arch Gen Psychiatry 1997; 54 (3): 214-22.
9. Army anti-suicide initiative brings $3 million to IU School of Medicine scientists’ research. Indiana University School of medicine. July 24, 2012.
10. Nillni EA: Neuroregulation of proTRH biosynthesis and processing. Endocrinology 1999; 10 (3) 185-99.
11. Sun Y, Lu X, Gershengorn MC: Thyrotropin-releasing hormone receptors: similarities and differences. J Mol Endocrinol 2003; 30: 87-97.
12. Mariotti 2006; Normal physiology of the hypothalamo-pituitary-thyroidal system and relation to the neural system and other endocrine gland. Chap4. Thyroid Disease Manager. (http://www.thyroidmanager.org).
13. Refetoff S: Resistance to thyrotropin. J Endocrinol Invest 2003; 26: 770.
14. Camilot M, Teofoli F, Gandini A et al: Thyrotropin receptor gene mutations and TSH resistance: variable expressivity in the heterozygotes. Clin Endocrinol (Oxf) 2005; 63:146.
Created:October 21, 2014
Last update:October 21, 2014