Σοφία Τσελένη-Μπαλαφούτα
Καθηγήτρια Παθολογικής Ανατομικής
Α Εργαστήριο Παθολογικής Ανατομικής ΕΚΠΑ
Eισαγωγή
Η βιοψία με λεπτή βελόνη (Fine Needle Aspiration, FNA) έχει πλέον καθιερωθεί ως το πλέον χρήσιμο εργαλείο στην ανίχνευση του θυρεοειδικού καρκίνου και ταυτόχρονα ως το πλέον αξιόπιστο και χαμηλού κόστους εργαστηριακό τέστ, για αυτό και αποτελεί τον θεμέλιο λίθο στις περισσότερες κατευθυντήριες οδηγίες για το χειρισμό των θυρεοειδικών όζων (1). Μετά την εισαγωγή της μεθόδου στην διαγνωστική ρουτίνα το ποσοστό των κακοηθειών στο χειρουργικό υλικό παρουσίασε δραματική μείωση, σαν αποτέλεσμα ακριβέστερης επιλογής για χειρουργική αντιμετώπιση των υπόπτων όζων. Παρ όλα αυτά η μέθοδος δεν αποτελεί πάντα ανεξάρτητο διαγνωστικό εργαλείο, δεδομένης της σημασίας να αξιολογούνται τα κυταρολογικά ευρήματα σε σχέση με τα κλινικά και τα απεικονιστικά ευρήματα. Είναι εξαιρετικά χρήσιμο ο κυταροπαθολόγος να γνωρίζει την κλινική αξιολόγηση κάθε ευρήματος ο δε κλινικός να είναι ενήμερος για την αξιοπιστία των ευρημάτων, για τις δυνατότητες και τους περιορισμούς της μεθόδου, να κατανοεί δε τη στοιχειώδη κυταρολογική ορολογία (2).
1. Διαγνωστική προσέγγιση των θυρεοειδικών όζων με βιοψία με λεπτή βελόνα
1.1. Ενδείξεις και στόχοι της βιοψίας
Με βάση διεθνείς κατευθυντήριες οδηγίες για το χειρισμό των θυρεοειδικών όζων ένδειξη για βιοψία υπάρχει για όλους τους όζους που υπερβαίνουν το 1 εκ. σε διάμετρο και για μικρότερους όζους, εφόσον είναι υπερηχογραφικά ύποπτοι (1). Δεν αναφέρεται κατώτερο όριο στη διάμετρο υπόπτων όζων, ωστόσο στην πράξη διαπιστώνεται μία δυσχέρεια στη λήψη υλικού για όζους με διάμετρο μικρότερη των 5 χιλ.
Οι συνήθεις στόχοι για βιοψία είναι:
- Να διαγνωσθεί ένας επιθετικός όγκος και να τεθεί έστω υπόνοια για ένα όγκο χαμηλής κακοήθειας μέσα στην πληθώρα των θυρεοειδικών όζων
- Να επιβεβαιωθεί η διάγνωση μιας καλοήθειας ώστε να κατοχυρωθεί ο κλινικός που προτείνει συντηρητική αγωγή
- Να αναγνωρισθεί ή έστω να τεθεί η υπόνοια για κάποιους ιστολογικούς τύπους που απαιτούν τροποποιημένη αντιμετώπιση (μυελοειδές καρκίνωμα,λέμφωμα, αναπλαστικό καρκίνωμα, μεταστατικό στο θυρεοειδή νεόπλασμα)
- Να επιβεβαιωθεί κάποια διάγνωση διάχυτης διόγκωσης όπως υποξείας ή αυτοάνοσης θυρεοειδίτιδας
- Να ταυτοποιηθούν μετεγχειρητικές διογκώσεις της περιοχής (εάν αφορούν υπόλειμμα, υποτροπή, λεμφαδενική διόγκωση ή μετεγχειρητικό κοκκίωμα)
- Να διαγνωσθούν λοιπές αλλοιώσεις της περιοχής του τραχήλου (τραχηλικές κύστεις όπως θυρεογλωσσικού πόρου ή βραγχιακή, λεμφαδενικές διογκώσεις διογκώσεις μαλακών μορίων και ενίοτε νεοπλασίες σιελογόνων αδένων)
- Να επιβεβαιωθούν λεμφαδενικές μεταστάσεις
Στόχο της βιοψίας δεν μπορεί να αποτελούν σε μορφολογική βάση:
- Η ανίχνευση εστίας μικροκαρκινώματος
- Η τελική ταξινόμιση θυλακιώδους νεοπλάσματος
- Η διαπίστωση της επέκτασης ενός νεοπλάσματος στην κάψα του αδένα
- Ο αποκλεισμός λεμφαδενικής μετάστασης
- Η ασφαλής αναγνώριση παραθυρεοειδικής αλλοίωσης
1.2. Αντενδείξεις για βιοψία με λεπτή βελόνη
Δεν έχουν καταδειχθεί κάποιες σαφείς αντενδείξεις, δεδομένου ότι η μέθοδος είναι απλή και ασφαλής.Μία βαρειά αιμορραγική διάθεση θα μπορούσε να προκαλεσει προβληματισμό. Η χορήγηση αντιπηκτικών δεν αποτελεί αντένδειξη για τη βιοψία ωστόσο σκόπιμη είναι η διακοπή λίγες μέρες πριν την βιοψία. Σε κάθε περίπτωση αυτός που διενεργεί τη βιοψία μπορεί σε κάποιο βαθμό να μειώσει τον κίνδυνο αιμορραγίας με χρήση πιο λεπτής βελόνης, αποφυγή πολλών βιοψιων και κύρια στοχευμένες και πολύ γρήγορες κινήσεις. Η υπερηχογραφική καθοδήγηση μειονεκτεί στις περιπτώσεις αυτές εφόσον η βελόνη παραμένει περισσότερο στην αλλοίωση.
2. Τεχνική της βιοψίας
2.1. Γενική άποψη
Η φιλοσοφία της μεθόδου βασίζεται στην εισαγωγή μιας λεπτής βελόνης σε μία αλλοίωση με στόχο την αποδιοργάνωση του ιστού, την λήψη μικρότατων ιστοτεμαχιδίων και την επίστρωσή τους σε αντικειμενοφόρες πλάκες («άμεσα επιχρίσματα») ή την έκπλυση της βελόνης σε υγρό (είτε φυσιολογικό ορό είτε κάποιο μονιμοποιητικό μέσο), την φυγοκέντρηση στην συνέχεια του υγρού και την παρασκευή επιχρισμάτων από το ίζημα της φυγοκέντρησης («έμμεσα επιχρίσματα»).
Φυγοκέντρηση και επίστρωση του ιζήματος στην συνέχεια εφαρμόζεται και σε όλες τις περιπτώσεις αναρρόφησης υγρού από κυστικές αλλοιώσεις.
Παρά την φαινομενική της απλότητα η μέθοδος οδηγεί συχνά σε μη ικανοποιητικά επιχρίσματα, οφειλόμενα κυρίως σε ελλειπή εμπειρία κατά την λήψη του υλικού ή κατά την παρασκευή και την επεξεργασία των επιχρισμάτων. Είναι προφανές ότι για την επιτυχή διαγνωστική με την μέθοδο αυτή απαιτείται συνεργασία ομάδας με εμπειρία στην εντόπιση της αλλοίωσης, την προσέγγισή της με την βελόνη, την λήψη επαρκούς υλικού, την κατάλληλη επίστρωση, μονιμοποίηση και χρώση του υλικού αυτού, την μικροσκοπική αξιολόγηση των επιχρισμάτων και τέλος την συσχέτιση των ευρημάτων με τα κλινικά και τα απεικονιστικά ευρήματα.
2.2. Ποιος θα πρέπει να διενεργεί την βιοψία του θυρεοειδούς;
Το θέμα αυτό έχει κατά το παρελθόν πυροδοτήσει πολλές συζητήσεις και διαφωνίες και η μόνη έντιμη απάντηση είναι «ας παρακεντήσει όποιος μπορεί να το κάνει σωστά», δηλαδή όποιος είναι σε θέση να εντοπίσει ένα θυρεοειδικό όζο είτε ψηλαφητικά είτε με την καθοδήγηση υπερήχων και έχει εκπαιδευθεί να πάρει υλικό και να το επιστρώσει .Ετσι η βιοψία μπορεί να διενεργηθεί από κλινικό γιατρό ( κυρίως ενδοκρινολόγο ή χειρουργό του αδένα), από απεικονιστή υπερήχων ή από κυταροπαθολόγο. Αρκετές μελέτες καταδεικνύουν υψηλότερα ποσοστά επιτυχών παρακεντήσεων όταν αυτές διενεργούνται από έμπειρο κυτταροπαθολόγο για τους εξής προφανείς λόγους: Αμεση εκτίμηση της ποιότητας και της ποσότητας του υλικού, καλή επίστρωση και προσωπική εκτίμηση του κλινικού ευρήματος, συμπεριλαμβανομένης και της «αίσθησης» κατά την αναρρόφηση. Εάν υπάρχει σχετική εμπειρία έχει κανείς άμεση εκτίμηση της υφής του όζου που παρακεντά, δεδομένου ότι μαλακοί, αγγειοβριθείς όζοι διαφέρουν ως προς την αίσθηση της βιοψίας από ινώδεις ή ασβεστοποιημένους όζους, ενώ η αναρρόφηση ζελατινώδους κολλοειδούς έχει πολύ χαρακτηριστική υφή του υλικού. Σημαντική μπορεί να είναι και η πληροφορία από την παρακέντηση κύστεων σε σχέση με την ποιότητα, το χρώμα και την ποσότητα του υγρού. Κυστικά εκφυλιζόμενα θηλώδη καρκινώματα λ.χ. μπορεί να δίνουν λιγοστό «θολό» ξανθοχρωματικό υγρό σε αντίθεση με καλοήθεις εκφυλιζόμενους όζους, όπου το υγρό συνήθως είναι διαυγές, ενώ εκφυλιζόμενα ογκοκυταρικά νεοπλάσματα χαρακτηρίζονται από παχύ σοκολατόχρουν περιεχόμενο. Εφόσον διενεργεί την βιοψία ο κυτταροπαθολόγος, μπορεί να εκμεταλλευθεί και όλες τις αρχικές πληροφορίες σε συνεκτίμηση με την μικροσκοπική εικόνα των επιχρισμάτων στη συνέχεια (3).
2.3. Σχεδιασμός της βιοψίας: Επιλογή του τρόπου καθοδήγησης
Ο σχεδιασμός της διαδικασίας προυποθέτει την κλινική εξέταση του ασθενούς σε σύγκριση με τα απεικονιστικά ευρήματα του υπερηχογραφήματος .Κατ αρχήν θα πρέπει να προσδιορισθούν όλοι οι όζοι που χρήζουν βιοψίας με βάση τις υφιστάμενες κατευθυντήριες οδηγίες (1). Στην συνέχεια θα πρέπει να διαπιστωθεί εάν οι όζοι αυτοί ψηλαφώνται σαφώς και είναι αρκούντως ακινητοποιήσιμοι , ώστε μία βιοψία με ψηλάφηση να είναι αξιόπιστη ως προς την λήψη αντιπροσωπευτικού υλικού από την συγκεκριμένη αλλοίωση.Σε αντίθετη περίπτωση είναι αναγκαία η χρήση υπερήχων για την εξασφάλιση της αντιπροσωπευτικότητας. Η αξιοπιστία της ψηλάφισης εξαρτάται κύρια από την εμπειρία του ιατρού αλλά και από το μέγεθος, την εντόπιση και την υφή του όζου και τέλος από την κατασκευή του τραχήλου του ασθενούς.Σε μεγάλη εμπειρία και σε λεπτό τράχηλο είναι δυνατή η αξιόπιστη παρακέντηση ακόμη και ενός όζου μείζονος διαμέτρου 5 mm με εντόπιση στον ισθμό. Όζοι σκληρής σύστασης φηλαφώνται ευκολότερα. Σκληρή σύσταση παρατηρείται συχνά σε ίνωση και ασβεστώσεις (συνήθη ευρήματα σε θηλώδη καρκινώματα ) αλλά και σε κυστικούς, υπό τάσιν όζους, αδιακρίτως βιολογικής συμπεριφοράς. Δυσχέρεια στην ψηλάφιση εμφανίζουν γενικά όζοι εντοπιζόμενοι στην οπισθία επιφάνεια του θυρεοειδούς, καθώς και όζοι του κάτω τριτημορίου με επέκταση στο μεσοθωράκιο.Οι τελευταίοι είναι δυνατόν να ψηλαφώνται κατά την κατάποση λόγω της μετακίνησής τους κατά μήκος της τραχείας, ωστόσο συχνά είναι αδύνατη η ακινητοποίησή τους για την λήψη του υλικού. Στις περιπτώσεις αυτές ακόμη και εάν ληφθεί υλικό, υπάρχει αβεβαιότητα ως προς την δειγματοληψία των κατώτερων τμημάτων των όζων άρα ως προς την συνολική αντιπροσωπευτικότητα του υλικού. Παχύσαρκοι ασθενείς ή ασθενείς με εξαιρετικά εκπτυγμένους τους τραχηλικούς μύες (λ.χ. αθλητές), κυρίως άνδρες, αποτελούν δυσκολότερο στόχο για βιοψία με ψηλάφιση. Οι πολυοζώδεις βρογχοκήλες αποτελούν ένα ακόμη περιορισμό για την βιοψία με ψηλάφιση, δεδομένου ότι συχνά είναι δυσχερής η διάκριση των όζων ψηλαφητικά, ιδιαίτερα όταν είναι μικροί και σε επαφή μεταξύ τους. Στις περιπτώσεις αυτές πρέπει να επιστρατεύεται η υπερηχογραφική καθοδήγηση, ιδιαίτερα όταν συνυπάρχουν όζοι με καλοήθεις και όζοι με ύποπτους ηχομορφολογικούς χαρακτήρες. Η τελική απόφαση για τον τρόπο διενέργειας της βιψίας λαμβάνεται με τον ασθενή σε ύπτια θέση με υπερέκταση της τραχηλικής χώρας και ένα μικρό μαξιλάρι κάτω από τους ώμους. Ο βαθμός της υπερέκτασης διαφέρει ανάλογα με την εντόπιση του όζου και την κατασκευή του τραχήλου του ασθενούς και προσδιορίζεται ζητώντας από τον ασθενή να καταπιεί ενώ ψηλαφάται ο όζος του. Η σωστή θέση για βιοψία προυποθέτει τραχηλικούς μύες χαλαρους και σαφές ψηλαφητικό εύρημα. Τονίζεται ότι θα είναι σημαντικό να διαθέσει κανείς χρόνο για τον προσδιορισμό της σωστής θέσης και τον σχεδιασμό για την διενέργεια ασφαλούς βιοψίας, καθώς και για τον έλεγχο του ασθενούς σε όλη την διάρκεια της διαδικασίας. Εάν ο ασθενής καταπιεί η βιοψία διακόπτεται ώστε να μην παρακεντηθούν εξωθυρεοειδικές δομές. Η βιοψία εκτός του όζου έχει σαν αποτέλεσμα μη διαγνωστικό υλικό, είναι επώδυνη για τον ασθενή και επιπλέον εγκυμονεί τον κίνδυνο αιματώματος ή θεωρητικά ακόμη και τραυματισμό λ.χ. μεγαλύτερου αγγείου. Μονήρεις στον λοβό καλά ψηλαφητοί όζοι αποτελούν ιδανικό στόχο για βιοψία με ψηλάφιση. Η προσέγγιση αυτή έχει το πλεονέκτημα να είναι απλή, χαμηλού κόστους εφόσον δεν είναι απαραίτητος ο υπερηχογραφικός εξοπλισμός, και πολύ σύντομη, μειώνοντας έτσι τη δυσφορία του ασθενούς και την αιμορραγία στον όζο. Για τον λόγο αυτό ενδείκνυται ιδιαίτερα για αγγειοβριθείς όζους καθώς και για παιδιά και γενικότερα φοβισμένους ασθενείς και για ασθενείς με μειωμένη πηκτικότητα, όπως ασθενείς στους οποίους χορηγούνται αντιπηκτικά. Οι ιδανικές συνθήκες για μία ασφαλή βιοψία συνδέονται με την δυνατότητα πιθανής συνεργασίας διαφόρων ειδικοτήτων (aspiration clinic).
2.4. Βιοψία με λεπτή βελόνη: Πόσο λεπτή η βελόνη;
Εξ ορισμού βελόνες 19-27 g είναι κατάλληλες για την τεχνική της βιοψίας σε διάφορα όργανα. Ωστόσο ο θυρεοειδής είναι αγγειοβριθές όργανο και βελόνες 21 g είναι οι μεγαλύτερες αποδεκτές για το όργανο αυτό. Οι περισσότεροι παρακεντούν με βελόνες 21-25 g. Προσωπικά, θεωρώ όπως και άλλοι(4) καταλληλότερη για την αρχική βιοψία μία βελόνη 22g (εξωτερικής διαμέτρου 0,6 χιλ), δεδομένου ότι επαρκεί για την αναρρόφηση ζελατινώδους υλικού αλλά και ελαφρά ινώδους υποστρώματος χωρίς εκτεταμένη αιμορραγία σαν επιπλοκή. Μεγαλύτερες βελόνες (21g) ενδείκνυνται κύρια για την εκκένωση κυστικών αλλοιώσεων καθώς και για την βιοψία όζων με ινοπλασία ή ασβεστώσεις. Το μήκος της βελόνης είναι επίσης σημαντικό διότι εκεί παγιδεύονται τα κυτταρικά στοιχεία κατά την αναρρόφηση και κυμαίνεται μεταξύ 20-32 χιλ. Χρησιμοποιώ την βελόνη συνδεδεμένη με σύριγγα 20ml για την αναρρόφηση, προκειμένου να επιτυγχάνεται αρκετή αρνητική υποπίεση. Αλλοι θεωρούν επαρκή σύριγγα 10 ml, ενώ κάποιοι υποστηρίζουν την μέθοδο «αναρρόφηση χωρίς αναρρόφηση», χωρίς εφαρμογή υποπίεσης, λαμβάνοντας το υλικό απλά με παλινδρομικές κινήσεις μίας λεπτής βελόνης μέσα στον όζο, με βάση τον νόμο των τριχοειδών. Προσωπικά δεν έχω καλή εμπειρία με την μέθοδο αυτή σε θυρεοειδικούς όζους, ιδιαίτερα σε περιπτώσεις με παχύρρευστο κολλοειδές ή ίνωση. Ενδέχεται την μέθοδο αυτή να την προτιμήσεις κανείς σε μαλακούς αγγειοβριθείς όζους.
2.5. Περιγραφή της διαδικασίας
2.5.1. Ενημέρωση του ασθενούς
Πριν την βιοψία ο ασθενής θα πρέπει να ενημερώνεται για τον στόχο και την αναγκαιότητα της βιοψίας και την κεντρική θέση που κατέχει στον χειρισμό του όζου. Ωστόσο δεν θα πρέπει να παραλείπονται οι περιορισμοί της μεθόδου αυτής καθώς και το ενδεχόμενο μη διαγνωστικού υλικού ή ακόμη και ψευδών διαγνώσεων. Το ενδεχόμενο σπάνιων επιπλοκών δεν θα πρέπει να παραλείπεται, όπως αιμάτωμα, φλεγμονή ή επεισόδιο βαγοτονίας, ωστόσο θα πρέπει να τονίζεται η σπανιότητά τους και να μην αποθαρρύνετα ο ασθενής από την βιοψία. Προκειμένου να εξασφαλισθεί η συναίνεση και η συνεργασία του ασθενούς σκόπιμο είναι να περιγράφει κανείς σύντομα την διαδικασία και να τονίζει την ανώδυνη πλευρά. Εάν χορηγούνται αντιπηκτικά θα πρέπει να προηγηθεί της βιοψίας σύντομη διακοπή των σκευασμάτων μετά από συνενόηση με τον θεράποντα ιατρό.
2.5.2. Πόσο σκόπιμη είναι η τοπική αναισθησία;
Δεν συνιστώ την χορήγηση τοπικού αναισθητικού κυρίως διότι την θεωρώ περιττή, δεδομένου ότι η βιοψία είναι γενικά ανώδυνη και άριστα ανεκτή από τον ασθενή. Παράλληλα, αποφεύγεται μία σπάνια αλλεργική αντίδραση αλλά και μία ενδεχόμενη δυσχέρεια στην ψηλάφηση μετά την έγχυση υγρού στην περιοχή. Επίσης αποφεύγεται πρόσμιξη του αναισθητικού στο υλικό της βιοψίας που θα μπορούσε να επηρεάσει την ποιότητά του. Σε πολύ φοβισμένους ασθενείς ή σε παιδιά θα μπορούσε να προηγηθεί ένα ημίωρο πρίν την βιοψία μία επάλειψη με αναισθητική αλοιφή. Ωστόσο θεωρώ ότι καλύτερη από κάθε αναισθησία είναι για τον ασθενή μία σύντομη, σχεδιασμένη, καλά στοχευμένη διαδικασία με παράλληλη ενημέρωση ώστε να αισθάνεται ασφαλής.
2.5.3. Η τεχνική της αναρρόφησης με ψηλαφητική καθοδήγηση
Ο δεξιόχειρας γιατρός στέκεται στα δεξιά του υπτίου ασθενούς άσχετα από την εντόπιση του όζου.Μετά την απολύμανση του δέρματος και εφόσον η καθοδήγηση γίνει με την ψηλάφηση ζητούμε από τον ασθενή να καταπιεί, προκειμένου να αισθανθούμε τον όζο να κινείται και να σιγουρευτούμε για το ψηλαφητικό μας εύρημα, οπότε ακινητοποιούμε τον όζο μεταξύ του δείκτη και του μέσου δακτύλου του αριστερού μας χεριού. Στην συνέχεια ζητάμε από τον ασθενή να μην καταπιεί και τον ενημερώνουμε ότι θα αισθανθεί την είσοδο της βελόνης, την οποία εισάγουμε στον όζο με το δεξί χέρι και συνδεδεμένη με την σύριγγα (Εικόνες 1 και 2). Για την διευκόλυνση της βιοψίας κυκλοφορούν στο εμπόριο κατάλληλα μηχανικά εργαλεία όπου εφαρμοζεται η σύριγγα ωστόσο θεωρώ ότι ενώ διευκολύνουν το γιατρό στην λήψη του υλικού με το ένα χέρι, δυσχεραίνουν την ψηλαφητική αίσθηση του ερήματος και τον προσδιορισμό του βάθους της βιοψίας, ιδιαίτερα σε όζους με βαθύτερη εντόπιση. Τραβώντας γρήγορα το έμβολο της σύριγγας (μεταξύ 10-15 ml) επιτυγχάνουμε μία επαρκή αρνητική πίεση για την αναρρόφηση. Ο βαθμός της απαιτούμενης αρνητικής πίεσης εξαρτάται από την υφή του όζου και θα έπρεπε να εφαρμόζεται βαθμιαία ώστε να αποφεύγεται μεγάλη αρνητική πίεση σε πολύ αγγειοβριθείς ιστούς, και να σταματάει μόλις το αίμα εμφανισθεί στο χωνί της βελόνης. Το επόμενο σημαντικό βήμα προκειμένου να αποκτηθεί ιστικό τμήμα είναι μία γρήγορη παλινδρομική κίνηση της βελόνης μέσα στον όζο με ελαφρά απόκλιση στην κατεύθυνση, προκειμένου να αποδιοργανωθεί τοπικά η ιστική συνοχή(«needle stroke»). Η κίνηση αυτή φαίνεται να είναι σημαντικότερη από την αρνητική πίεση και επιτρέπει την λήψη υλικού σε μία ευρύτερη περιοχή (5). Κατά την διάρκεια αυτής της κίνησης ο γιατρός πρέπει να είναι ιδιαίτερα προσεκτικός η βελόνη να παραμείνει μέσα στον όζο για την λήψη αντιπροσωπευτικού υλικού. Επιπλέον θα πρέπει να παρατηρεί το χωνί της βελόνης και να σταματήσει αμέσως την αναρρόφηση μόλις εμφανισθεί εκεί το υλικό αναρρόφησης ώστε να αποφευχθούν προσμίξεις αίματος (hemodilution). Η επιθηλιακή συνιστώσα, που αποτελεί και τον κύριο στόχο της βιοψίας, αποκολλάται εύκολα με τις κινήσεις της βελόνης. Κυτταροβριθείς αλλοιώσεις, όπως αδενωματώδεις όζοι, αδενώματα και καρκινώματα δίνουν συχνά άφθονο υλικό. Δυσχέρεια στην λήψη παρατηρείται περισσότερο σε ινοπλαστικές ή ασβεστοποιούμενες αλλοιώσεις (κυρίως φλεγμονώδεις, εκφυλιστικές ή και νεοπλασματικές) καθώς και έντονα αγγειοβριθείς αλλοιώσεις (όπως υπερλειτουργικοί όζοι) λόγω μεγάλων προσμίξεων αίματος.

Εικόνα 1. Ελάχιστος εξοπλισμός για την διενέργεια βιοψίας με βελόνη.

Εικόνα 2. Ο όζος ακινητοποιείται μεταξύ δείκτη και μέσου δακτύλου του αριστερού χεριού (σε δεξιόχειρες).
Στο τέλος της βιοψίας και πριν την έξοδο της βελόνης γίνεται επαναφορά του εμβόλου και εξισορρόπιση της πίεσης. Εάν αυτό παραληφθεί, η ατμοσφαιρική πίεση θα σπρώξει το υλικό από την βελόνη στην σύριγγα και θα χαθεί.
Σε περίπτωση αναρρόφησης υγρού η αναρρόφηση συνεχίζεται μέχρι να σταματήσει να εισρέει υγρό στην σύριγγα διότι άδειασε η κύστη ή κάποιο τμήμα της αφοριζόμενο από διαφραγμάτια. Δεν συνιστώ να γίνει προσπάθεια επιπλέον εκκένωσης μετακινώντας την βελόνη διότι μπορεί να προκληθει ρήξη διαφραγματίων και εκ νέου αιμορραγία μέσα στον όζο. Κινήσεις της βελόνης δεν γίνονται επομένως κατά την διάρκεια της εκκένωσης, ωστόσο η βιοψία επαναλαμβάνεται στο τυχόν υπόλειμμα του όζου.
2.5.4. Πόσες βιοψίες πρέπει να γίνονται;
Ο αριθμός των βιοψιών ανά όζο εξαρτάται από το μέγεθος του όζου δεδομένης της ενδεχόμενης ετερογένειας του ιστικού υποστρώματος του όζου, οπότε βιοψία σε μία θέση ενδέχεται να μην είναι αντιπροσωπευτική, όπως συμβαίνει με όλες τις μικρές δειγματοληψίες. Γενικά κάθε βιοψία με τις παλινδρομικές κινήσεις παράλληλα μέσα στον όζο καλύπτει περίπου 1-1,5 εκ. ιστού. Κάθε μεγάλος όζος απαιτεί αντίστοιχα περισσότερες βιοψίες λ.χ. ένας όζος διαμέτρου 3 εκ. απαιτεί 2 βιοψίες σε απόσταση 1 εκ., προκειμένου να μην μείνει εκτός ελέγχου μία περιοχή μεγαλύτερη του 1 εκ. Μερικοί γιατροί κάνουν πάντα πολλαπλές βιοψίες. Ωστόσο πρέπει να επισημάνουμε ότι πολλαπλές βιοψίες συνεπάγονται αιμορραγία στον όζο οπότε η λήψη επιπλέον υλικού γινεται εξαιρετικά δυσχερής. Για τον ίδιο λόγο η επανάληψη μιας ανεπιτυχούς βιοψίας θα πρέπει να μην γίνεται άμεσα, ώστε να απορροφηθεί το αιμάτωμα από την πρώτη βιοψία. Σε αντίθετη περίπτωση ελλοχεύει αυξημένος κίνδυνος δεύτερης μη διαγνωστικής βιοψίας.
2.5.5. Φροντίδα του ασθενούς μετά την βιοψία
Μετά την έξοδο της βελόνης από τον όζο εφαρμόζεται τοπική πίεση για αιμόσταση κατά προτίμηση από τον ίδιο τον ασθενή με την υπόδειξη του γιατρού, για 3-5 λεπτά.Εάν ο όζος ήταν πολύ αιμορραγικός ή έγιναν πολλαπλές βιοψίες ενδέχεται να απαιτηθεί μεγαλύτερος χρόνος αιμόστασης. Ιδιαίτερα ηλικιωμένοι ασθενείς ή πάσχοντες από αυχενικό σύνδρομο θα πρέπει να σηκώνονται σταδιακά από την θέση υπερέκτασης της τραχηλικής χώρας διότι ενδέχεται να νοιώσουν παροδική ζάλη.
2.5.6. Συχνά λάθη κατά την διαδικασία αναρρόφησης
- Εάν η ακινητοποίηση του όζου δεν είναι σταθερή ενδέχεται η βελόνη να μετακινηθεί εκτός του όζου κατά την διάρκεια της βιοψίας
- Εάν δεν γίνουν οι παλινδρομικές κινήσεις της βελόνης μέσα στον όζο ενδέχεται να μην αποκολληθεί υλικό για την αναρρόφηση
- Εάν η αναρρόφηση συνεχιστεί και μετά την εμφάνιση υλικού στο χωνί της βελόνης ενδέχεται να αναρροφηθεί μεγάλη ποσότητα αίματος και να σχηματίσει πήγματα με το υλικό
- Εάν δεν εξισορροπηθεί η αρνητική πίεση πριν την έξοδο της βελόνης από τον όζο το υλικό θα χαθεί στην σύριγγα.
2.5.7. Βιοψία με υπερηχογραφική καθοδήγηση
Σε γενικές γραμμές η διαδικασία είναι η ίδια με την ψηλαφητικά καθοδηγούμενη βιοψία.Το κυριότερο πλεονέκτημα είναι η οπτική εξασφάλιση της επιλογής του όζου και το κύριο μειονέκτημα ο μακρύτερος χρόνος της διαδικασίας. Το τελευταίο ενδέχεται να προκαλέσει δυσφορία στον ασθενή αλλά και μεγαλύτερη αιμορραγία κατά την βιοψία, με συχνότερα αιμορραγικά, μη διαγνωστικά επιχρίσματα. Θα πρέπει επίσης να αποφεύγεται η πρόσμιξη ζελ στο υλικό της βιοψίας διότι προκύπτουν ιζήματα στα επιχρίσματα που καλύπτουν την κυτταρική μορφολογία.
2.5.8. Επιπλοκές της βιοψίας
Ενδοοζικά αιματώματα συμβαίνουν ενίοτε, ιδίως όταν δεν εφαρμοσθεί σωστά πίεση για αιμόσταση μετά την βιοψία, εάν η βιοψία διάρκεσε πολλή ώρα, έγιναν πολλαπλές λήψεις στον όζο ή ο ασθενής είχε μειωμένη πηκτικότητα. Επίσης ορισμένες αλλοιώσεις έχουν αυξημένο κίνδυνο αιμορραγίας ιδίως οι ογκοκυτταρικές επεξεργασίες, που καμμιά φορά οδηγούν σε πλήρη αιμορραγική νέκρωση με δυσχέρεια στην ιστολογική διάγνωση μετεγχειρητικά. Η δυσχέρεια αυτή της ιστολογικής διάγνωσης σαν post FNA αλλοίωση έχει αναφερθεί σαν η σημαντικότερη «επιπλοκή» της βιοψίας (6). Τα περισσότερα ενδοοζικά αιματώματα εμφανίζονται με οξύ πόνο, διόγκωση του όζου και ενδεχομένως δυσχέρεια στην κατάποση. Στον ασθενή θα πρέπει να συστηθεί τοπική εφαρμογή πάγου και αποφυγή ασπιρίνης ως παυσίπονου. Σπανίως απαιτείται εκ νέου παρακέντηση για εκκένωση του αίματος για την ανακούφιση του ασθενούς. Εξωθυρεοειδικά αιματώματα είναι δυνατά σε κατά λάθος βιοψία εκτός του αδένα.
Λοίμωξη αναφέρεται στην βιβλιογραφία σαν σπάνια επιπλοκή, ωστόσο με τήρηση των στοιχειωδών κανόνων αντισηψίας δεν παρατηρήσαμε ούτε μία φορά την επιπλοκή αυτή σε περισσότερες από 300.000 βιοψίες θυρεοειδούς σε πάνω από 27 χρόνια διενέργειας βιοψιών, ούτε καν σε έδαφος αιματώματος.
Η πλέον αξιοσημείωτη επιπλοκή που αντιμετωπίσαμε σπάνια είναι βαγοτονική κρίση πιθανότατα οφειλόμενη σε ερεθισμό του πνευμονογαστικού νεύρου. Συνήθως διαρκεί λίγο και ο ασθενής συνέρχεται χωρίς φαρμακευτική παρέμβαση, ωστόσο ενδομυική χορήγηση θειικής ατροπίνης λειτουργεί άμεσα σε έντονη συμπτωματολογία.
Βιοψία στην τραχεία δεν είναι αδύνατη ιδίως σε όζους με εντόπιση στον ισθμό. Ο έμπειρος ιατρός το αντιλαμβάνεται άμεσα, διότι ο ασθενής βήχει αιφνίδια και ταυτόχρονα παρατηρείται είσοδος αέρα στην σύριγγα προερχόμενη από τον αυλό της τραχείας. Σπάνια ο ασθενής αντιλαμβάνεται αιματηρά πτύελα, τα οποία μπορεί να τον θορυβήσουν, στερούνται ωστόσο κλινικής σημασίας. Το μόνο πρόβλημα που μπορεί να προκύψει από την βιοψία της τραχείας είναι λανθασμένη κυτταρολογική εκτίμηση των ευρημάτων από μή έμπειρο κυτταρολόγο, που ενδέχεται να μην σκεφτεί το ενδεχόμενο, και να υπερεκτιμήσει τα αναπνευστικά επιθήλια και την βλέννη. Ως εκ τούτου όταν ο κλινικός έχει την υπόνοια ότι παρακέντησε την τραχεία σκόπιμο έίναι να ενημερώσει τον κυτταροπαθολόγο.
3. Επεξεργασία του υλικού της βιοψίας
Υπάρχουν διάφοροι τόποι επεξεργασίας του υλικού και οι απόψεις διαφέρουν ανάλογα με την εμπειρία του καθενός στην μικροσκοπία (7,8). Με αυτή την έννοια όποιος παρακεντά θα πρέπει να ακολουθεί τις οδηγίες του κυτταροπαθολόγου που συνεργάζεται, προκειμένου να εξαντληθούν οι διαγνωστικές δυνατότητες με βάση την εμπειρία του με συγκεκριμένη χρώση. Γενικά η άμεση επίστρωση του υλικού παρέχει περισσότερες πλήροφορίες για τη μορφολογία της αλλοίωσης, αφού οι επιθηλιακές δομές καταστρέφονται λιγότερο και περιέχονται και πολλά στοιχεία του υποστρώματος καλά αξιολογούμενα.Το μειονέκτημα της άμεσης επίστρωσης είναι ότι απαιτεί ειδική εκπαίδευση στην παρασκευή των επιχρισμάτων, και προκειμένου την επίστρωση να την αναλάβει κάποιος άπειρος είναι προτιμότερα έμμεσα επιχρίσματα ή κυταρολογία υγρής φάσης (όπως λ.χ.Thin Prep). Ωστόσο τα άμεσα επιχρίσματα έχουν γενική αποδοχή σαν η προτιμητέα μέθοδος και οι περισσότερες εικόνες μικροσκοπίου στην βιβλιογραφία αναφέρονται σε καλά επιστρωμένα άμεσα επιχρίσματα.
3.1. Λήψη του υλικού της βιοψίας – Παρασκευή των επιχρισμάτων
3.1.1. Λήψη του υλικού της βιοψίας
Μετά την έξοδο της βελόνης από τον όζο η βελόνη αποσυνδέεται από την σύριγγα,και στην σύριγγα αναρροφάται αέρας (10-20 κ.εκ.) με την βοήθεια του οποίου εξάγεται το υλικό της βελόνης (αφού επανασυνδεθεί με την σύριγγα) γρήγορα πάνω στις αντικειμενοφόρες πλάκες, ανάλογα με την υφή και την ποσότητα του υλικού σε μία ή περισσότερες, ώστε να σχηματισθεί μία μέτρια σταγόνη για την περίπτωση άμεσης επίστρωσης.Εάν ο γιατρός δεν έχει εμπειρία στην άμεση επίστρωση είναι προτιμότερο να ξεπλένει το υλικό της βελόνης σε ένα υγρό μέσο ( φυσιολογικό ορό ή μονιμοποιητικό) και να το αποστέλει στο εργαστήριο για την περαιτέρω επεξεργασία και την παρασκευή έμμεσων επιχρισμάτων ή κυτταρολογία υγρής φάσης, ανάλογα με την προτίμηση του κυταροπαθολόγου (9).Το υλικό ξεπλένεται επίσης εάν υάρχει επιθυμία να εφαρμοσθεί κυταρολογία υγρής φάσης ή εάν υπάρχει απαίτηση για ανοσοιστοχημεία, οπότε σκόπιμο είναι να ξεπλένεται το υλικό σε μονιμοποιητικό όπως ακετόνη , αλκοόλ ή και φορμαλίνη προκειμένου το υγρό να φυγοκεντρηθεί και από το ίζημα να παρασκευασθούν κύβοι κυτάρων εγκλεισμένοι σε παραφίνη (cell block) για την κοπή σειριακών τομών και εφαρμογή ανοσοιστοχημείας (10).
Σε περίπτωση που αναρροφηθεί υγρό επίσης μπορεί να προωθηθεί απευθείας για κυταρολογία υγρής φάσης ή να φυγοκεντρηθεί σε 1500 rpm (400X g) επί 5 περίπου λεπτά, και στην συνέχεια να παρασκευασθούν επιχρίσματα από το ίζημα της φυγοκέντρησης.Συχνά ωστόσο είχαμε επαρκές κυτταρικό υλικό για άμεση επίστρωση αποσυνδέοντας την βελόνη από την σύριγγα και εξωθώντας κυταρικό υλικό που έχει συγκρατηθεί στην βελόνη με μία καθαρή σύριγγα με αέρα πάνω σε αντικειμενοφόρο πλάκα προκειμένου να επιστρωθεί.
3.1.2. Άμεση επίστρωση επιχρισμάτων
Προκειμένου να επιστρωθεί άμεσα το υλικό θα πρέπει να εξάγεται από την βελόνη σε μία αντικειμενοφόρο πλάκα και σε απόσταση 0,5-1 εκ. από το εσμύρισμα γραφής του πλακιδίου προκειμένου να αφεθεί χώρος στην υπόλοιπη πλάκα για την επίστρωση. Κατά την εξαγωγή του υλικού η μύτη της βελόνης θα πρέπει να άπτεται της πλάκας ώστε το υλικό να βγεί ομοιόμορφα σε μία σταγόνη, η οποία θα πρέπει να είναι τόσο μεγάλη ώστε να επαρκέσει για μία ομοιόμορφη επίστρωση και τόσο μικρή ώστε να επιστρωθεί το υλικό χωρίς να χυθεί από την πλάκα (απαιτείται εκμάθηση για την εκτίμηση του μεγέθους της σταγόνης) (Εικόνα 3) Η επίστρωση γίνεται με μία άλλη αντικειμενοφόρο πλάκα, μία μόνο φορά και με τον τρόπο απογείωσης του αεροπλάνου (Εικόνα 4). Η πίεση με την οποία θα πρέπει να γίνει η επίστρωση απαιτεί εμπειρία, ώστε το επίχρισμα να μην είναι πολύ παχύ ώστε να μην αξιολογείται, ούτε όμως η πίεση να συνθλίψει τα κύτταρα. Σημειώνεται ότι επιχρίσματα από αιμορραγικό υλικό είναι συχνά ακατάλληλα δεδομένου ότι τα κύτταρα εγκλωβίζονται σε αιματόπηγμα και δεν είναι αξιολογήσιμη η μορφολογία τους. Το σωστό επίχρισμα χαρακτηρίζεται συνήθως από αποστρογγυλεμένο το ένα του άκρο.

Εικόνα 3. Εξαγωγή του υλικού-Η βελόνη εφάπτεται της αντικειμενοφόρου.

Εικόνα 4. Επίστρωση του υλικού με δεύτερη αντικειμενοφόρο ( «σαν απογείωση»).
Την επίστρωση ακολουθεί άμεση σήμανση των πλακιδίων με το ονοματεπώνυμο του ασθενούς και το νούμερο της βιοψίας με βάση αρίθμηση των βιοψιών που κατά προτίμηση θα αποτυπώνεται ευκρινώς σε ένα πρόχειρο σχέδιο του αδένα με την τοπογραφία των όζων. Περισσότερες βιοψίες στον ίδιο όζο θα πρέπει να σημειώνονται με ιδιαίτερη αρίθμηση λόγω της σημασίας που έχει για την εκτίμηση του όζου η πιθανή ετερογένεια της υφής. Η σήμανση θα πρέπει να γίνεται με μολύβι και να είναι ιδιαίτερα ευκρινής, αφού τα επιχρίσματα εμβαπτίζονται στην συνέχεια σε χρωστικές. Η ιδιαίτερη σήμανση των όζων έχει σημασία κυρίως σε περίπτωση ανεπαρκούς υλικού σε ένα από τους όζους, διότι έτσι γνωρίζει ο γιατρός σε ποιόν όζο απαιτείται επανάληψη της βιοψίας. Επίσης σκόπιμο είναι να σημειώνονται ειδικά στοιχεία, λ.χ. μία κατά λάθος παρακέντηση της τραχείας.
Επισημαίνω την σημασία της αξιόπιστης σήμανσης , η οποία δεν μπορεί να αφήνεται σε μη εκπαιδευμένο ή αναξιόπιστο προσωπικό. Λάθος ονοματεπώνυμο μπορεί να έχει ως συνέπεια λανθασμένο χειρισμό .Συνιστώ το ονοματεπώνυμο να αναγράφεται στις τομές ΜΕΤΑ την βιοψία και μετά παραίνεση του ασθενούς να επαναλάβει το όνομά του. Σε κάθε αλλαγή ασθενούς πλακίδια χρησιμοποιημένα ή απλωμένα στο τραπεζάκι πρέπει να απομακρύνονται, ώστε να εξασφαλίζεται η καθαριότητα των πλακιδίων, τα οποία πρέπει να διατηρούνται καθαρά για αποφυγή προσμίξεων από κυτταρικά στοιχεία προερχόμενα από προηγούμενους ασθενείς, από τα χέρια του προσωπικού κ.λ.π.
3.1.3. Μονιμοποίηση και χρώση των επιχρισμάτων
Τα άμεσα επιχρίσματα μονιμοποιούνται είτε ξηρά (στέγνωμα στον αέρα) είτε υγρά σε κάποιο μονιμοποιητικό λ.χ. αλκοόλη. Προκειμένου η χρώση να είναι επιτυχής θα πρέπει η μονιμοποίηση να γίνει γρήγορα. Ετσι εάν τα επιχρίσματα περιέχουν αρκετό υγρό ,χρήσιμο είναι για γρήγορο στέγνωμα να χρησιμοποιηθεί στεγνωτήρας αέρα, εάν έχει επιλεγεί ξηρή μονιμοποίηση (αποφυγή wet artifacts). Εξάλλου για υγρή μονιμοποίηση η γρήγορη εφαρμογή του μονιμοποιητικού θα συμβάλλει στην αποφυγή ξήρανσης των επιχρισμάτων(drying artifacts).
Μετά την μονιμοποίηση τα επιχρίσματα χρώνυνται ανάλογα (11). Για τα ξηρά επιχρίσματα ενδείκνυνται χρώσεις τύπου Romanowsky, είτε ταχείες χρώσεις όπως Diff Quick ή Hemacolor ή η πλέον ποιοτική χρώση May Gruenwald Giemsa (MGG) .Τα υγρά επιχρίσματα χρώννυνται συνήθως κατά Παπανικολάου, ωστόσο κάποιοι, κυρίως ιστοπαθολόγοι, προτιμούν την χρώση αιματοξυλίνης ηωσίνης λόγω της προφανούς ομοιότητας της μορφολογίας με τις ιστολογικές τομές. Η ξηρή μονιμοποίηση και η χρώση May Gruenwald Giemsa διαθέτει εξαιρετικά πλεονεκτήματα, για αυτό και οι περισσότερες εικόνες σε κυτταρολογικούς άτλαντες βιοψίας με βελόνη αφορούν την χρώση αυτή, βεβαίως και διότι είναι η χρώση που πρωτοχρησιμοποιήθηκε. Πέραν αυτού αναδεικνύει με εξαιρετικό κοντράστ το υπόστρωμα (κολλοειδές, λεμφοκύτταρα, νέκρωση), σημείο εξαιρετικά κρίσιμο για την ερμηνεία στη βιοψία του θυρεοειδούς, καθώς και την μορφολογία του κυτταροπλάσματος ενώ υστερεί στην ανάδειξη της μορφολογίας του πυρήνα σε σχέση με την χρώση Παπανικολάου. Εφόσον οι χρώσεις είναι συμπληρωματικές ιδανικό θα ήταν να διατίθενται και οι δύο. Ωστόσο συχνά το υλικό είναι περιωρισμένο και θα πρέπει να επεξεργάζεται ανάλογα με την προτίμηση και την εμπειρία αυτού που θα μικροσκοπήσει τα επιχρίσματα. Εδώ θα ήθελα να τονίσω ιδιαίτερα την σημασία της άριστης χρώσης των επιχρισμάτων προκείμένου να εξαντληθεί η διαγνωστική ακρίβεια της μεθόδου. Ωρισμένα εργαστήρια με πολύ υψηλά ποσοστά μη διαγνωστικών βιοψιών ενδέχεται να μην πάσχουν στην λήψη αλλά στην επεξεργασία των υλικών.
3.1.4. Συμπληρωματικές τεχνικές
Εάν υπάρχει διαγνωστική εμπειρία του κυτταροπαθολόγου σπάνια είναι απαραίτητες συμπληρωματικές τεχνικές, οι οποίες ανεβάζουν και το κόστος της μεθόδου αλλά και τον χρόνο αναμονής της διάγνωσης. Ωστόσο ανοσοιστοχημικές και τελευταία μοριακές μέθοδοι μπορεί να είναι υποβοηθητικές της διάγνωσης.
Ανοσοιστοχημικές εφαρμογές. Η ανοσοιστοχημεία είναι περισσότερο τέχνη παρά επιστήμη και η ερμηνεία της προυποθέται άριστο σταντάρισμα στο εργαστήριο και ακριβή γνώση του τρόπου αξιολόγησης κάθε ανιχνευόμενου αντιγόνου, σε αντίθετη περίπτωση μπορεί να παρασύρει σε λανθασμένες διαγνώσεις. Η εφαρμογή σε επιχρίσματα είναι ακόμη δυσκολότερη δεδομένης της σύνθλιψης των κυτάρων κατά την επίστρωση, ιδιαίτερα για κυταροπλασματικά αντιγόνα, και απαιτεί υψηλής ποιότητας επίστρωση. Για αυτό είναι προτιμότερη η εφαρμογή της σε κυταρικούς κύβους παραφίνης (cell blocks)
Η ανίχνευση καλσιτονίνης-συναπτοφυσίνης-χρωμογρανίνης-θυρεοσφαιρίνης-TTF 1 –παραθορμόνης ενδέχεται να βοηθήσει στην επιβεβαίωση διάγνωσης μυελοειδούς καρκινώματος, στην αναγνώριση παραθυρεοειδικού αδενώματος και σε κάποιες περιπτώσεις μεταστατικών καρκινωμάτων. Επίσης μπορεί κανείς με ανοσοιστοχημεία να ελέγξει την κλονικότητα λεμφικού πληθυσμού σε υπόνοια λεμφώματος(12). Σε επιχρίσματα δεν έχει βοηθήσει η ανοσοιστοχημεία στην διάγνωση οριακών ή υπόπτων αλλοιώσεων, λόγω της χαμηλής ευαισθησίας ή ειδικότητας προτεινόμενων κατά καιρούς δεικτών (λ.χ. το ΗΒΜΕ 1 είναι αρκετά ειδικό για το θηλώδες καρκίνωμα, ωστόσο με εστιακή θετικότητα και με υψηλές απαιτήσεις στην μικροσκοπική αξιολόγηση, που είναι ακόμη δυσχερέστερη σε επιχρίσματα λόγω της μεμβρανικής εντόπισης του αντιγόνου)
Μοριακές τεχνικές. Μοριακές τεχνικές είναι περισσότερα υποσχόμενες σε επίπεδο οριακών επιχρισμάτων. Η ανίχνευση της μετάλλαξης V 600 του Braf έχει υψηλή ειδικότητα, περιωρισμένη ωστόσο ευαισθησία, ώστε το αρνητικό εύρημα δεν κατοχυρώνει αρνητική διάγνωση. Η ανίχνευση της μετάλλαξης φαίνεται να έχει νόημα σε μικρούς ασαφείς όζους που υπάρχει κατ αρχήν η πρόθεση για στάση αναμονής και επανελέγχου. Το κύριο πρόβλημα είναι κατά την γνώμη μου ότι η μετάλλαξη ανιχνεύεται κύρια σε όζους με χαρακτηριστική μορφολογία, ενώ είναι απάνια έως απούσα στην θυλακιώδη ποικιλία του θηλώδους καρκινώματος, που αποτελεί συνήθως και το διαγνωστικό πρόβλημα. Τεχνικές που συνεκτιμούν περισσότερους δείκτες (μοριακά τέστς) ενδεχομένως έχουν μεγαλύτερη χρησιμότητα στις περιπτώσεις αυτές, ωστόσο έχουν υψηλό κόστος, υψηλές απαιτήσεις μεταφοράς του υλικού σε εξειδικευμένα εργαστήρια και αναμένεται η αξιολόγηση της αξιοπιστίας τους σε μεγάλες σειρές.
4. Κυτταρολογική αξιολόγηση
Η αξιολόγηση των επιχρισμάτων μοιάζει με την διαδικασία σύνθεσης ενός παζλ, όπου τα κομμάτια του παζλ αποτελούν τα στοιχεία του ξεριζωμένου και επιστρωμένου ιστού. Ο κυτταροπαθολόγος θα πρέπει να τα χρησιμοποιήσει για την ανασύσταση της αρχικής εικόνας (παθολογικό υπόστρωμα). Εννοείται ότι πρέπει για αυτό να διαθέτει πλήρη γνώση των δυνατών παθολογικών υποστρωμάτων («ζητούμενες δυνατές εικόνες») και συνθετική φαντασία. Όταν τα κομματάκια του παζλ δεν επαρκούν για την σύνθεση της εικόνας προκύπτει ένα μη διαγνωστικό υλικό, ενώ όταν με τα κομματάκια είναι δυνατή η σύνθεση περισσοτέρων της μιας εικόνων το αποτέλεσμα δεν είναι παθογνωμονικό. Άλλοτε μεταξύ κομματιών που συνθέτουν μία αθών εικόνα παρεμβάλλονται λιγοστά κομματάκια που αντιστοιχούν σε ένα ύποπτό υπόστρωμα, οπότε καταλήγουμε σε ένα «εστιακά ύποπτο» επίχρισμα. Τα κύρια κομματάκια που περιλαμβάνονται στο επίχρισμα θα πρέπει να ανφέρονται στην περιγραφή και οι κλινικοί γιατροί σκόπιμο είναι να έχουν βασικές γνώσεις για την κατανόηση της αλλοίωσης και των ενδεχόμενων λαθών, δεδομένου πως τα διάφορα στοιχεία συνδέονται με διαφόρου βαθμού ειδικότητα και διαγνωστική αξιοπιστία (13).
4.1. Κυτταρολογική περιγραφή επιχρισμάτων
4.1.1. Μη ειδικά στοιχεία
Άμορφα στοιχεία υποστρώματος. Κολλοειδές, αμυλοειδές, ινώδη στοιχεία, ψαμμώδη σωμάτια.
Κυτταρικά στοιχεία. Αίμα (παρόν στα περισσότερα επιχρίσματα, ιδιαίτερα σε αγγειοβριθείς αλλοιώσεις), φλεγμονώδη κύτταρα (συνήθως λεμφοκύτταρα), φαγοκύτταρα (ιστιοκυταρικά στοιχεία με φαγοκυταρωμένα κοκκία, ενδεικτικά κυστικής εκφύλισης), πολυπύρηνα γιγαντοκύτταρα (ευμεγέθη σε υποξεία θυρεοειδίτιδα, μικρότερα σε θυρεοειδίτιδα Hashimoto και θηλώδες καρκίνωμα), σπάνια προσμίξεις από μη θυρεοειδικά μόρια όπως λιποκύτταρα, γραμμωτές μυικές ίνες ή αναπνευστικά επιθήλια σε βιοψία της τραχείας).Μη ειδικά κυτταρικά στοιχεία δεν στοιχειοθετούν τελική διάγνωση, ενδέχεται ωστόσο να είναι ενδεικτικά κάποιας βλάβης λ.χ. η παρουσία αναγεννητικών γραμμωτών μυικών στοιχείων παρατηρείται κύρια σε καρκινώματα που διηθούν τους μύες.
4.1.2. Κυτταρικά στοιχεία που στοιχειοθετούν διάγνωση
Θυλακικά κύτταρα. Σε καλοήθεια συνήθως είναι ελεύθερα ή διατάσσονται σε μονοστοιβάδωση και έχουν ομοιόμορφους, υποστρόγγυλους, μικρούς πυρήνες και λιγοστό κυταρόπλασμα με ασαφή όρια. Λειτουργικού τύπου ατυπία με ανισοκαρύωση και υπερχρωματικούς πυρήνες μπορεί να εμφανισθεί σε οζώδη υπερπλασία και περισσότερο σε αυτοάνοση θυρεοειδίτιδα, ενώ σποραδικοί υπερμεγέθεις πυρήνες είναι ενδεικτικοί λήψης αντιθυρεοειδικών σκευασμάτων.
Ογκοκύτταρα (οξύφιλα κύταρα). Οξύφιλη μετατροπή του θυλακικού επιθηλίου (μετάπλαση)είναι συχνή σε αυτοάνοση θυρεοειδίτιδα σε ενήλικες αλλά είναι δυνατή και σε υπερπλαστικούς όζους. Μεταπλαστικά επιθήλια χαρακτηρίζονται από άφθονο, οξύφιλο, κοκκιώδες κυτταρόπλασμα με σαφή όρια και καλή κυταρική συνοχή. Ενδέχεται να συνυπάρχει κάποιου βαθμού πυρηνική ατυπία, που οδηγεί μερικές φορές σε υπερδιάγνωση. Αφετέρου οξύφιλα κύτταρα θηλώδους καρκινώματος υποδιαγνώσκονται μερικές φορές σαν μεταπλαστικά.
Παραθυλακικά κύτταρα. Συνυπάρχουν κάποιες φορές σε επιχρίσματα ,ωστόσο συνήθως είναι λιγοστά και ταυτοποιούνται δύσκολα σε μορφολογική βάση. Πρόκειται για αραιοχρωματικά κύτταρα με υποστρόγγυλους πυρήνες και αζουρόφιλη διακριτική κοκκίωση (νευροενδοκρινή εκκριτικά κοκκία).
Παραθυρεοειδικά κύτταρα (θεμέλια ή οξύφιλα). Μορφολογικά δεν διαχωρίζονται σαφώς από τα θυλακικά.
Πλακώδη κύτταρα. Μπορεί να αφορούν είτε θέσεις πλακώδους μετάπλασης είτε επικάλυψη κάποιας τραχηλικής κύστης (λ.χ. θυρεογλωσσικού πόρου).
Νεοπλασματικά κύτταρα. Τα νεοπλασματικά κύτταρα του θυρεοειδούς επιδεικνύουν κάποιου βαθμού επιθηλιακή διαφοροποίηση, αφού οι συνηθέστερες πρωτοπαθείς νεοπλασίες του θυρεοειδούς αφορούν καρκινώματα. Δεύτερη σε συχνότητα νεοπλασία είναι το θυρεοειδικό λέμφωμα. Μεσεγχυματικοί όγκοι είναι εξαιρετικά σπάνιοι. Τα θυρεοειδικά καρκινώματα διαφέρουν εξαιρετικά ως προς τα φαινοτυπικά τους χαρακτηριστικά με έναευρύ φάσμα από κυτταρικά στοιχεία άριστης διαφοροποίησης, που μιμούνται σε τέτοιο βαθμό το θυλακικό κύτταρο ώστε να είναι σχεδόν αδύνατη η αναγνώριση της νεοπλασματικής του φύσης, έως κυταρικά στοιχεία μεγάλης πολυμορφίας και ατυπίας (σε αναπλαστικά καρκινώματα). Ενδιάμεσες κυταρικές μορφολογίες αντιστοιχούν σε ενδιάμεσους φαινοτύπους, που εμφανίζουν ως γνωστό μεγάλη ποικιλία, με αποτέλεσμα δυσχέρειες στην τυποποίηση των θυρεοειδικών νεοπλασματων και σε ιστολογικό επίπεδο.
4.2. Βασικά ιστικά πρότυπα ανάπτυξης σε επιχρίσματα του θυρεοειδούς
H εκτίμηση όλων των παραμέτρων σε σχέση με την ποσότητα και την διάταξη των κυτταρικών στοιχείων οδηγεί στην αναγνώριση ενός ιστικού πρότυπου που πιθανότερα αντιστοιχεί στην αλλοίωση με κυριότερα τα εξής βασικά πρότυπα
Μεγαλοθυλακιώδες πρότυπο. Αποτελεί το πρότυπο της καλοήθειας με σπάνιες εξαιρέσεις (κύρια την μακροθυλακιώδη ποικιλία του θηλώδους καρκινώματος). Τα επιχρίσματα χαρακτηρίζονται από άφθονο παχύ κολλοειδές και θυλακικά κύτταρα με μικρούς πυρήνες ελεύθερα, σε μονοστοιβάδωση και τρισδιάστατες μικροθυλακιώδεις δομές, με παρουσία συχνά κυστικής εκφύλισης (με πολλά φαγοκύτταρα με κοκκία χρωστικής).
Μικροθυλακιώδες («κυτταροβριθές») πρότυπο. Περιλαμβάνει την «γκρίζα ζώνη».Τα επιχρίσματα περιέχουν λιγοστό κολλοειδές και πολλά θυλακικά κύτταρα, κυρίως σε θυλακιώδη διάταξη γύρω από κενό κέντρο, ή σε συμπαγείς αθροίσεις. Συχνή ανισοκαρύωση και εστιακή ατυπία. Η εικόνα αντιστοιχεί σε ένα «αδενωματώδη όζο», και η διαφορική διάγνωση σε ιστολογικό επίπεδο βασίζεται στην παρουσία ή όχι περιφερικής κάψας και η ενδεχόμενη διήθησή της από τα επιθηλιακά στοιχεία. Αφού το κριτήριο της διήθησης είναι το κλειδί για την διαφορική διάγνωση και το κριτήριο αυτό απουσιάζει σε τυχαίο δείγμα της βιοψίας με βελόνη, είναι προφανές ότι ο διαχωρισμός καλοήθειας από κακοήθεια δεν είναι δυνατός με την μέθοδο αυτή. Η «θυλακιώδης αλλοίωση» λοιπόν είναι μοιραία ο κύριος περιορισμός στην βιοψία.
Πρότυπο κυστικής εκφύλισης. Χαρακτηρίζεται από την παρουσία αφθόνων φαγοκυτάρων. Από στατιστική άποψη η πλεινότητα των κυστικών όζων αφορά καλοήθεις όζους, ιδίως σε συνύπαρξη κολλοειδούς, ωστόσο η περίπτωση κυστικά εκφυλιζόμενου νεοπλάσματος (κύρια θηλώδους και ογκοκυταρικού) πρέπει να περιλαμβάνεται στις πιθανές εκδοχές. Την επιβεβαίωση της καλοήθειας την παρέχει η παρουσία διατηρημένων θυλακικών κυττάρων, που υποδεικνύουν το παθογνωμονικό υπόστρωμα.
Φλεγμονώδες πρότυπο. Αφορά βασικά επιχρίσματα αυτοάνοσης θυρεοειδίτιδας με κυτταροβρίθεια οφειλόμενη κυρίως σε λεμφοκυτταρικά στοιχεία διαφόρου ωρίμανσης, με παρουσία στοιχείων από τα βλαστικά κέντρα των λεμφοζιδίων, και επιθηλιακά στοιχεία με την μορφή κλασσικού θυλακικού κυττάρου ή ογκοκυττάρου. Η παρουσία των επιθηλιακών κυττάρων επιβεβαιώνει και την αντιστοιχία σε θυρεοειδικό παρέγχυμα, δεδομένου ότι κάποιες φορές υπάρχει αμφιβολία, εάν πρόκειται για όζο ή παρακείμενο λεμφαδένα. Η παρουσία ιστιοκυτάρων με ευμεγέθη πολυπύρηνα γιγαντοκύτταρα σε συρροή με αντιστοιχία κοκκιώματος είναι διαγνωστική για υποξεία θυρεοειδίτιδα, η απουσία τους ωστόσο δεν την αποκλείει, ιδιαίτερα εάν βρίσκεται σε στάδιο αποδρομής ή έχει χορηγηθεί κορτιζόνη, η οποία αποδιοργανώνει τα κοκκιώματα. Στοιχεία οξείας θυρεοειδίτδας (πολυμορφοπύρηνα) είναι σπανιότατα και περισσότερο πιθανά σε φλεγμαίνουσα κύστη θυρεογλωσσικού πόρου. Αραιά λεμφοκυτταρικά στοιχεία είναι συχνά και σε υπερπλαστικούς όζους και έχουν αναφερθεί συχνότερα σε όζους που αυξάνουν το μέγεθός τους(14).
Νεοπλασματικά πρότυπα. Κυτταροβριθή συνήθως πρότυπα (εκτός από νεκρωτικά υψηλής κακοήθειας καρκινώματα ή ινοποιούμενα καρκινώματα), χωρίς παρουσία κολλοειδούς, με διαφορετικούς κυτταρικούς φαινοτύπους και διαφορετικές διατάξεις ανάλογα με τον νεοπλασματικό τύπο και υπότυπο. Συχνότερα αρχιτεκτονικά πρότυπα είναι το θηλώδες πρότυπο (σε θηλώδες καρκίνωμα), το μικροθυλακιώδες (κυρίως στα θυλακιώδη νεοπλάσματα αλλά και σε θηλώδες καρκίνωμα θυλακιώδους ποικιλίας), το συμπαγές (σε χαμηλής διαφοροποίησης θυλακιοκυτταρικό καρκίνωμα , σε ογκοκυτταρικά νεοπλάσματα, σε πλακώδη, σε ποικιλίες του θηλώδους και στο μυελοειδές καρκίνωμα) και το διάχυτο (αναπλαστικό καρκίνωμα, μυελοειδές καρκίνωμα, λέμφωμα)
Το μη διαγνωστικό επίχρισμα. Κάθε επίχρισμα που στερείται ειδικών κυταρικών στοιχείων(κύρια θυλακιών κυτάρων),που έχουν μονιμοποιηθεί και χρωσθεί κατάλληλα και επαρκούν για μονοσήμαντη διάγνωση ή έστω για διαφορική διάγνωση, θα πρέπει να χαρακτηρίζεται σαν μη διαγνωστικό και όχι σαν «αρνητικό για κακοήθεια», λόγω της απουσίας νεοπλασματικών κυτάρων, δεδομένου μάλιστα ότι η αναλογία νεοπλασμάτων φαίνεται αυξημένη σε μη διαγνωστικά επιχρίσματα (2). Ο κλινικός θα πρέπει στην περίπτωση αυτή να χειρισθεί τον ασθενή ανάλογα με τα λοιπά ευρήματα επαναλαμβάνοντας την βιοψία κατά το δοκούν (15,16). Τα περισσότερα μη διαγνωστικά επιχρίσματα αποτελούνται από αίμα με ενδεχόμενες κυτταρικές αθροίσεις εγκλωβισμένες σε πήγματα και για αυτό αδύνατο να αξιολογηθούν, ή υλικά από κύστεις με φαγοκύτταρα σε απουσία θυλακικών κυττάρων. Ωστόσο όχι σπάνια τα επιχρίσματα είναι μη διαγνωστικά λόγω κακής επίστρωσης (λ.χ. πολύ παχειά ή κακοεπιστρωμένα επιχρίσματα) ή επεξεργασίας. Το ποσό των απαιτούμενων κυττάρων διαφέρει ανάλογα με το είδος και το μέγεθος της αλλοίωσης, την υπερηχογραφική εικόνα και την εμπειρία του κυτταροπαθολόγου, και καμμία από τις κατά καιρούς δημοσιευμένες προτάσεις για καθορισμό ενός ελάχιστου αριθμού δεν έχει γίνει ευρύτερα αποδεκτή. Ακόμη και με μία κυτταρική άθροιση μπορεί λ.χ. να διαγνωσθεί ένα θηλώδες καρκίνωμα, εάν έχει τυπικούς χαρακτήρες και ο κυτταροπαθολόγος σαφή εικόνα του ευρήματος. Πάντως ο κλινικός πρέπει να αποδέχεται τον περιορισμό του μη διαγνωστικού επιχρίσματος και να μην ασκεί πίεση στον κυτταροπαθολόγο να υπερβεί τα διαγνωστικά του όρια, διότι ενεδρεύει μία λανθασμένη διάγνωση και ένας κακός χειρισμός αντίστοιχα. Από την άλλη εάν το ποσοστό των μη διαγνωστικών επιχρισμάτων είναι υπερβολικά υψηλό (υπερβαίνει τα αποδεκτά όρια 12-15%) η εφαρμογή της μεθόδου δεν μπορεί να θεωρηθεί επιτυχής και θα πρέπει να αναζητηθούν τα αίτια ώστε να γίνουν οι κατάλληλες βελτιώσεις.
4.3. Πληροφορίες που πρέπει να παρέχονται από τους κλινικούς στον κυτταροπαθολόγο
Για την ορθή αξιολόγηση των μικροσκοπικών εικόνων χρήσιμες ή και απαραίτητες είναι κάποιες κλινικές πληροφορίες, που θα έπρεπε να συνοδεύουν τα παραπεμπτικά.
- Φύλο και ηλικία του ασθενούς με ειδική αναφορά στην περίπτωση εγκυμοσύνης, δεδομένου ότι επιχρίσματα εγκύων ενδέχεται να είναι ιδιαίτερα κυτταροβριθή όπως πολλές φορές και επιχρίσματα νεαρών ατόμων, και να οδηγήσουν σε ψευδώς θετικές διαγνώσεις.
- Πληροφορίες από το ατομικό και οικογενειακό ιστορικό που ενδέχεται να έχουν σχέση με την αλλοίωση όπως λ.χ. οικογενές μυελοειδές καρκίνωμα ή ευρήματα υπερπαραθυρεοειδισμού.
- Πληροφορίες για την λειτουργική κατάσταση του θυρεοειδούς, με ενδεχόμενα σπινθηρογραφικά ευρήματα, και για την λήψη αντιθυρεοειδικών σκευασμάτων. Αντιθυρεοειδικά φάρμακα προκαλούν κυταρικές αλλοιώσεις, που ενδέχεται να υπερερμηνευθούν (ευμεγέθεις υπερχρωματικοί πυρήνες), όπως και η λειτουργικού τύπου πυρηνική ατυπία σε υπερλειτουργικούς όζους.
- Η πλέον απαραίτητη ωστόσο πληροφορία αφορά τα υπερηχογραφικά ευρήματα, όπως τον αριθμό, το μέγεθος,την εντόπιση, το σχήμα και την υφή των όζων, με ειδική αναφορά στην περίπτωση μικροαποτιτανώσεων και στον τύπο της αγγείωσης.
5. Διαγνωστικές δυνατότητες της βιοψίας σε θυροειδικούς όζους
Η διαγνωστική ακρίβεια της βιοψίας σε έμπειρα κέντρα, και εάν εξαιρέσει κανείς τα μη διαγνωστικά επιχρίσματα, υπερβαίνει το 95% με την ευαισθησία να κυμαίνεται μεταξύ 65% και 98% (μέση τιμή 77,7%) και την ειδικότητα μεταξύ 72% και 100% (μέση τιμή 85,4%)(4,17-21) Ολες οι στατιστικές εκτιμήσεις βασίζονται σε συγκρίσεις με την ιστολογική εικόνα χειρουργημένων ασθενών, δεδομένου ότι η ιστολογική διάγνωση θεωρείται χρυσό στάνταρ. Βεβαίως έχει αμφισβητηθεί η απόλυτη βεβαιότητα της ιστολογικής διάγνωσης λόγω των μεγάλων αποκλίσεων μεταξύ διαφορετικών παρατηρητών(interobserver variability) που οφείλονται σε εγγενείς δυσχέρειες στην αποκρυστάλλωση μορφολογικών κριτηρίων αλλά και ιστικών δεικτών (22). Ιδιαίτερα η διάγνωση του θηλώδους καρκινώματος, που βασίζεται κύρια σε κυτταρολογικά κριτήρια, είναι μερικές φορές ευκολότερη σε καλά παρασκευασμένο κυτταρολογικό υλικό από ότι σε ιστό που έχει λ.χ. υποστεί post FNA νέκρωση και ινοπλασία. Επιπλέον το ποσοστό των ψευδώς αρνητικών διαγνώσεων σε υλικό βιοψίας είναι πλασματικά υψηλό, αφού στους χειρουργημένους ασθενείς προφανώς περιλαμβάνεται ψηλότερο ποσοστό νεοπλασμάτων από ότι σε μη επιλεγμένους ασθενείς.
5.1. Οι περιορισμοί της μεθόδου
Οι κύριοι περιορισμοί της μεθόδου είναι το ανεπαρκές-μη αντιπροσωπευτικό υλικό και το απροσδιόριστο επίχρισμα
5.1.1. Ανεπαρκές-μη αντιπροσωπευτικό υλικό
Η εκτίμηση της απάρκειας και αντιπροσωπευτικότητας του υλικού μπορεί να είναι δυσχερής και είναι συνάρτηση πολλών παραγόντων, όπως της τεχνικής λήψης και επεξεργασίας του υλικού, αλλά και κλινικών παραμέτρων, η σύγκριση με τις οποίες είναι απαραίτητη. Προτάσεις που αναφέρουν στην βιβλιογραφία ποσοτικές εκτιμήσεις, δεν είναι δυνατόν να ισχύσουν γενικά και είναι προφανές, ότι το υλικό που ενδεχομένως είναι ικανοποιητικό για ένα μικρό, ισόηχο όζο, πιθανόν δεν κρίνεται το ίδιο όταν πρόκειται για ένα μεγάλο, υπερηχογραφικά ύποπτο όζο. Θεωρώ ότι η εκτίμηση της επάρκειας του υλικού απαιτεί συχνά εμπειρία του κυταροπαθολόγου αλλά και ευρύτερη γνώση του σε υπερηχογραφικές και κλινικές παραμέτρους. Ενας αποδεκτός ορισμός της επάρκειας θα ήταν «Διαγνωστικό θα πρέπει να θεωρείται ένα επίχρισμα καλά επιστρωμένο, μονιμοποιημένο και χρωσμένο, που περιέχει επαρκή και ειδικά κυτταρικά στοιχείαγια μία διάγνωση συμβατή με τα κλινικά και υπερηχογραφικά ευρήματα»
5.1.2. Απροσδιόριστο επίχρισμα
Αυτή η ομάδα περιλαμβάνει δύο κατηγορίες επιχρισμάτων: Επιχρίσματα με κυταρικά στοιχεία χωρίς διαγνωστικούς φαινοτυπικούς χαρακτήρες, ή με καλοήθη κύτταρα σε συνύπαρξη με άτυπες κυτταρικές αθροίσεις («εστιακά ύποπτο επίχρισμα»), και όλα τα κυτταροβριθή επιχρίσματα, χωρίς όμως άτυπα κυτταρικά στοιχεία («θυλακιώδης αλλοίωση»), που αποτελούν μία «γκρίζα ζώνη» στην κυταρολογία αλλά συχνά και στην ιστολογία αλλοιώσεων με θυλακιώδες πρότυπο ανάπτυξης. Με βάση προσωπικές, μη δημοσιευμένες στατιστικές στην πρώτη ομάδα κακοήθεια παρατηρείται τελικά σε 65% περίπου των επιχρισμάτων, ενώ στην δεύτερη ομάδα σε περίπου 20%.
5.2. Διαγνωστική αξιοπιστία της μεθόδου ανάλογα με το ιστοπαθολογικό υπόστρωμα
Εκτός από την εμπειρία των εμπλεκομένων γιατρών η διαγνωστική ακρίβεια της μεθόδου εξαρτάται σε σημαντικό βαθμό και από το είδος της εξεταζόμενης αλλοίωσης, δεδομένου ότι κάποιες αλλοιώσεις οδηγούν σε μονοσήμαντα, διαγνωστικά επιχρίσματα, ενώ άλλες συνδέονται συχνά με μη διαγνωστικά ή και παρελκυστικά επιχρίσματα (23-26).
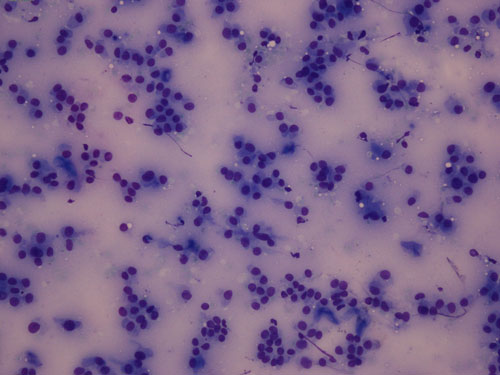
Καλοήθεις όζοι. Τυπικοί υπερπλαστικοί όζοι, κυρίως οι κολλοειδείς, διαγνώσκονται συνήθως με ευχέρεια. (Εικόνα 5). Θέσεις με οξύφιλη μετάπλαση ή θυλακική υπερπλασία,ή με λειτουργική ατυπία, ενδέχεται να υπερδιαγνωσθούν.Η θυρεοειδίτιδα Hashimoto επιβεβαιώνεται εύκολα με με τη βιοψία, ωστόσο τα επιχρίσματα συχνά παρελκύουν τόσο προς ψευδώς θετικές όσο και προς ψευδώς αρνητικές διαγνώσεις (27). Τα θυλακικά κύτταρα συμπεριλαμβανομένων των μεταπλαστικών επιδεικνύουν συχνά σημαντική ατυπία που μπορεί σα υπερδιαγνωσθεί ως νεόπλασμα (28). Αντίθετα οι πυκνές φλεγμονώδεις διηθήσεις είναι δυνατόν να καλύψουν τα νεοπλασματικά κύτταρα, ενώ ο ινώδης τύπος της θυρεοειδίτιδας ενδέχεται να συνδέεται με σημαντική δυσχέρεια στην λήψη του δείγματος. Επιχρίσματα από την υποξεία θυρεοειδίτιδα επιβεβαιώνουν την διάγνωση εφόσον περιλαμβάνονται τα ευμεγέθη πολυπύρηνα γιγαντοκύτταρα, τα οποία ωστόσο ενδέχεται να απουσιάζουν, ιδίως στην φάση υποστροφής.
Εικόνα 5. Κολλοειδής όζος-Άφθονο ίζημα κολλοειδούς.
Από τα νεοπλάσματα η ψηλότερη διαγνωστική ακρίβεια επιτυγχάνεται για το θηλώδες καρκίνωμα, που αποτελεί το συχνότερο νεόπλασμα και επιδεικνύει χαρακτηριστική μορφολογία. (Εικόνα 6). Σε μερικές μάλιστα περιπτώσεις είναι δυνατή και η αναγνώριση κάποιας ποικιλίας (όπως η διάχυτη σκληρυντική, ή η ποικιλία από υψηλά κύτταρα).

Εικόνα 6. Θηλώδες καρκίνωμα-Πολυγωνικά κύτταρα με ευμεγέθεις ακανόνιστους πυρήνες.
Το αναπλαστικό καρκίνωμα διαγνώσκεται επίσης με ευχέρεια λόγω της εξαιρετικής κυτταρικής ατυπίας και πολυμορφίας, ωστόσο η λήψη αντιπροσωπευτικού υλικού ενδέχεται να αποτύχει, λόγω των συχνών εκτεταμένων νεκρώσεων στο νεόπλασμα αυτό (Εικόνα 7).

Εικόνα 7. Αναπλαστικό καρκίνωμα.Διάχυτο πρότυπο με μεγάλη ατυπία και πολυμορφία.
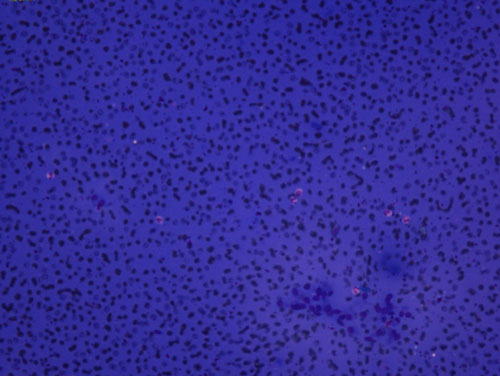
Το μυελοειδές καρκίνωμα μπορεί να έχει πολύ καλή διαγνωστική προσπέλαση, απαιτεί ωστόσο μεγάλη διαγνωστική εμπειρία (Εικόνα 8).
Εικόνα 8. Μυελοειδές καρκίνωμα.Τριγωνικά κύτταρα με έκκεντρο πυρήνα και αζουρόφιλη κοκκίωση στο κυτταρόπλασμα.
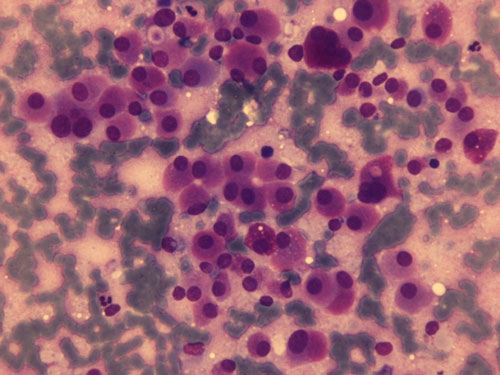
Δεδομένης της μεγάλης σημασίας της προεγχειρητικής αναγνώρισης του νεοπλάσματος, συνιστώ τον έλεγχο καλσιτονίνης σε όλα τα ύποπτα επιχρίσματα που δεν ταξινομούνται επακριβώς. Ιδιαίτερα δυσχερής ενδέχεται να είναι και η διάγνωση του καρκινώματος χαμηλής διαφοροποίησης, ιδιαίτερα του νησιδιακού καρκινώματος, με τα μικρά, ομοιόμορφα, ελάχιστα άτυπα κύτταρα (24,29) (Εικόνα 9).
Εικόνα 9. Χαμηλής διαφοροποίησης νησιδιακό καρκίνωμα (μικρά μονόμορφα κύτταρα).
Tην “γκρίζα διαγνωστική ζώνη» με τα απροσδιόριστα επιχρίσματα αποτελούν οι αλλοιώσεις με κυτταροβριθές, μικροθυλακιώδες πρότυπο ανάπτυξης, με κύτταρα κλασσικά θυλακικά ή οξύφιλα και χωρίς πυρήνες θηλώδους καρκινώματος, που αντιστοιχούν σε «αδενωματώδεις» υπερπλαστικούς όζους, σε αδενώματα ή και θυλακιώδη καρκινώματα (Εικόνα 10).

Εικόνα 10. Θυλακιώδες πρότυπο σε θυλακιώδη νεοπλασία.
Εφόσον η διάγνωση βασίζεται στην παρουσία ή όχι διηθημένης κάψας είναι προφανές ότι με βάση την μορφολογία η γκρίζα ζώνη δεν είναι δυνατόν να εξαλειφθεί, ωστόσο εάν υπάρχει εμπειρία, είναι δυνατόν να γίνει πάρα πoλύ μικρή (30,31,32). Έχω δει λ.χ. να υπερδιαγνώσκονται σαν ύποπτα κυτταροβριθή επιχρίσματα, που απλώς αφορούσαν χονδρή επίστρωση. Επίσης θηλώδη καρκινώματα με οξύφιλο κυταρόπλασμα είναι δυνατόν να υποδιαγνωσθούν σαν γκρίζες οξύφιλες αλλοιώσεις. Εάν ωστόσο τηρηθούν αυστηρά τα διαγνωστικά κριτήρια, τα απροσδιόριστα «γκρίζα» επιχρίσματα εμφανίζουν κακοήθεια σε ποσοστό 30-35% σε χειρουργικό υλικό (2). Σαν γκρίζο επίχρισμα ή ακόμη και σαν καρκίνωμα διαγνώσκονται συνήθως και παραθυρεοειδικές διογκώσεις που παρακεντώνται «κατά λάθος» ως θυρεοειδικές (33). Για τον λόγο αυτό είναι σκόπιμο να ελέγχεται και παραθορμόνη σε όλα τα απροσδιόριστα κυτταροβριθή επιχρίσματα, ιδιαίτερα σε βιοψίες που έχουν διενεργηθεί με υπερηχογραφική καθοδήγηση, που έχει ευκολότερα πρόσβαση σε διογκώσεις της οπισθίας επιφάνειας του θυρεοειδούς.
Κακοήθη λεμφώματα αναγνωρίζονται ευχερώς ως λεμφοκυτταρικές επεξεργασίες, ωστόσο χαμηλής κακοήθειας λεμφώματα είναι δύσκολο να διαφοροδιαγνωσθούν έναντι φλεγμονώδους επεξεργασίας. Επιπλέον, ακόμη και υψηλής κακοήθειας λεμφώματα έχουν ανάγκη ταυτοποίησης, έτσι απαιτείται λήψη επιπλέον υλικού για κυτταρομετρία ροής ή ανοσοιστοχημικό προσδιορισμό του ανοσοφαινοτύπου των λεμφοειδών κυττάρων (12,34-35).
5.2.1. Πόσο αξιόπιστος είναι ο έλεγχος των τραχηλικών λεμφαδένων με βιοψία με λεπτή βελόνη σε παρουσία θυρεοειδικού καρκινώματος;
Ένα θετικό εύρημα είναι διαγνωστικό μετάστασης, ωστόσο ένα αρνητικό δεν αποκλείει την παρουσία μετάστασης ,δεδομένου πως η μετάσταση δεν αφορά απαραίτητα όλη την έκταση του λεμφαδένα. Μεταστατικά διηθημένοι λεμφαδένες υφίστανται συχνά κυστική εκφύλιση, η οποία μπορεί να είναι τόσο εκτεταμένη, ώστε να υπάρχει δυσχέρεια στην ανεύρεση νεοπλασματικών κυττάρων στην βιοψία. Κυστικά εκφυλισμένοι τραχηλικοί λεμφαδένες σε ιστορικό θηλώδους καρκινώματος λ.χ. παραμένουν ύποπτοι για διήθηση ακόμη και με αρνητική, ακυταρική βιοψία. Η μέτρηση της θυρεοσφαιρίνης στο υγρό αυτών των εστιών αποτελεί μία ενδιαφέρουσα εναλλακτική λύση, εφόσον βέβαια είναι δυνατή μία αξιόπιστη μέτρηση.
5.2.2. Πόσο συνεισφέρει η βιοψία με βελόνη στην εκτίμηση μετεγχειρητικών διογκώσεων
Με την βιοψία είναι σχετικά εύκολο να διαγνώσει κανείς ένα μετεγχειρητικό κοκκίωμα έναντι ενός λεμφαδένα ή υπολείμματος θυρεοειδικού ιστού, όπως και να επιβεβαιώσει την παρουσία καρκινικού ιστού (λ.χ. τοπική υποτροπή)
6. Τελικό βήμα: Η αξιολόγηση της πληροφορίας από τον κλινικό-Συστήματα αναφοράς ευρημάτων
Το τελευταίο αλλά όχι ασήμαντο βήμα είναι η επικοινωνία μεταξύ κυτταροπαθολόγου και κλινικού, προκειμένου ο πρώτος να ενημερώσει τον δεύτερο για τα ευρήματά του, ώστε να γίνει ο τελικός σχεδιασμός για το χειρισμό του ασθενούς. Δεδομένων των προσπαθειών για την επεξεργασία θεραπευτικών πρωτοκόλλων, όπου προκειμένου για τις θυρεοειδικές διογκώσεις η βιοψία με βελόνη κατέχει κεντρική θέση, είναι εμφανής η αναγκαιότητα κοινής γλώσσας εργαστηριακού-κλινικού, με βάση κάποιο εύχρηστο σύστημα αναφοράς των ευρημάτων (Reporting systems). Κατά καιρούς έχουν προταθεί διάφορα συστήματα αναφοράς, κυρίως από κυταροπαθολογικές ομάδες εργασίας (36,37), που συχνά λειτουργούν μάλλον συγχυτικά. Σε γενικές γραμμές όλα τα συστήματα, που ομαδοποιούν τα ευρήματα σε 4-6 βαθμίδες (4-6 tiered) κινούνται γύρω από την εξής βασική ομαδοποίηση των επιχρισμάτων:
- Επίχρισμα μη διαγνωστικό (nondiagnostic/inadequate)
- Καλόηθες (benign)
- Απροσδιόριστο (indeterminate)
- Ύποπτο για κακοήθεια (suspicious)
- Κακοήθεια (malignant)
Θα αναφερθώ εκτενέστερα στην τελευταία προσπάθεια που ξεκίνησε με μία διάσκεψη που οργανώθηκε από το αμερικανικό NCI το 2007, στη συνέχεια ωστόσο έλαβαν μέρος σε διεθνές επίπεδο επιστήμονες διαφορετικών ειδικοτήτων εμπλεκόμενοι στη διάγνωση και χειρισμό του θυρεοειδικού όζου (26). Το αποτέλεσμα ήταν ένα εξαβάθμιο σύστημα ταξινόμησης για τα κυτταροπαθολογικά ευρήματα (Τhe Βethesda –FΝΑ Reporting System), το οποίο μεταφέρει κατά την γνώμη μου στον κλινικό πιο εύστοχα την πληροφορία και τους προβληματισμούς (38). Κάθε κατηγορία αναλύεται ακριβώς ως προς το περιεχόμενο και τις υποκατηγορίες, συνδέεται δε με ρίσκο κακοήθειας, καθώς και με κάποια σύσταση για τον προτεινόμενο χειρισμό.
6.1. Συνοπτική παρουσίαση των κατηγοριών του συστήματος Bethesda
Κατηγορία Ι – Μη διαγνωστικό ή μη ικανοποιητικό υλικό. Ακυτταρικό υλικό ή με κακή επεξεργασία, δεν οδηγεί με σχετική ασφάλεια σε διάγνωση. Το ρίσκο για κακοήθεια υπολογίζεται 1-4%. Προτείνεται επανάληψη της βιοψίας.
Κατηγορία ΙΙ – Καλοήθεια. Αναφέρεται σε περιπτώσεις υπερπλαστικών όζων με σαφείς χαρακτήρες, θυρεοειδιτίδων κ.λ.π. Το ρίσκο για κακοήθεια είναι ελάχιστο, 0-3% Συνιστάται παρακολούθηση του όζου.
Κατηγορία ΙΙΙ – Ατυπία αγνώστου σημασίας, θυλακιώδης αλλοίωση ή οξύφιλη αλλοίωση αγνώστου σημασίας ( AUS: Atypia of undetermined significance, FLUS: Follicular lesion of undetermined significance. HCLUS: Huerthle cell lesion of undetermined significance). Περιλαμβάνει επιχρίσματα, όπου εκτός από καλοήθη στοιχεία, παρατηρούνται άτυπες κυταρικές αθροίσεις ή κυτταροβριθείς περιοχές από θυλακικά ή οξύφιλα κύτταρα με κάποιου βαθμού ατυπία. Το ρίσκο υπολογίζεται 5-15%. Στην περίπτωση AUS συνιστάται επανάληψη της βιοψίας, στην περίπτωση FLUS ή HCLUS λοβεκτομή.
Κατηγορία IV – Θυλακιώδης νεοπλασία ή υπόνοια για θυλακιώδη ( ή ογκοκυταρική) νεοπλασία. Αναφέρεται σε μονόμορφα κυτταροβριθή άτυπα επιχρίσματα.Το ρίσκο κακοήθειας έχει υπολογισθεί 15-30%. Συνιστάται λοβεκτομή .
Κατηγορία V – Yπόνοια κακοήθειας. Περιλαμβάνει επιχρίσματα ύποπτα για κάποιο καρκίνωμα (θηλώδες, μυελοειδές, αναπλαστικό, χαμηλής διαφοροποίησης), χωρίς απόλυτα παθογνωμονικούς χαρακτήρες. Το ρίσκο για κακοήθεια υπολογίζεται 65-75%. Συνιστάται σχεδόν ολική θυρεοειδεκτομή.
ΚατηγορίαVI – Κακοήθεια. Αναφέρεται σε καρκινώματα με παθογνωμονικούς χαρακτήρες. Το ρίσκο για κακοήθεια είναι εξαιρετικά υψηλό, 97-99%, και συστήνεται σχεδόν ολική θυρεοειδεκτομή.
6.2. Προσωπικές επισημάνσεις στο σύστημα ταξινόμισης των επιχρισμάτων
Όταν υπάρχει προσωπική επικοινωνία με τον κλινικό γιατρό συχνά τίθεται λιγότερο ή περισσότερο ευθέως το ερώτημα στον κυταροπαθολόγο «Πόσο σίγουρη είναι η διάγνωση;» Το ιδανικό θα ήταν κατά την γνώμη μου να συνοδεύεται κάθε διάγνωση από μία πρόχειρη εκτίμηση του βαθμού βεβαιότητας της διάγνωσης, ακόμη καλύτερα από ένα πρόχειρο υπολογισμό του ποσοστού πιθανώς ψευδώς αρνητικού ή ψευδώς θετικού αποτελέσματος. Η προσθήκη ενός ποσοστού μιας ενδεχόμενης ψευδούς διάγνωσης με βάση τις διεθνείς στατιστικές θα ήταν και μία αναφορά στην εγγενή αδυναμία της μεθόδου να προσφέρει απαραίτητα την τελική διάγνωση, και θα αποθάρρυνε τους ασθενείς από παράλογες ενίοτε απαιτήσεις, ενώ θα ενεθάρρυνε τους κυτταροπαθολόγους σε λιγότερο ευθυνόφοβες και περισσότερο στοχευμένες διαγνώσεις. Μία τέτοια προσθήκη έχει κατά καιρούς προταθεί σε διεθνείς ομάδες εργασίας, χωρίς ωστόσο να έχει μέχρι στιγμής καθιερωθεί. Για το λόγο αυτό θεωρώ πως θα βοηθούσε προς αυτή την κατεύθυνση εάν τουλάχιστον γινόταν μία υποταξινόμιση των ομάδων Ι και ΙΙ (39)
Η ομάδα Ι «μη διαγνωστικό υλικό» θα μπορούσε να χωρισθεί σε 3 υποομάδες α, β και γ.
Σαν Ια να χαρακτηρίζονται όλες οι περιπτώσεις που στερούνται οποιουδήποτε ειδικού στοιχείου (περιέχουν αίμα και συνδετικό υπόστρωμα), δεν παρέχουν δηλαδή καμμία πληροφορία.
Σαν Ιβ οι περιπτώσεις που πιθανολογούμε καλοήθεια, δεν επαρκεί ωστόσο το υλικό να την στοιχειοθετήσουμε (κολλοειδείς κύστεις χωρίς κύτταρα, υγρό από κυστική εκφύλιση με φαγοκύτταρα χωρίς παρουσία επιθηλιακών κυττάρων)
Σαν Ιγ οι περιπτώσεις που το υλικό είναι ελάχιστο και όχι διαγνωστικό, με στοιχεία ωστόσο που εγείρουν υπόνοια κακοήθειας (λιγοστά άτυπα κύτταρα, κύτταρα με διαφαινόμενη ατυπία που ωστόσο δεν εκτιμάται επαρκώς λόγω κακής επίστρωσης, μονιμοποίησης ή χρώσης, κάποια στοιχεία του υποστρώματος συχνά σε νεοπλασίες όπως λ.χ. πολυπύρηνα γιγαντοκύτταρα ή πιθανά ψαμμώδη σωμάτια). Στην κατηγορία αυτή ένας έμπειρος κυτταροπαθολόγος θα μπορούσε να εντάξει και περπτώσεις, όπου αμφισβητεί την αντιπροσωπευτικότητα, λ.χ. υλικά χωρίς αντιστοιχία με τα υπερηχογραφικά ευρήματα .
Είναι προφανές ότι ο διαχωρισμός αυτός θα είχε ενδιαφέρον για τους κλινικούς, δεδομένου πως στην ομάδα Ιβ η ανάγκη για επανάληψη της βιοψίας δεν είναι τόσο άμεση και πιεστική όπως στην ομάδα Ιγ, πράγμα ουσιώδες κάποιες φορές σε αδυναμία ή απροθυμία του ασθενούς για άμεση επανάληψη, ή σε πολύ μικρούς και υπερηχογραφικά αθώους όζους.
Η ομάδα ΙΙ σημαίνει σαφώς καλοήθεια, ωστόσο δεν είναι όλες οι διαγνώσεις της κατηγορίας αυτής το ίδιο σίγουρες. Εδώ είναι ιδιαίτερα σημαντικό το πρόβλημα της επάρκειας και της αντιπροσωπευτικότητας του υλικού, όπου δεν υπάρχουν γενικά αποδεκτά αποκρυσταλλωμένα κριτήρια, και κυρίως δεν υπάρχουν κριτήρια που να λαμβάνουν υπόψη το μέγεθος και την υπερηχογραφική εικόνα του όζου. Έτσι σκόπιμο θα ήταν η ομάδα ΙΙ να χωρισθεί ως εξής:
ΙΙα, με αβέβαιη επάρκεια/αντιπροσωπευτικότητα, όπου ο κλινικός θα πρέπει να συσχετίσει την διάγνωση με τα ευρήματα και να παρακολουθήσει στενά.
ΙΙβ ομάδα με χαμηλό ρίσκο για ψευδώς αρνητικό. Αφορά τις κλασσικά καλοήθεις εικόνες, ο κλινικός μπορεί να θεωρεί την καλοήθεια δεδομένη στους χειρισμούς του.
ΙΙγ ομάδα με ψηλό ρίσκο για ψευδώς αρνητικό. Περιλαμβάνει τις εικόνες με έντονη κυταροβρίθεια, εστιακή ατυπία και οξύφιλη μετάπλαση, τις οποίες ναι μεν ταξινομούμε ως καλοήθεις, ωστόσο δεν αισθανόμαστε τόσο ασφαλείς όσο στις περιπτώσεις της ομάδας ΙΙβ. Εάν οι κυτταροπαθολόγοι είχαν την δυνατότητα να χρησιμοποιούν μια τέτοια κατάταξη, όπου να εκφράζουν τις αμφιβολίες τους, θα είχαμε πολύ μικρότερα ποσοστά αμυντικών διαγνώσεων του τύπου «Θέσεις ατυπίας, δεν μπορεί να αποκλεισθεί νεοπλασία, συνιστάται επανάληψη» κ.ο.κ.
6.3. Διαβάζοντας την έκθεση της βιοψίας με λεπτή βελόνη του θυρεοειδούς: Επεξηγήσεις για ενδοκρινολόγους
Μία κυτταροπαθολογική ή ιστοπαθολογική έκθεση καταλήγει σε ένα τελικό συμπέρασμα, ωστόσο είναι σκόπιμο ο κλινικός γιατρός να την διαβάζει προσεκτικά ολόκληρη, διότι ενδέχεται να περιέχει πληροφορίες, που να μπορέσει να αξιοποιήσει σχηματίζοντας και την δική του άποψη για την ασφάλεια ή αντίθετα για τις ασάφειες της διάγνωσης. Ένας γνώστης των κυτταροπαθολογικών εικόνων και αντίστοιχα περιγραφών σχηματίζει εύκολα σαφή εικόνα της αξιοπιστίας του εργαλείου που λέγεται βιοψία. Η αξιοπιστία λοιπόν αυτή κυμαίνεται με βάση τα εξής:
6.3.1. Καλοήθεις διαγνώσεις
Κολλοειδείς όζοι. Οζοι με μεγαλοθυλακιώδες πρότυπο ανάπτυξης χαρακτηρίζονται από άφθονο κολλοειδές, φαγοκύτταρα και τυπικά θυλακικά κύτταρα. Με ασφάλεια καλοήθεια (σπάνια εξαίρεση η μακροθυλακιώδης πουκιλία του θηλώδους καρκινώματος)
«Αδενωματώδεις» όζοι. Πρόκειται για κυτταροβριθείς, μικροθυλακιώδεις ή με συμπαγές πρότυπο όζους.Η διαφορική διάγνωση από νεοπλασίες δεν μπορεί να γίνει με απόλυτη ασφάλεια, ιδιαίτερα εάν οι όζοι είναι μεγάλοι (επειδή διηθητική συμπεριφορά σε θυλακιώδεις νεοπλασίες είναι εξαιρετικά σπάνια σε μικρές αλλοιώσεις). Απαραίτητη είναι η συνεκτίμηση με τα άλλα ευρήματα, κυρίως την υπερηχογραφική εικόνα, και η στενή παρακολούθηση.
Επιχρίσματα με οξύφιλη μετάπλαση. Οξύφιλη μετάπλαση είναι ιδιαίτερα συχνή σε νόσο Hashimoto αλλά παρατηρείται και σε οζώδη υπερπλασία. Ανησυχητικό είναι όταν οι οξύφιλες αθροίσεις είναι άφθονες, και ακόμη περισσότερο, όταν τα κύτταρα είναι αποκλειστικά οξύφιλα, όταν χαρακτηρίζονται από χαμηλή κυτταρική συνοχή, και όταν έχουν ευμεγέθη πυρήνια. Μη έμπειροι κυτταροπαθολόγοι είναι δυνατόν να υποεκτιμήσουν κύτταρα του θηλώδους καρκινώματος σαν οξύφιλη μετάπλαση. Επιχρίσματα από άτυπους οξύφιλους όζους, ιδιαίτερα σε έδαφος θυρεοειδίτιδας μπορεί να επιδεικνύουν εξαιρετική δυσκολία στην αξιολόγηση.
Επιχρίσματα με πυκνή λεμφοκυτταρική διήθηση. Επιχρίσματα με άφθονα λεμφοκύτταρα συχνά οδηγούν τόσο σε ψευδώς αρνητικές όσο και σε ψευδώς θετικές διαγνώσεις. Τα νεοπλασματικά κύτταρα μπορεί να καλυφθούν από τα λεμφοκυτταρικά στοιχεία, αντίθετα ατυπία λόγω φλεγμονής είναι δυνατόν να υπερεκτιμηθεί ως νεοπλασματική. Συνιστούμε τη σύγκριση με το υπερηχογράφημα στις περιπτώσεις ατύπων κυττάρων σε συνύπαρξη με θυρεοειδίτιδα, ιδίως σε απουσία διαγνωστικά υψηλών αντισωμάτων, λόγω του ενδεχόμενου περινεοπλασματικής θυρεοειδίτιδας (40).
6.3.2. Κακοήθεις διαγνώσεις
Όσο ακριβέστερη είναι η τυποποίηση της νεοπλασίας, τόσο απομακρύνεται το ενδεχόμενο ψευδώς θετικής διάγνωσης. Διαγνώσεις του τύπου «στοιχεία ατυπίας, εγείρεται υπόνοια νεοπλασίας κ.ο.κ.» ενδέχεται να αντιστοιχούν σε λειτουργική ατυπία.
Η διαγνωστική ακρίβεια και ειδικότητα διαφέρουν μεταξύ των διαφόρων νεοπλασμάτων. Η πλέον αξιόπιστη διάγνωση γίνεται σε επάρκεια του υλικού στο θηλώδες καρκίνωμα, ειδικά στον κοινό τύπο και στις επιθετικές πουκιλίες από υψηλά κύτταρα, διάχυτο σκληρυντικό, κυλινδροκυτταρικό. Αντίθετα η θυλακιώδης ποικιλία ενδέχεται να εμφανίζεται σαν κυτταροβριθής άτυπος όζος της γκρίζας ζώνης, ενώ η μεγαλοθυλακιώδης ποικιλία ακόμη και σαν κολλοειδής όζος. Η διάγνωση στις περιπτώσεις αυτές ανιχνεύεται με λεπτομερή μικροσκόπιση της κυταρικής μορφολογίας. Το ενδεχόμενο εκτεταμένης κυστικής εκφύλισης με συνέπεια την δυσχέρεια στην αναγνώριση του νεοπλάσματος, ιδιαίτερα σε λεμφαδενικές μεταστάσεις, αναφέρθηκε ήδη.
Θυλακιώδεις και ογκοκυτταρικές νεοπλασίες αποτελούν μία γκρίζα ζώνη, όπως εκτενώς αναφέραμε, με μεγάλες αποκλίσεις και μεταξύ των κυτταροπαθολογικών αξιολογήσεων. Ο ενδοκρινολόγος θα πρέπει να εκτιμήσει προς ποιά πλευρά κλίνει το πόρισμα της βιοψίας, ποιά είναι η υπερηχογραφική εικόνα, το μέγεθος και η αυξητικότητα του όζου.
Το μυελοειδές καρκίνωμα γενικά διαγνώσκεται με καλή ακρίβεια, ειδικά όταν χρησιμοποιείται ξηρό επίχρισμα και χρώση τύπου Romanowski (MGG). Ωστόσο λόγω της σχετικής σπανιότητας μπορεί κάποιος που δεν το συναντά συχνά να μην είναι ευαισθητοποιημένος. Εξάλλου το μυελοειδές πέραν των κλασσικών εικόνων εμφανίζεται και με διάφορους, λιγότερο κλασσικούς φαινοτύπους, που ενδέχεται να διαλάθουν της διάγνωσης. Κάποιοι τύποι μπορεί να διαγνωσθούν ως πιθανό λέμφωμα ή χαμηλής διαφοροποίησης θυλακιοκυτταρικό καρκίνωμα. Το σημαντικό βέβαια για το μυελοειδές καρκίνωμα είναι να τεθεί η υπόνοια, αφού η μέτρηση της καλσιτονίνης μπορεί να επιβεβαιώσει την διάγνωση.
Θα πρέπει να τονίσουμε ότι το χαμηλής διαφοροποίησης θυλακιοκυτταρικό καρκίνωμα, ιδιαίτερα το νησιδοειδές καρκίνωμα (insular Ca) αν και συμπεριφέρεται επιθετικότερα από το διαφοροποιημένο, συχνά έχει αθώο φαινότυπο με μικρά κύτταρα χωρίς ουσιώδη πολυμορφία και είναι δυνατόν να μην διαγνωσθεί ή να χαρακτηρισθεί σαν άτυπος κυτταροβριθής όζος.
Το αναπλαστικό καρκίνωμα διαγνώσκεται γενικά με ευχέρεια λόγω της μεγάλης ατυπίας και πολυμορφίας. Βέβαια το καρκίνωμα αυτό ενδέχεται να εμφανίζει ακυτταρικά επιχρίσματα, λόγω εκτεταμένης νέκρωσης. Για αυτό σε περιπτώσεις με την κλινική εικόνα του αναπλαστικού καρκινώματος θα πρέπει η δειγματοληψία να επιμείνει μέχρι την λήψη ικανοποιητικού, μη νεκρωτικού υλικού.
Διαφοροποιημένα καρκινώματα μπορεί να περιέχουν συνιστώσα καρκινώματος χαμηλής διαφοροποίησης ή και αναπλαστικού. Μια τέτοια συνιστώσα είναι πολλές φορές δυνατόν να διαγνωσθεί με την βιοψία ή έστω να εκφρασθεί υπόνοια, δεν είναι όμως δυνατό να αποκλεισθεί σε καμμία περίπτωση καρκινώματος. Γενικότερα εφόσον είναι γνωστή η μεγάλη φαινοτυπική ποικιλία και η ιστική ετερογένεια στα θυρεοειδικά καρκινώματα, είναι προφανές ότι ο στόχος της βιοψίας με λεπτή βελόνη είναι η επιλογή των ασθενών για χειρουργική αντιμετώπιση και όχι η τελική ταξινόμιση του όγκου, η οποία είναι ενίοτε δυσχερής ακόμη και στο ιστολογικό παρασκεύασμα.
Βιβλιογραφία
1. Gharib H, Papini E, Paschke R, Duick DS, Valcavi R, Hegedüs L, Vitti P; AACE/AME/ETA Task Force on Thyroid Nodules :American Association of Clinical Endocrinologists, Associazione Medici Endocrinologi, and European Thyroid Association medical guidelines for clinical practice for the diagnosis and management of thyroid nodules: executive summary of recommendations.J Endocrinol Invest.2010; 33(5 Suppl):51-6.
2. Buesseniers AE,Silver SA : Fine needle aspiration cytology of the thyroid.In: Oertli D, Udelsman R(eds) Surgery of the thyroid and parathyroid glands.Springer Verlag, Berlin, Heidelberg ,2007, pp 61-80
3. Hall TL,Layfield LG, Philippe A, Rosenthal DL : Sources of diagnostic error in fine needle aspiration of the thyroid. Cancer 1989; 63:718-725
4. Droese M .Aspiration cytology of the thyroid. Schattauer Stuttgart, New York1995; pp 3-25
5. Boerner SL,Asa SL : Biopsy interpretation of thyroid.Lippincott,Williams and Wilkins ,Philadelphia 2010: pp13-37
6. Tseleni S. :Fine needle aspiration of thyroid: confusion v. subsequent histology. J Clin Pathol 1986; :39(6):697-8
7. Keebler CM.Cytopreparatory techniques.In :Bibo M (ed) Comprehensive Cytopathology.Saunders Philadelphia1991
8. Crystal BS, Wang HH,Ducatman BS: Comparison of different preparation techniques for fine needle aspiration specimens.A semiquantitative and statistical analysis.Acta Cytol 1993;37:24-28
9. Kocjan G :.FNAC technique and slide preparation.In:Fine needle aspiration cytology.Springer, Berlin Heidelberg, 2006; pp. 7-33
10. Zito FA, Gadaleta CD, Salvatore C,et al. :A modified cell block technique for fine needle aspiration cytology.Acta Cytol 1995;39 :93-99
11. Boon M :Routine cytologic staining procedures.In:Weid GL,Bibbo M,Keebler CM, et al41. (eds) Tutorials of Cytology,International Academy of Cytology, Chicago 1992
12. Henrique RM,Sousa ME,GodinhoMI, et al.: .Immunophenotyping by flow cytometry of fine needle aspirates in the diagnosis of lymphoproliferative disorders :A retrospective study.J Clin Lab Anal 1999;13 :224-228
13. Delibasis KK, Asvestas PA, Matsopoulos GK, Zoulias E, Tseleni-Balafouta S. :Computer-aided diagnosis of thyroid malignancy using an artificial immune system classification algorithm.IEEE Trans Inf Technol Biomed 2009;13(5):680-6.
14. Tseleni-Balafouta S, Katsouyanni K, Kitsopanides J, Koutras DA. : The outcome of benign thyroid nodules correlates with the findings of fine needle biopsy.Thyroidology 1991; 3(2):75-8.
15. Hamburger JI, Hussein M :Semiquantitative criteria for fine needle aspiration diagnosis:reduced false negative diagnosis Diagn Cytopathol 1988;4:14-17
16. Chow LS, Gharib H, Goellner JR et al. : Nondiagnostic thyroid fine needle aspiration cytology :management dilemmas. Thyroid 2001;11:1147-1151
17. Hamburger JI, Hamburger SW : Fine needle biopsy of thyroid nodules:avoiding the pitfalls. NY State J Med 1986; 86:241-249
18. Gharib H, Goellner JR :. Fine –needle aspiration biopsy of the thyroid: An appraisal. Ann Intern Med 1993;118:282-289
19. Jayaram G, Razak A,Chan SK ,et al. : Fine needle aspiration of the thyroid:a review of experience in 1854 cases. Malays J Pathol 1999;21:17-27
20. Revetto C, Colombo L, Dottorini ME:Usefulness of fine needle aspiration in the diagnosis of thyroid carcinoma:a retrospective study in 37,895 patients. Cancer 2000;90:357-363
21. Ko HM, JhuIK,Yang SH , et al. :Clinicopathologic analysis of fine needle aspiration cytology of the thyroid.Acta Cytol 2003;47:727-732
22. Saxen E, Franssila K,Bjarnason O, Norman T, Ringertz N.: Observer variation in histologic classification of thyroid cancer.Acta Path Microbiol Scand Section A 1978; 86: 483-486
23. Lowhagen T, Sprenger E : Cytologic presentation of thyroid tumors in aspiration biopsy smear:a review of 60 cases. Acta Cytol 1974;18:192-197
24. Nguyen GK, Akin MR :Cytopathology of insular carcinoma of the thyroid.Diagn Cytopathol 2001;25:325-330
25. Orell SR,Philips J.:The thyroid.fine needle biopsy and cytological diagnosis of thyroid lesions. Karger ,Basel London New York1997;,pp 8-29
26. Baloch ZW, Livolsi VA, Asa SL, et al :.Diagnostic terminology and morphologic criteria for cytologic diagnosis of thyroid lesions:a synopsis of the National Cancer Institute thyroid fine needle aspiration state of the science conference.Diagn Cytopathol 2008;36:425-437
27. Guarda LA, Baskin HJ :.Inflammatory and lymphoid lesions of the thyroid gland:cytomorphology by fine needle aspiration.Am J Clin Pathol 1987;87:14-22
28. Ravinsky E, Safneck JR:Differentiation of Hashimoto’s thyroiditis from thyroid neoplasms in fine needle aspirates. Acta Cytol 1988;32:854-861
29. Pietribiasi F, Sapino A, Papotti M, et al. : Cytologic features of poorly differentiated « insular » carcinoma of the thyroid, as revealed by fine needle aspiration biopsy. Am J Clin Pathol 1990;94:687-692
30. Kini SR,Miller JM, Hamburger JI, et al. : Cytopathology of follicular lesions of the thyroid gland. Diagn Cytopathol 1985; 1:123-132
31. Raber W, Kasserer K, Niederle B, et al. : Risk factors of malignancy of thyroid nodules initially identified as follicular neoplasia by fine needle aspiration:results of a prospective study of one hundred twenty patients. Thyroid 2000;10:109-112
32. Baloch ZW,Fleisher S, livolsi VA, et al.: Diagnosis of « follicular neoplasm » :a gray zone in thyroid fine-needle aspiration cytology.Diagn Cytopathol 2002;26 :41-44
33. Tseleni-Balafouta S, Gakiopoulou H, Kavantzas N, Agrogiannis G, Givalos N, Patsouris E.: Parathyroid proliferations: a source of diagnostic pitfalls in FNA of thyroid.Cancer. 2007; 25:111(2):130-6.
34. Matsuzuka F, Miyauchi A,Katayama S,Narabayashi I,Ikeda H,Kuma K,Sugawara M.: Clinical aspects of primary thyroid lymphoma:Diagnosis and treatment based on our experience of 119 cases. Thyroid 1993; 3:93-99
35. Dong HY,Harris NL,Preffer FI, Pitman MB :.Fine needle aspiration biopsy in the diagnosis and classification of primary and recurrent lymphoma:a retrospective analysis of the utility of cytomorphology and flow cytometry. Mod Pathol 2001; 14:472-481
36. Wang HH. : Reporting thyroid fine needle aspiration:literature review and proposal. Diagn Cytopathol 2006;34:67-76
37. Baloch ZW,Livolsi VA :Fine needle aspiration of thyroid nodules:past, present and future.Endocr Pract 2004; 10:234-241
38. Cibas ES &Syed A: The Bethesda system for reporting of thyroid cytopathology. AJCP 2009;132:658-665
39. Tseleni-Balafouta S: Fine needle aspiration of thyroid. In:Linos&Chung(eds):Minimaly invasive thyroidectomy. Springer Verlag Berlin Heidelberg 2012.pp 37-58
40. Tseleni-Balafouta S, Kyroudi-Voulgari A, Paizi-Biza P, Papacharalampous NX.: Lymphocytic thyroiditis in fine-needle aspirates: differential diagnostic aspects.Diagn Cytopathol. 1989; 5(4):362-5.
Created: October 25, 2014
Last update: October 25, 2014