Λαμπρινή Παπαναστασίου 1, Ιωάννης – Αναστάσιος Βατάλας 2
1 Ενδοκρινολόγος, Διδάκτωρ Ιατρικής Σχολής Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών,
Επιμελήτρια Β’ Ενδοκρινολογικού Τμήματος και Κέντρου Διαβήτη, ΓΝΑ «Γ. Γεννηματάς»
2 Ενδοκρινολόγος, Διδάκτωρ Ιατρικής Σχολής Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών,
Επιστημονικός Συνεργάτης Μονάδας Ενδοκρινολογίας, Μεταβολισμού και Διαβήτη,
Ιατρικής Σχολής Εθνικού και Καποδιστριακού Πανεπιστημίου Αθηνών
1. Εισαγωγή
Η διαβητική κετοξέωση (ΔΚ) και η υπεργλυκαιμική υπερώσμωση (ΥΥ) αποτελούν δύο σοβαρές οξείες μεταβολικές διαταραχές του σακχαρώδη διαβήτη (ΣΔ) οι οποίες χαρακτηρίζονται από απόλυτη ή σχετική ένδεια ινσουλίνης και σοβαρή υπεργλυκαιμία (1). Διαβητική κετοξέωση εκδηλώνεται όταν, λόγω της σοβαρής ένδειας ινσουλίνης, τα πολύ χαμηλά ή ανεπαρκή επίπεδα της ινσουλίνης οδηγούν όχι μόνο σε υπεργλυκαιμία και αφυδάτωση αλλά και σε παραγωγή κετονικών σωμάτων και οξέωση. Υπεργλυκαιμική υπερώσμωση παρατηρείται όταν η ένδεια ινσουλίνης είναι μερική με αποτέλεσμα να προκαλείται σοβαρή υπεργλυκαιμία, η οποία οδηγεί σε αφυδάτωση και σοβαρή υπερώσμωση χωρίς όμως συνήθως τη δημιουργία οξέωσης. Η διαταραχή αυτή ονομαζόταν στο παρελθόν υπεργλυκαιμικό υπερωσμωτικό μη κετωτικό κώμα, όμως επικράτησε ο όρος ΥΥ επειδή συχνά υπάρχει διαταραχή του επιπέδου συνείδησης και όχι πάντοτε κώμα, ενώ κάποιες φορές παρατηρείται και μικρού βαθμού κέτωση.
2. Ορισμοί
Η ΔΚ και η ΥΥ θεωρούνται δύο ακραίες κλινικές οντότητες απορρύθμισης ΣΔ που εξακολουθούν, παρά την κατανόηση των φυσιοπαθολογικών μηχανισμών και την εφαρμοζόμενη εντατική αντιμετώπισή τους, να αποτελούν ακόμη και στις μέρες μας σημαντικές αιτίες νοσηρότητας και θνητότητας στους ασθενείς με ΣΔ. Περιγράφονται σαν δύο διακριτές οντότητες, ωστόσο στο 30% των ασθενών συνυπάρχουν χαρακτηριστικά και των δύο διαταραχών (μικτή διαταραχή) (2). Η ΔΚ και η ΥΥ είναι τα δύο άκρα του φάσματος των οξέων υπεργλυκαιμικών επιπλοκών και οι ασθενείς μπορεί να βρεθούν οπουδήποτε «κατά μήκος της συνέχειας» της διαβητικής μεταβολικής διαταραχής (3, 4, 5). Στον πίνακα 1 φαίνονται τα διαγνωστικά κριτήρια των διαταραχών (ΔΚ και ΥΥ) όπως αυτά έχουν προταθεί από την Αμερικανική Διαβητολογική Εταιρεία (ADA) το 2009 (6). Επίσης, φαίνονται και τα χαρακτηριστικά της μικτής διαταραχής. Η ΔΚ χαρακτηρίζεται από την παρουσία υπεργλυκαιμίας (γλυκόζη > 250 mg/dl), κέτωσης και μεταβολικής οξέωσης (pΗ < 7,3) ενώ, η ΥΥ χαρακτηρίζεται από την παρουσία σοβαρής υπεργλυκαιμίας (γλυκόζη > 600 mg/dl), υπερώσμωσης (> 320 mosm/Kg) και ελάχιστης ή καθόλου κέτωσης. Η ΔΚ ταξινομείται ανάλογα με το βαθμό της οξέωσης (το αρτηριακό pΗ), τα επίπεδα των διττανθρακικών του ορού και το επίπεδο συνείδησης σε ήπια, μέτρια, σοβαρή.
Πίνακας 1. Διαγνωστικά κριτήρια ΔΚ και ΥΥ.
|
Διαβητική κετοξέωση |
Υπεργλυκαιμική υπερώσμωση |
Μικτή διαταραχή |
|||
|
ήπια |
Μέτρια |
Σοβαρή |
|||
| Γλυκόζη (mg/dl) |
>250 |
> 250 |
> 250 |
> 600 |
> 600 |
| pH |
7,25 – 7,30 |
7,00 – 7,24 |
< 7,00 |
> 7,30 |
ποικίλλει |
| HCO3 (mEq/L) |
15 – 18 |
10 – 14 |
< 10 |
> 18 |
≤ 15 |
| Κετονουρία/ Κετοναιμία |
παρούσα |
παρούσα |
παρούσα |
μικρή |
παρούσα |
| Χάσμα ανιόντων |
> 10 |
> 12 |
> 12 |
ποικίλλει |
ποικίλλει |
| Δραστική ωσμωτικότητα (mosm/kg) |
ποικίλλει |
ποικίλλει |
ποικίλλει |
>320 |
> 320 |
| Επίπεδο συνείδησης |
εγρήγορση |
εγρήγορση/υπνηλία |
λήθαργος/κώμα |
ποικίλλει |
ποικίλλει |
Αναπροσαρμογή από Kitabchi Α et al 2009 (6).
Η ΔΚ συμβαίνει συνήθως σε ασθενείς με ΣΔ τύπου 1, ενώ η ΥΥ σε ασθενείς με ΣΔ τύπου 2 (7). Οι ασθενείς με ΣΔ τύπου 2 μπορούν να αναπτύξουν ΔΚ σε καταστάσεις που υπάρχει αφενός μεγάλη αύξηση των απαιτήσεων σε ινσουλίνη και αύξηση αφετέρου της αντίστασης των ιστών στην ινσουλίνη. Η αντίσταση στην ινσουλίνη μπορεί να αυξηθεί σε περιπτώσεις σοβαρού stress όπως πχ λοίμωξη, τραύμα, καρδιαγγειακά συμβάματα και να συμβάλλει, σε συνθήκες μερικής έλλειψης ινσουλίνης, στη δημιουργία κέτωσης. Στις καταστάσεις αυτές οι ασθενείς με ΣΔ τύπου 2 έχουν ανεπαρκή, για τις ιδιαίτερες αυτές μεταβολικές συνθήκες και απαιτήσεις, επίπεδα ινσουλίνης.
Η ΔΚ εμφανίζεται επίσης σπανιότερα σε ασθενείς με ΣΔ επιρρεπή στην κέτωση (ketosis – prone diabetes mellitus). Η διαταραχή αυτή είναι συχνή στους Αφρο – Αμερικάνους και στους ισπανόφωνους Αμερικάνους όπου πάνω από το 50% των ασθενών αυτών παρουσιάζουν ΔΚ ως πρώτη εκδήλωση του διαβήτη (8, 9). Οι ασθενείς με ΣΔ επιρρεπή στην κέτωση εμφανίζουν κλινικά και μεταβολικά χαρακτηριστικά ΣΔ τύπου 2 όπως παχυσαρκία, οικογενειακό ιστορικό ΣΔ, απουσία δεικτών αυτοάνοσης καταστροφής των β – κυττάρων του παγκρέατος και ενδογενή υπολειπόμενη έκκριση ινσουλίνης. Η μορφή αυτή του ΣΔ χαρακτηρίζεται από αιφνίδια αλλά παροδική έκπτωση των β – κυττάρων του παγκρέατος και δεν έχει διευκρινιστεί αν υπεύθυνη για την εμφάνιση αυτής της κλινικής οντότητας είναι η γλυκοτοξικότητα, η λιποτοξικότητα ή υπάρχει γενετική προδιάθεση. Μετά τη θεραπεία με ινσουλίνη και τη διόρθωση της υπεργλυκαιμίας υπάρχει συχνά ύφεση του ΣΔ και ο γλυκαιμικός έλεγχος επιτυγχάνεται για αρκετά χρόνια με δίαιτα και λήψη αντιδιαβητικών δισκίων.
3. Επιδημιολογία
Ο επιπολασμός της ΔΚ είναι 4 – 8 περιπτώσεις ανά 1000 εισαγωγές ασθενών με ΣΔ ανά έτος. Η ΔΚ είναι πιο συχνή σε ασθενείς ηλικίας μικρότερης των 30 ετών όπου ο επιπολασμός κυμαίνεται σε 13 περιπτώσεις ανά 1000 εισαγωγές ασθενών ανά έτος (10, 11). Η ετήσια επίπτωση της ΔΚ ποικίλει ανάλογα με το γεωγραφικό τόπο, πχ στη Δανία υπολογίζεται σε 12,9 περιπτώσεις ανά 100.000 κατοίκους (12). Η επίπτωση της ΔΚ φαίνεται να παρουσιάζει αύξηση. Σύμφωνα με το Κέντρο Ελέγχου Νοσημάτων των ΗΠΑ (Centers for Disease Control and Prevention) οι εισαγωγές στο νοσοκομείο των ασθενών με ΔΚ παρουσίασαν αύξηση από 80.000 το 1988 σε 140.000 περίπου το 2009, ενώ, ταυτόχρονα η μέση χρονική διάρκεια νοσηλείας μειώθηκε κατά 2,3 ημέρες μεταξύ των ετών 1988 – 2009 (13). Η ΔΚ είναι πιο συχνή στις γυναίκες συγκριτικά με τους άνδρες καθώς και σε ασθενείς ηλικίας μικρότερης των 65 ετών (14). Αν και η επίπτωση της ΔΚ παρουσιάζει αύξηση, η θνησιμότητά της στις ανεπτυγμένες χώρες έχει μειωθεί σημαντικά στις μέρες μας αφενός λόγω της έγκαιρης διάγνωσης και αφετέρου της καλύτερης αντιμετώπισής της. Συγκεκριμένα, παρατηρήθηκε τα τελευταία 20 έτη μείωση πάνω από 15%, η μεγαλύτερη δε μείωση σημειώθηκε στους ασθενείς ηλικίας άνω των 65 ετών (15 – 17). Στους ενήλικες, σε εξειδικευμένα κέντρα, η θνητότητα από ΔΚ είναι μικρότερη από 1% (< 5% στους ηλικιωμένους) και οφείλεται κυρίως σε υποκείμενη νόσο και σπάνια στις μεταβολικές επιπλοκές της υπεργλυκαιμίας ή της κετοξέωσης (14, 15). Στα παιδιά με ΣΔ τύπου 1, η ΔΚ είναι η πιο συχνή αιτία θανάτου λόγω του εγκεφαλικού οιδήματος που μπορεί να εμφανιστεί (18).
Η ΥΥ είναι πιο συχνή σε ασθενείς με ΣΔ τύπου 2, ηλικίας μεγαλύτερης από 65 έτη. Ωστόσο, έως 20% των ασθενών με ΥΥ είναι ηλικίας μικρότερης από 30 έτη (2, 14). Η ανάπτυξη ΣΔ τύπου 2 στη νεαρή ηλικία που μπορεί να οδηγήσει σε ΥΥ, εξαρτάται από κοινωνικοοικονομικούς παράγοντες, την ανάπτυξη παχυσαρκίας και την εθνικότητα (19). Η επίπτωση της ΥΥ είναι δύσκολο να καθοριστεί επακριβώς λόγω της έλλειψης μεγάλων πληθυσμιακών μελετών, υπολογίζεται δε ότι κυμαίνεται στο 1% των εισαγωγών στο νοσοκομείο των ασθενών με ΣΔ (14). Η θνητότητα της ΥΥ είναι μεγαλύτερη σε σχέση με εκείνη της ΔΚ, εξακολουθεί ακόμη και σήμερα να είναι υψηλή, κυμαινόμενη μεταξύ 5 – 20% σε διάφορα κέντρα στις ανεπτυγμένες χώρες και οφείλεται όπως και στη ΔΚ, σε υποκείμενη νόσο και σε παρουσία συνυπαρχουσών παθήσεων (17). Η πρόγνωση δε τόσο της ΔΚ όσο και της ΥΥ είναι χειρότερη στις ακραίες ηλικίες καθώς και όταν συνυπάρχει κώμα ή υπόταση (20, 21).
4. Εκλυτικοί παράγοντες
Οι πιο συχνοί εκλυτικοί παράγοντες της ΔΚ και της ΥΥ είναι οι λοιμώξεις κυρίως του αναπνευστικού και του ουροποιητικού στο 40 – 50% των περιπτώσεων καθώς και η ανεπαρκής θεραπεία με ινσουλίνη (6, 14). Η ανεπαρκής θεραπεία με ινσουλίνη αφορά τη μη συμμόρφωση στην αγωγή, τη διακοπή της θεραπείας και την παράληψη ή την ανεπαρκή δόση της ινσουλίνης (22). Επεισόδια ΔΚ παρατηρούνται συχνά σε ασθενείς με ΣΔ τύπου 1 (30% των ασθενών) οι οποίοι παρουσιάζουν ψυχολογικά και κοινωνικά προβλήματα καθώς και διαταραχές της όρεξης και της λήψης τροφής με αποτέλεσμα τη μη συμμόρφωση και την παράληψη των δόσεων της ινσουλίνης που απαιτούνται για την επίτευξη της σωστής γλυκαιμικής ρύθμισης (23). Στις καταστάσεις που μπορεί να οδηγήσουν στην εμφάνιση ΔΚ συμπεριλαμβάνονται επίσης τα σφάλματα από τη χρήση της φορητής αντλίας συνεχούς έγχυσης ινσουλίνης, η εφαρμογή της οποίας έχει αυξηθεί τα τελευταία χρόνια. Η σωστή χρήση και η καλή λειτουργία της αντλίας συνεχούς έγχυση ινσουλίνης είναι σημαντικές, διαφορετικά μπορεί να υπάρξει διακοπή στο ρυθμό έγχυσης της ινσουλίνης με αποτέλεσμα συχνά την εμφάνιση ΔΚ. Η τεχνική εξέλιξη των αντλιών ινσουλίνης, η καλύτερη εκπαίδευση και παρακολούθηση των ασθενών με αντλία ινσουλίνης έχουν μειώσει σημαντικά τη συχνότητα εμφάνισης ΔΚ συγκριτικά με το παρελθόν (24, 25). Άλλοι παράγοντες που μπορούν να οδηγήσουν στην εμφάνιση ΔΚ ή ΥΥ είναι η παγκρεατίτιδα, το έμφραγμα του μυοκαρδίου, το αγγειακό εγκεφαλικό επεισόδιο ή οποιοιδήποτε άλλη κατάσταση με οξύ stress. Συχνά, σε ποσοστό περίπου 20% των περιπτώσεων, ο ΣΔ τύπου 1 πρωτοεμφανίζεται με ΔΚ. Στους εκλυτικούς παράγοντες της ΔΚ ή της ΥΥ συμπεριλαμβάνονται επίσης και φάρμακα που παρεμβαίνουν στο μεταβολισμό των υδατανθράκων όπως πχ τα γλυκοκορτικοειδή, τα θειαζιδικά διουρητικά, οι συμπαθητικομιμητικές αμίνες καθώς και τα αντιψυχωσικά φάρμακα 2ης γενιάς (ολανζαπίνη). Επιπλέον, η χρήση κοκαΐνης, η οποία συχνά συνδέεται με παράληψη δόσεων της ινσουλίνης και σε συνδυασμό με την αύξηση των αντιρροπιστικών ορμονών που επάγει, μπορεί να οδηγήσει σε επεισόδια ΔΚ (26). Στους ενοχοποιητικούς παράγοντες εμφάνισης ΔΚ ή ΥΥ συμπεριλαμβάνονται επίσης ενδοκρινοπάθειες όπως η μεγαλακρία, το σύνδρομο Cushing, η θυρεοτοξίκωση και το φαιοχρωμοκύττωμα (27 – 30). Τέλος, στα ηλικιωμένα άτομα ο περιορισμός της πρόσληψης ύδατος, συνήθως λόγω υποκείμενου νοσήματος και η ακινητοποίηση σε συνδυασμό με τη συνυπάρχουσα διαταραχή του αισθήματος της δίψας συμβάλλουν σε σοβαρή αφυδάτωση και σε ανάπτυξη ΥΥ (2, 20). Οι κυριότεροι εκλυτικοί παράγοντες των ΔΚ και ΥΥ φαίνονται στον Πίνακα 2.
Πίνακας 2. Εκλυτικοί παράγοντες ΔΚ και ΥΥ.
| Διαβητική κετοξέωση | Υπεργλυκαιμική υπερώσμωση |
| Ανεπαρκής θεραπεία με ινσουλίνη | Ανεπαρκής θεραπεία με ινσουλίνη |
| Οξεία νόσος/σοβαρό stress | Οξεία νόσος/σοβαρό stress |
| Λοιμώξεις (30 – 40%) | Λοιμώξεις (32 – 60%) |
| Αγγειακό εγκεφαλικό επεισόδιο | Αγγειακό εγκεφαλικό επεισόδιο |
| Οξύ έμφραγμα μυοκαρδίου | Οξύ έμφραγμα μυοκαρδίου |
| Οξεία παγκρεατίτιδα | Οξεία παγκρεατίτιδα |
| Πνευμονική εμβολή | |
| Πρωτοεμφανιζόμενος ΣΔ (15 – 20%) | Απόφραξη εντέρου |
| Αιμοκάθαρση, περιτοναϊκή κάθαρση | |
| Φάρμακα | Θρόμβωση μεσεντερίου |
| Κλοζαπίνη – ολανζαπίνη | Χρόνια νεφρική ανεπάρκεια |
| Κοκαΐνη | Θερμοπληξία, υποθερμία |
| Λίθιο | Υποσκληρίδιο αιμάτωμα |
| Τερμπουταλίνη | Σοβαρά εγκαύματα |
| Κορτικοστεροειδή | Χειρουργικές επεμβάσεις |
| Ενδοκρινοπάθειες | |
| Θυρεοτοξίκωση | |
| Μεγαλακρία | |
| Σύνδρομο Cushing | |
| Φάρμακα | |
| Ανταγωνιστές διαύλων ασβεστίου | |
| Χλωροπρομαζίνη | |
| Χλωροθαλιδόνη | |
| Σιμετιδίνη | |
| Διαζοξίδη | |
| Κλοζαπίνη – ολανζαπίνη | |
| Αιθακρυνικό οξυ | |
| Ανοσοκατασταλτικοί παράγοντες | |
| L – ασπαραγινάση | |
| Λοξαπίνη | |
| Φαινυτοίνη | |
| Προπρανολόλη | |
| Κορτικοστεροειδή | |
| Θειαζιδικά διουρητικά | |
| Ολική παρεντερική διατροφή | |
| Αδιάγνωστος ΣΔ |
Αναπροσαρμογή από Kitabchi Α et al. 2001 (14).
5. Παθογένεια
Οι κύριοι παθογενετικοί μηχανισμοί που οδηγούν στην εμφάνιση της ΔΚ και της ΥΥ είναι: α) η ένδεια, πλήρης ή μερική, της ινσουλίνης με ή χωρίς παρουσία αντίστασης στην ινσουλίνη και β) η αντιρροπιστική αύξηση των ορμονών του stress (γλυκαγόνης, κατεχολαμινών, κορτιζόλης και αυξητικής ορμόνης) που οδηγούν σε διαταραχή του μεταβολισμού των υδατανθράκων, των λιπιδίων και των πρωτεϊνών (1, 2).
Η ένδεια της ινσουλίνης, είναι απαραίτητη για την εμφάνιση τόσο της ΔΚ όσο και της ΥΥ (Εικόνα 1). Αν η ένδεια της ινσουλίνης είναι αρκετά σοβαρή, παρατηρείται αυξημένη λιπόλυση και κετογένεση με αποτέλεσμα την εμφάνιση ΔΚ. Αν η ένδεια της ινσουλίνης είναι μερική, επαρκής μεν για την επίτευξη καταστολής της λιπόλυσης και της κετογένεσης όχι όμως και για την καταστολή της υπεργλυκαιμίας, έχουμε την ανάπτυξη ΥΥ (31). Η συγκέντρωση της ινσουλίνης που απαιτείται για την καταστολή της λιπόλυσης φαίνεται να είναι το 1/10 εκείνης που απαιτείται για την προαγωγή της χρησιμοποίησης της γλυκόζης και την καταστολή της υπεργλυκαιμίας (32).
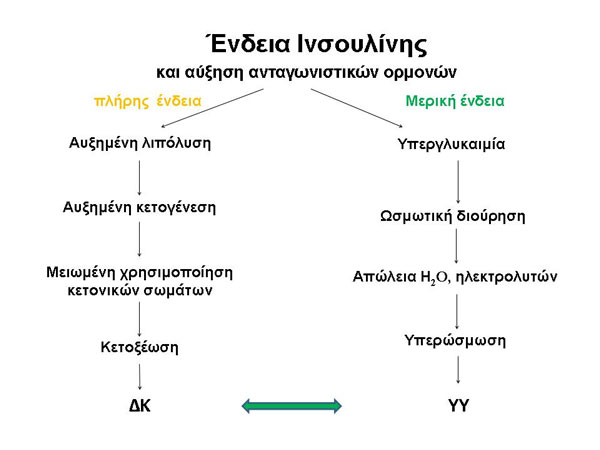
Εικόνα 1. Οξείες επιπλοκές ΣΔ: ΔΚ και ΥΥ.
Η γλυκαγόνη, από τις ορμόνες του stress, διαδραματίζει κυρίαρχο ρόλο στην παθογένεια της ΔΚ ενώ ο ρόλος της αυξητικής ορμόνης είναι μικρότερος. Η ινσουλίνη έχει κατασταλτική επίδραση στην έκκριση της γλυκαγόνης, η οποία είναι αυξημένη στη ΔΚ λόγω της ένδειας της ινσουλίνης και η πιθανότητα να συμβεί ΔΚ απουσία γλυκαγόνης είναι μικρή (33). Ωστόσο, ασθενείς οι οποίοι έχουν υποστεί ολική παγκρεατεκτομή και επομένως δεν έχουν ενδογενή έκκριση ινσουλίνης και γλυκαγόνης, όταν διακοπεί η θεραπεία με εξωγενή ινσουλίνη, αναπτύσσουν ηπιότερη ΔΚ σε σχέση με εκείνους τους ασθενείς με ΣΔ τύπου 1 που διατηρούν ένα βαθμό ενδογενούς παραγωγής και έκκρισης γλυκαγόνης (34).
Τα κύρια χαρακτηριστικά της ΔΚ και της ΥΥ είναι η υπεργλυκαιμία, η κετογένεση και η αφυδάτωση.
5.1. Υπεργλυκαιμία
Φυσιολογικά, ο μεταβολισμός της γλυκόζης στα κύτταρα ποικίλλει ανάλογα με τις εκάστοτε μεταβολικές ανάγκες του οργανισμού. Η γλυκόζη μπορεί είτε να αποθηκευτεί στον οργανισμό με τη μορφή γλυκογόνου, είτε να διασπαστεί μέσω γλυκόλυσης σε πυροσταφυλικό οξύ. Το πυροσταφυλικό οξύ στη συνέχεια μπορεί να μετατραπεί σε γαλακτικό, σε αλανίνη ή σε ακέτυλο – συνένζυμο Α (ακέτυλο – συνΑ). Το ακέτυλο – συνΑ μπορεί να οξειδωθεί σε CO2 και Η2Ο ή να μετατραπεί σε λιπαρά οξέα, τα οποία να χρησιμοποιηθούν στην παραγωγή κετονικών σωμάτων ή στη σύνθεση τριγλυκεριδίων.
Η υπεργλυκαιμία στη ΔΚ και την ΥΥ είναι αποτέλεσμα δύο μηχανισμών: α) της μείωσης της χρησιμοποίησης της γλυκόζης στους ινσουλινοευαίσθητους ιστούς (λιπώδης ιστός, ήπαρ, μύες), που έχει ως αποτέλεσμα τον περιορισμό της γλυκόλυσης, της λιπογένεσης και της σύνθεσης γλυκογόνου και β) της αύξησης της παραγωγής της γλυκόζης κυρίως μέσω αύξησης της γλυκονεογένεσης, πρωτίστως στο ήπαρ και δευτερευόντως στους νεφρούς καθώς και της γλυκογονόλυσης (7, 35).
Η έλλειψη της ινσουλίνης και η αυξημένη γλυκαγόνη αναστέλλουν τη φωσφο – φρουκτοκινάση με αποτέλεσμα την ελάττωση της περιφερικής χρησιμοποίησης της γλυκόζης από τους ιστούς (μείωση γλυκόλυσης).
Η αυξημένη ηπατική παραγωγή γλυκόζης οφείλεται στην αυξημένη προσφορά γλυκονεογενετικών υποστρωμάτων όπως: α) αμινοξέων, αλανίνης και γλουταμίνης, αποτέλεσμα της αυξημένης πρωτεόλυσης και της μειωμένης πρωτεϊνοσύνθεσης, β) γαλακτικού οξέος, αποτέλεσμα της αυξημένης διάσπασης του μυϊκού γλυκογόνου (γλυκογονόλυση) και γ) γλυκερόλης, αποτέλεσμα της αυξημένης λιπόλυσης (36, 37). Ο αυξημένος λόγος γλυκαγόνης/ινσουλίνης καθώς και η υπερκορτιζολαιμία επάγουν νεογλυκογενετικά ένζυμα όπως την 1,6 φρουκτοζοδιφωσφατάση, την καρβοξυκινάση του φωσφο – ενολο – πυροσταφυλικού οξέος (ΡΕPCΚ), τη γλυκόζο – 6 – φωσφατάση, και τη καρβοξυλάση του πυροσταφυλικού με αποτέλεσμα την αυξημένη ηπατική παραγωγή γλυκόζης (38, 39).
Στη συνολική υπεργλυκαιμία που παρατηρείται στη ΔΚ και την ΥΥ, εκτός από τη μειωμένη διαθεσιμότητα της ινσουλίνης συμβάλλει επίσης και η αντίσταση των ιστών στην ινσουλίνη με την ελαττωμένη περιφερική χρησιμοποίηση της γλυκόζης που προκαλεί.
5.2. Κετογένεση
Η κετογένεση, η παραγωγή δηλαδή κετονικών σωμάτων, και η οξέωση αποτελούν χαρακτηριστικά γνωρίσματα της ΔΚ (7, 35). Η ινσουλίνη προάγει τη μετατροπή των ελεύθερων λιπαρών οξέων (ΕΛΟ) σε τριγλυκερίδια και αναστέλλει τη λιπόλυση. Η γλυκαγόνη είναι η πιο σημαντική καταβολική ορμόνη, αυξάνεται νωρίς στην έναρξη της απορρύθμισης, διατηρεί σταθερά επίπεδα γλυκόζης διεγείροντας την ηπατική γλυκονεογένεση και γλυκογονόλυση, έχει απευθείας λιπολυτική δράση και συμβάλλει στην αύξηση των επιπέδων των κετονικών σωμάτων (40). Τα αυξημένα επίπεδα αυξητικής ορμόνης μπορούν επίσης να αυξήσουν τα ΕΛΟ και τα κετονικά σώματα.
Η ανεπάρκεια της ινσουλίνης σε συνδυασμό με την αύξηση των αντιρροπιστικών ορμονών του stress, ιδιαίτερα δε της αδρεναλίνης, οδηγεί στην ενεργοποίηση στο λιπώδη ιστό της ορμονοευαίσθητης ενδοκυττάριας λιποπρωτεϊνικής λιπάσης. Το ένζυμο αυτό προάγει τη λιπόλυση, τη διάσπαση δηλαδή των τριγλυκεριδίων και την απελευθέρωση στην κυκλοφορία μεγάλων ποσοτήτων γλυκερόλης και ΕΛΟ (41).
Η κετογένεση, εξαρτάται από την ποσότητα των ΕΛΟ που φθάνουν στο ήπαρ από την κυκλοφορία. Τα ΕΛΟ μετατρέπονται στο κυτταρόπλασμα των ηπατοκυττάρων σε παράγωγα του ακυλ – συνΑ και μεταφέρονται στη συνέχεια στην έσω μεμβράνη των μιτοχονδρίων μέσω ενεργοποίησης του ειδικού ενζυματικού συστήματος της ακυλ – συνΑ τρανσφεράσης της καρνιτίνης (CPT1). Η αυξημένη, λόγω έλλειψης της ινσουλίνης, γλυκαγόνη ελαττώνει τα επίπεδα του μαλονυλ – συνA (αναστολέας της CPT1) και επάγει τη δραστηριότητα της CPT1 με αποτέλεσμα τη μεταφορά των παραγώγων του ακυλ – συνΑ στo εσωτερικό των μιτοχονδρίων και τη β – οξείδωσή τους (42). Οι β – οξειδώσεις των ΕΛΟ έχουν σαν τελικό προϊόν το ακετυλο – συνΑ το οποίο συσσωρεύεται και στη συνέχεια, ένα μέρος του εισέρχεται στον κύκλο του Krebs για περαιτέρω οξείδωση ενώ το υπόλοιπο μετατρέπεται, μέσω οξείδωσης, σε ακετοξεικό οξύ που είναι το πρώτο παραγόμενο κετονικό σώμα. Το ακετοξεικό οξύ ανάγεται σε β – υδροξυβουτυρικό οξύ με μία αμφίδρομη αντίδραση που εξαρτάται από την οξειδοαναγωγική κατάσταση του ήπατος. Η ακετόνη σχηματίζεται από την αποκαρβοξυλίωση του ακετοξεικού οξέος, αποτελεί μία πτητική ουσία που αποβάλλεται με την αναπνοή και προσδίδει τη χαρακτηριστική απόπνοια σάπιου μήλου που παρατηρείται στη ΔΚ και δεν έχει οξειδωτικές ιδιότητες (Εικόνα 2). Σε περιόδους νηστείας ή όταν η τροφή είναι φτωχή σε υδατάνθρακες τα κετονικά σώματα αποτελούν την εναλλακτική πηγή ενέργειας στους περισσότερους ιστούς και ιδίως στο ΚΝΣ. Σε φυσιολογικές συνθήκες τα κετονικά σώματα αυξάνουν την έκκριση της ινσουλίνης η οποία με τη σειρά της αναστέλλει την κετογένεση. Σε καταστάσεις έλλειψης ινσουλίνης η παραγωγή κετονικών σωμάτων δεν μπορεί να περιοριστεί και ο μεταβολισμός τους είναι μειωμένος. Τα δύο κετονικά σώματα, το ακετοξεικό οξύ και το β – υδροξυβουτυρικό οξύ, είναι ισχυρά οξέα τα οποία, όταν ο ρυθμός παραγωγής τους αυξηθεί σημαντικά, αθροίζονται στο αίμα, με αποτέλεσμα την ανάπτυξη μεταβολικής οξέωσης. Σε φυσιολογικές συνθήκες ο λόγος β – υδροξυβουτυρικού οξέος προς ακετοξεικό είναι 1:1. Στη ΔΚ, τα επίπεδα όλων των κετονικών σωμάτων αυξάνονται, ο λόγος όμως β – υδροξυβουτυρικού οξέος προς ακετοξεικό είναι ιδιαίτερα αυξημένος και μπορεί να φτάσει έως το 10:1 (43).

Εικόνα 2. Κετογένεση.
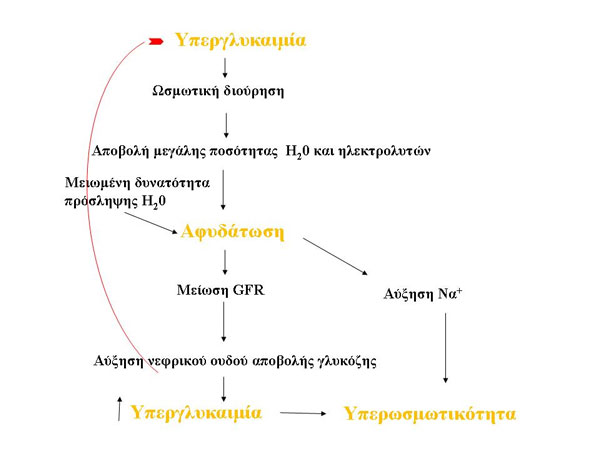 Εικόνα 3. Διαταραχές ύδατος, ηλεκτρολυτών.
Εικόνα 3. Διαταραχές ύδατος, ηλεκτρολυτών.
5.3. Διαταραχή ύδατος και ηλεκτρολυτών
Η υπεργλυκαιμία που υπάρχει στη ΔΚ και στην ΥΥ προκαλεί γλυκοζουρία, η οποία οδηγεί σε αυξημένη ωσμωτική διούρηση με αποτέλεσμα την απώλεια ύδατος και ηλεκτρολυτών. Αρχικά, η γλυκοζουρία περιορίζει την αύξηση της γλυκόζης του αίματος, στη συνέχεια όμως η ωσμωτική διούρηση οδηγεί σε αφυδάτωση, υποογκαιμία, ηλεκτρολυτικές διαταραχές και μείωση του ρυθμού σπειραματικής διήθησης (GFR), σε έκπτωση δηλαδή της νεφρικής λειτουργίας, με αποτέλεσμα την ελάττωση της απέκκρισης της γλυκόζης και την επιδείνωση της υπάρχουσας υπεργλυκαιμίας (35) (Εικόνα 3). Στην αυξημένη ωσμωτική διούρηση συμβάλει επίσης η απέκκριση ανιόντων κετοξέων η οποία προκαλεί ταυτόχρονη απέκκριση κατιόντων όπως αλάτων Na+ και Κ+. Η απώλεια ύδατος και ηλεκτρολυτών είναι σοβαρότερη στην ΥΥ σε σχέση με εκείνη της ΔΚ, λόγω της σταδιακής εγκατάστασης της διαταραχής και της ελαττωμένης, κυρίως σε ηλικιωμένους ασθενείς, πρόσληψης υγρών. Η σοβαρότερη αφυδάτωση της ΥΥ σε συνδυασμό με τη μεγαλύτερη ηλικία και τις συνυπάρχουσες παθήσεις συμβάλλουν στη μεγαλύτερη θνητότητα των ασθενών με ΥΥ συγκριτικά με τους ασθενείς με ΔΚ. Στον Πίνακα 3 αναγράφονται οι απώλειες του ύδατος και των ηλεκτρολυτών που παρατηρούνται στη ΔΚ και στην ΥΥ (44).
Πίνακας 3. Έλλειμμα ύδατος και ηλεκτρολυτών στη ΔΚ και ΥΥ.
|
Διαβητική κετοξέωση |
Υπεργλυκαιμική υπερώσμωση |
|
| H20 (ml/Kg) |
100 (7 L) |
100 – 200 (10,5 L) |
| Na (mmol/Kg) |
7 – 10 (490 – 700) |
5 – 13 (350 – 910) |
| K (mmol/Kg) |
3 – 5 (210 – 300) |
5 – 12 (350 – 1050) |
| Cl (mmol/Kg) |
3 – 5 (210 – 350) |
3 – 7 (210 – 490) |
| P (mmol/Kg) |
1 – 1,5 (70 – 105) |
1 – 2 (70 – 140) |
| Mg (mmol/Kg) |
1 – 2 (70 – 140) |
1 – 2 (70 – 140) |
| Ca (mmol/Kg) |
1 – 2 (70 – 140) |
1 – 2 (70 – 140) |
Το ολικό έλλειμμα ύδατος και ηλεκτρολυτών για έναν ασθενή 70 Kg φαίνεται σε παρένθεση (πηγή: Chiasson JL et al 2003 (44)).
6. Κλινική εικόνα
Η ΔΚ αναπτύσσεται γρήγορα, συνήθως εντός 24 ωρών, σε αντίθεση με την ΥΥ η οποία συνήθως αναπτύσσεται σταδιακά, ίσως και μέσα σε αρκετές μέρες πριν από την εισαγωγή του ασθενούς στο νοσοκομείο. Η κλινική εικόνα ποικίλει ανάλογα με τη σοβαρότητα του κάθε περιστατικού. Η συνήθης κλινική εικόνα και των δύο διαταραχών περιλαμβάνει συμπτώματα πολυουρίας, πολυδιψίας, απώλειας βάρους, κακουχίας, ναυτίας, εμέτων, αφυδάτωσης και διαταραχής του επιπέδου συνείδησης. Μπορεί επίσης να υπάρχουν συμπτώματα υποκείμενης νόσου (πχ λοίμωξης αναπνευστικού, έμφραγμα του μυοκαρδίου) ή ολιγουρίας σε περιπτώσεις οξείας νεφρικής ανεπάρκειας.
Οι διαφορές που παρατηρούνται στην κλινική εικόνα των δύο διαταραχών σχετίζονται με την παρουσία ή μη της κετοξέωσης και των συνεπειών της.
Κοιλιακό άλγος μπορεί να εμφανιστεί στους ασθενείς με ΔΚ, είναι δε πολύ σπάνιο στους ασθενείς με ΥΥ, παρατηρείται όμως πιο συχνά στα παιδιά και μπορεί να είναι τόσο έντονο ώστε να μιμείται εικόνα οξείας κοιλίας. Πιθανόν οφείλεται σε συσπάσεις του μυϊκού χιτώνα του εντέρου λόγω της αφυδάτωσης, της παράτασης του χρόνου γαστρικής κένωσης και της συνύπαρξης ειλεού από τις ηλεκτρολυτικές διαταραχές. Η παρουσία κοιλιακού άλγους σχετίζεται με τη σοβαρότητα της μεταβολικής οξέωσης, δεν σχετίζεται με το βαθμό της υπεργλυκαιμίας ή της αφυδάτωσης, ενώ υφίεται με την άρση της μεταβολικής διαταραχής (45).
Νευρολογικές εκδηλώσεις όπως σύγχυση, λήθαργος, εστιακά συμπτώματα (ημιπάρεση, αφασία, ημιανοψία) και επιληπτοειδείς σπασμοί και οι οποίες μπορεί να εξελιχθούν σε κώμα, είναι πιο συχνές στους ασθενείς με ΥΥ και οφείλονται στην υπερώσμωση και στη σοβαρή αφυδάτωση (4, 46, 47). Η σοβαρότητα των διαταραχών του επιπέδου συνείδησης είναι ανάλογη τόσο του βαθμού και του ρυθμού ανάπτυξης όσο και της εξέλιξης της αφυδάτωσης και της υπερώσμωσης. Έχει διαπιστωθεί θετική γραμμική συσχέτιση μεταξύ της ωσμωτικότητας του πλάσματος και του επιπέδου συνείδησης. Χαρακτηριστικά, ασθενείς με δραστική ωσμωτικότητα πλάσματος πάνω από 320 – 330 mosmol/Kg παρουσιάζουν σοβαρή νευρολογική επιδείνωση (υπνηλία, λήθαργο ή κώμα) (48), ενώ ασθενείς με νευρολογική επιδείνωση και δραστική ωσμωτικότητα πλάσματος χαμηλότερη από 320 mosmol/kg θα πρέπει να διερευνηθούν για άλλες αιτίες, εκτός της υπεργλυκαιμίας, που προκαλούν διαταραχή του επιπέδου συνείδησης. Στη ΔΚ παρατηρείται μικρότερη αύξηση της ωσμωτικότητας του πλάσματος συγκριτικά με την ΥΥ και οι ασθενείς μπορούν να παρουσιάσουν νευρολογικές διαταραχές όπως σύγχυση ή/και κώμα οι οποίες συσχετίζονται με το βαθμό της οξέωσης (49).
Κατά την κλινική εξέταση και στις δύο διαταραχές διαπιστώνονται σημεία αφυδάτωσης όπως ξηροί βλεννογόνοι, ελαττωμένη σπαργή δέρματος, ελαττωμένος τόνος βολβών, ασθενής και συχνός καρδιακός σφυγμός. Αν η αφυδάτωση είναι σοβαρή μπορεί να εμφανιστεί ταχυκαρδία ή/και υπόταση. Χαρακτηριστικό κλινικό σημείο της ΔΚ είναι η οξεωτική αναπνοή τύπου Kussmaul δηλαδή βαθιές αναπνοές με ταχεία εκπνευστική φάση καθώς και η απόπνοια οξόνης (απόπνοια σάπιου μήλου). Η οξέωση προκαλεί αγγειοδιαστολή που οδηγεί σε υπόταση και υποθερμία. Ο πυρετός είναι σπάνιος, λόγω της περιφερικής αγγειοσύσπασης που προκαλείται από την υπογκαιμία, ακόμη και σε παρουσία λοίμωξης. Επίσης συχνά, λόγω της αγγειοδιαστολής που προκαλείται από το αυξημένο CΟ2, μπορεί να παρατηρείται ερυθρότητα προσώπου.
7. Διάγνωση – Εργαστηριακός έλεγχος
Ο αρχικός εργαστηριακός έλεγχος στον οποίο πρέπει να υποβάλλονται οι ασθενείς με ΔΚ ή ΥΥ περιλαμβάνει τον προσδιορισμό της γλυκόζης, των ηλεκτρολυτών, της ουρίας, της κρεατινίνης, της γενικής αίματος, των αερίων αίματος, των κετονών αίματος και ούρων, τον υπολογισμό του χάσματος ανιόντων και της ωσμωτικότητας πλάσματος. Ανάλογα δε με την κλινική εικόνα διενεργείται ακτινογραφία θώρακος ή άλλη κατάλληλη απεικόνιση, ΗΚΓ ή καλλιέργειες βιολογικών υγρών. Συμπληρωματικά, η μέτρηση της HbA1c μπορεί να δώσει πληροφορίες για το επίπεδο της προηγούμενης γλυκαιμικής ρύθμισης.
Η διάγνωση της ΔΚ και της ΥΥ επιβεβαιώνεται από τα εργαστηριακά ευρήματα. Η τριάδα της υπεργλυκαιμίας, της οξέωσης (pH < 7,3) με αυξημένο χάσμα ανιόντων και της κετοναιμίας θέτουν τη διάγνωση της ΔΚ. Τα ιδιαίτερα αυξημένα επίπεδα γλυκόζης (> 600 mg/dl), η απουσία οξέωσης (pH > 7,3) και κετοναιμίας, τα επίπεδα HCO3 > 20 mEq/L και η αυξημένη δραστική ωσμωτικότητα πλάσματος (> 320 mοsm/Kg) συνηγορούν υπέρ της διάγνωσης της ΥΥ (Πίνακας 1).
Τα σημαντικότερα εργαστηριακά ευρήματα της ΔΚ και της ΥΥ αναλύονται στη συνέχεια.
7.1. Γλυκόζη ορού
Τα επίπεδα γλυκόζης ποικίλουν και μπορεί να είναι μετρίως αυξημένα στη ΔΚ (> 250 mg/dl) και ιδιαίτερα αυξημένα στην ΥΥ (> 600 mg/dl). Ο βαθμός της υπεργλυκαιμίας αντανακλά το βαθμό της αφυδάτωσης και της υπερώσμωσης. Οι ασθενείς δε με νεφρική ανεπάρκεια εμφανίζουν, λόγω συνήθως της μειωμένης νεφρικής κάθαρσης της γλυκόζης, σοβαρή υπεργλυκαιμία και συχνά, λόγω απουσίας ωσμωτικής διούρησης, δεν αναπτύσσουν υπερώσμωση, ενώ παρουσιάζουν ηπιότερες διαταραχές του επιπέδου συνείδησης σε σχέση με τους ασθενείς που έχουν καλή νεφρική λειτουργία (50, 51).
Έχουν επίσης περιγραφεί περιπτώσεις ΔΚ με σχεδόν φυσιολογικά επίπεδα γλυκόζης (ευγλυκαιμική ΔΚ) στις οποίες όμως απαιτείται η θεραπευτική χορήγηση ινσουλίνης για την κάθαρση των κετονικών σωμάτων. Αυτό παρατηρείται πιο συχνά σε ασθενείς με μη ικανοποιητική σίτιση ή στην κύηση (52).
7.2. Κετονικά σώματα
Η συγκέντρωση των κετονικών σωμάτων αυξάνεται σε καταστάσεις νηστείας, εγκυμοσύνης ή άσκησης, όμως η μεγαλύτερη αύξηση συμβαίνει στη ΔΚ. Ο προσδιορισμός των κετονικών σωμάτων γίνεται με ταινίες ανίχνευσης κετονικών σωμάτων στα ούρα ή στο αίμα. Η ανίχνευση τους στα ούρα γίνεται με τη βοήθεια της αντίδρασης του νιτροπρωσσικού η οποία αναγνωρίζει την παρουσία ακετοξεικού οξέος και ακετόνης όχι όμως την παρουσία β – υδροξυβουτυρικού οξέος, το οποίο αποτελεί και το επικρατούν οξύ της ΔΚ (35). Επομένως, μία ασθενώς θετική αντίδραση νιτροπρωσσικού δεν αποκλείει τη διάγνωση της ΔΚ. Επίσης, κατά τη διάρκεια της θεραπείας της ΔΚ το β – υδροξυβουτυρικό μετατρέπεται σε ακετοξεικό οξύ, με αποτέλεσμα χρησιμοποιώντας τις ταινίες ανίχνευσης στα ούρα, να δίνεται η ψευδής εντύπωση της επιδείνωσης της κετοξέωσης. Για το λόγο αυτό οι ταινίες ανίχνευσης κετονικών σωμάτων στα ούρα δεν είναι κατάλληλες για την παρακολούθηση της πορείας της ΔΚ. Ψευδώς θετικά αποτελέσματα μπορεί να παρατηρηθούν όταν ασθενείς λαμβάνουν φάρμακα που περιέχουν ελεύθερη ομάδα σουλφυδρυλίου όπως πχ καπτοπρίλη και πενικιλλαμίνη (53). Έτσι, έχουν αναπτυχτεί μέθοδοι άμεσης ποσοτικής ενζυματικής αντίδρασης ανίχνευσης β – υδροξυβουτυρικού στο τριχοειδικό αίμα οι οποίες είναι ευρέως διαθέσιμες όχι μόνο στα τμήματα επειγόντων περιστατικών των νοσοκομείων αλλά και σε κάθε διαβητικό ασθενή με την εφαρμογή της κατάλληλης ταινίας στο μετρητή σακχάρου τριχοειδικού αίματος που χρησιμοποιεί κατά τον αυτοέλεγχο. (54, 55). Η ευαισθησία και η ειδικότητα των ταινιών ανίχνευσης κετονικών σωμάτων στο αίμα είναι σαφώς μεγαλύτερες σε σχέση με εκείνες των ταινιών ανίχνευσης κετονικών σωμάτων στα ούρα.
7.3. pH
Η οξέωση είναι ένα από τα κύρια χαρακτηριστικά της ΔΚ. Σε ασθενείς με φυσιολογικό κορεσμό οξυγόνου στον αέρα, η εκτίμηση της οξέωσης (προσδιορισμός pH) μπορεί να γίνει όχι μόνο με τη λήψη αρτηριακού pH αλλά και με φλεβικό αίμα, αφού το φλεβικό pH είναι συνήθως κατά 0,03 χαμηλότερο του αρτηριακού (56). Τα αέρια αίματος, σε ασθενείς με καρδιακή ή αναπνευστική νόσο, μας δίνουν πληροφορίες για τυχόν παρουσία υποξαιμίας, ενώ τo χαμηλό CO2 αντιπροσωπεύει συνήθως υπεραερισμό, ο οποίος είναι αντιρροπιστικός μηχανισμός της μεταβολικής οξέωσης.
7.4. Διττανθρακικά
Τα επίπεδα των διττανθρακικών του ορού είναι μειωμένα σε ποικίλο βαθμό στην ΔΚ (HCO3 < 18 mEqL ή συχνά < 15 mEq/L) και παρατηρείται αύξηση του χάσματος ανιόντων, ενώ είναι φυσιολογικά στην ΥΥ.
7.5. Χάσμα ανιόντων
Το χάσμα ανιόντων (ΧΑ) είναι χρήσιμο στην εκτίμηση της σοβαρότητας της οξέωσης. Η ομαλοποίησή του αποτελεί δείκτη της λύσης της οξέωσης. Με τον υπολογισμό του ΧΑ εκτιμάται η ποσότητα των μη μετρούμενων ανιόντων στο πλάσμα δηλαδή της λευκωματίνης και των κετοξέων. Το ΧΑ υπολογίζεται αφαιρώντας τα μετρούμενα ανιόντα από τα κατιόντα: ΧΑ = Νa+ – (Cl – + HCO3 – ) [φτ: < 11, (3 – 10 mEq/L)], και στον υπολογισμό του ΧΑ χρησιμοποιείται το μετρούμενο και όχι το διορθωμένο Νa+ (57).
Στη ΔΚ το ΧΑ, λόγω της συσσώρευσης του ακετοξεικού και β – υδροξυβουτυρικού οξέος, είναι συνήθως πολύ αυξημένο (> 20 mEq/L) η αύξηση δε αυτή είναι ανάλογη της μείωσης των διττανθρακικών του ορού.
Το ΧΑ ποικίλλει και εξαρτάται από τη διάρκεια και το ρυθμό παραγωγής και της απώλειας των ανιόντων κετοξέων στα ούρα καθώς και από την επάρκεια της αντιρροπιστικής αναπνευστικής αλκάλωσης. Η ποσότητα δε των ανιόντων κετοξέων που απεκκρίνονται εξαρτάται από το βαθμό της σπειραματικής διήθησης. Οι ασθενείς με φυσιολογική νεφρική λειτουργία μπορούν να αποβάλουν μεγάλες ποσότητες κετοξέων έως 30% του φορτίου των κετοξέων, γεγονός που ελαττώνει το ΧΑ ενώ η μετατροπή του ακετοξεικού σε ακετόνη μπορεί επιπλέον να μειώσει κατά 15 – 25% το φορτίο των υπαρχουσών στον οργανισμό κετοξέων (58, 59).
Ωστόσο, το ΧΑ μπορεί να οδηγήσει σε υποεκτίμηση της βαρύτητας της οξέωσης. Η απέκκριση με τα ούρα ανιόντων κετοξέων (όπως αλάτων Νa+ και Κ+) μειώνει το ΧΑ χωρίς όμως να επηρεάζει τη συγκέντρωση των διττανθρακικών στον ορό και επομένως το βαθμό της οξέωσης (57, 58). Με τη χορήγηση της ινσουλίνης τα ανιόντα των κετοξέων μεταβολίζονται με αποτέλεσμα τη δημιουργία διττανθρακικών και τη διόρθωση της μεταβολικής οξέωσης. Έτσι, τα ανιόντα των κετοξέων ονομάζονται «δυνητικά διττανθρακικά» και η απώλειά τους στα ούρα μπορεί να αντιπροσωπεύει απώλεια διττανθρακικών. Λόγω της νεφρικής απώλειας αυτών των πρόδρομων των διττανθρακικών κατά τη διάρκεια της θεραπείας παρατηρείται φυσιολογικό ΧΑ.
7.6. Ωσμωτικότητα ορού
Η ολική ωσμωτικότητα προσδιορίζεται από τις συγκεντρώσεις των διαλυμένων ουσιών στο πλάσμα όπως άλατα νατρίου, γλυκόζη και ουρία και υπολογίζεται σύμφωνα με τον τύπο: Ολική ωσμωτικότητα (mosmol/kg) = [2 x Na+ (mEq/L)] + [γλυκόζη (mg/dL) : 18] + [BUN (mg/dL) : 2,8] όπου BUN είναι το άζωτο ουρίας. Η δραστική ωσμωτικότητα διαφέρει από την ολική ως προς τη συγκέντρωση της ουρίας η οποία δεν συμπεριλαμβάνεται στον υπολογισμό της γιατί η ουρία είναι ουσία ελεύθερα διαπερατή από τις κυτταρικές μεμβράνες, η συγκέντρωσή της δεν προκαλεί ωσμωτική διαφορά διαμέσου των κυτταρικών μεμβρανών και επομένως σημαντική αλλαγή στον ενδο – και εξωκυττάριο χώρο. Η δραστική ωσμωτικότητα υπολογίζεται σύμφωνα με τον τύπο Osm (mosmol/kg)= [2 x Na+ (mΕq/L)] + [γλυκόζη (mg/dL) : 18].
Εκτός από την ωσμωτικότητα ορού μπορεί να υπολογιστεί και το έλλειμμα ύδατος. Το ύδωρ, είναι μειωμένο λόγω της ωσμωτικής διούρησης και το έλλειμμα ύδατος υπολογίζεται σύμφωνα με τον τύπο: Η20= 0,6 x ΒΣ x [(Νa+/140) – 1].
7.7. Νάτριο ορού
Τα επίπεδα του Νa+ στον ορό των ασθενών με ΔΚ ή ΥΥ ανευρίσκονται συνήθως χαμηλά, μπορεί όμως να είναι φυσιολογικά ή αυξημένα. Η υπεργλυκαιμία αυξάνει την ωσμωτικότητα του πλάσματος με αποτέλεσμα τη μετακίνηση ύδατος από τον ενδο – στον εξωκυττάριο χώρο και επακόλουθη μείωση, λόγω αραίωσης, της συγκέντρωσης του Νa+. Έχει υπολογιστεί ότι για κάθε αύξηση της γλυκόζης κατά 100 mg/dl τα επίπεδα του Νa+ ελαττώνονται κατά 1,6 mEq/L. Το διορθωμένο νάτριο υπολογίζεται σύμφωνα με τον τύπο: Διορθωμένο Νa+ =Na+ + 1,6 x [γλυκόζη (mg/dl) – 100] /100. Όταν τα επίπεδα της γλυκόζης είναι πολύ αυξημένα (>400 mg/dl) υπάρχει ακόμη μεγαλύτερη μείωση του Na+ και η συγκέντρωση του Na+ προσδιορίζεται επακριβώς όταν, για κάθε αύξηση γλυκόζης κατά 100 mg/dL, ως διορθωτικός παράγοντας χρησιμοποιείται το 2,4 mEq/L αντί του 1,6 mEq/L (60). Ψευδώς χαμηλά επίπεδα Na+ (ψευδο – υπονατριαιμία) παρατηρούνται σε καταστάσεις υπερτριγλυκεριδαιμίας ή υπερπρωτεΐναιμίας και ο προσδιορισμός του Νa+ γίνεται με συγκεκριμένες εργαστηριακές τεχνικές (φωτομετρία φλόγας και έμμεση ποτενσιομετρία) οι οποίες λόγω της αραίωσης του δείγματος ενδέχεται να δώσουν ψευδώς χαμηλές τιμές Νa+ (61).
Τα επίπεδα του Na+ μπορεί επίσης να βρεθούν, λόγω της σοβαρής αφυδάτωσης, αυξημένα ακόμα και αν το συνολικό Na+ του σώματος είναι μειωμένο. Επίσης, η υπεργλυκαιμία προκαλεί γλυκοζουρία, που οδηγεί σε ωσμωτική διούρηση με αποτέλεσμα την απώλεια ύδατος σε μεγαλύτερο βαθμό από τις απώλειες του Κ+ και του Να+ και η υπερνατριαιμία, παρά την παρουσία της υπεργλυκαιμίας, να επιτείνεται όταν η πρόσληψη ύδατος είναι ανεπαρκής (62).
Η διόρθωση της υπεργλυκαιμίας κατά τη διάρκεια της θεραπείας με τη χορήγηση ινσουλίνης και ισότονων διαλυμάτων, επιφέρει μείωση της ωσμωτικότητας του πλάσματος με αποτέλεσμα τη μετακίνηση ύδατος από τον εξω – στον ενδοκυττάριο χώρο και αύξηση έτσι της συγκέντρωσης του Να+ στον ορό (14, 60). Ένας ασθενής πχ με φυσιολογικά επίπεδα Na+ πριν από την έναρξη της θεραπείας, μπορεί να εμφανίσει κατά τη διάρκεια της θεραπείας υπερνατριαιμία.
7.8. Κάλιο ορού
Τα επίπεδα του Κ+ στον ορό αρχικά, παρά την υπάρχουσα σημαντική ένδεια του ολικού Κ+ του σώματος (300 – 600 mEq/L) μπορεί να είναι υψηλά, ή φυσιολογικά (63). Η ένδεια του Κ+ οφείλεται κυρίως σε νεφρικές και σε κάποιες περιπτώσεις σε γαστρεντερικές απώλειές του. Η αύξηση της νεφρικής αποβολής του Κ+ οφείλεται στην ωσμωτική διούρηση και στο δευτεροπαθή υπεραλδοστερονισμό που αναπτύσσεται λόγω της υπογκαιμίας. Οι απώλειες του Κ+ θα έπρεπε φυσιολογικά να οδηγούν σε υποκαλιαιμία. Ωστόσο, η ανεπάρκεια της ινσουλίνης, η υπερωσμωτικότητα και η οξέωση προκαλούν μετακίνηση του Κ+ από τον ενδοκυττάριο στον εξωκυττάριο χώρο με αποτέλεσμα αρχικά τα επίπεδα του Κ+ να είναι φυσιολογικά ή υψηλά. (63, 64). Στη ΔΚ, αν και συμβαίνει διαμεμβρανική ανταλλαγή ιόντων Κ+ με ιόντα Η+, η οξέωση φαίνεται να μην παίζει τον κυρίαρχο ρόλο στην εξωκυττάρια μετακίνηση του Κ+ (63). Ανεξάρτητα από τα αρχικά επίπεδα του Κ+, η θεραπεία με ινσουλίνη και η ενυδάτωση προκαλούν μείωση των επιπέδων του Κ+ και για το λόγο αυτό είναι απαραίτητη η στενή παρακολούθηση των τιμών του Κ+ ορού και η ανάλογη αντιμετώπιση των διαταραχών του.
7.9. Φωσφόρος ορού
Ο φωσφόρος είναι ενδοκυττάριο ιόν και οι ασθενείς με ΔΚ ή ΥΥ εμφανίζουν ένδεια φωσφόρου ανάλογη εκείνης του Κ+. Λόγω της ωσμωτικής διούρησης παρατηρείται νεφρική απώλεια φωσφόρου. Η έλλειψη της ινσουλίνης και η οξέωση προκαλούν μετακίνηση φωσφόρου έξω από τα κύτταρα και έτσι, αρχικά, ο φώσφορος είναι συνήθως φυσιολογικός ή αυξημένος (65). Η θεραπεία με ινσουλίνη έχει σαν αποτέλεσμα την ανάδειξη των ελλειμμάτων του φωσφόρου όπως συμβαίνει και με το Κ+.
7.10. Άλλες εργαστηριακές εξετάσεις
Στους ασθενείς με ΔΚ η αμυλάση και η λιπάση του ορού είναι συχνά αυξημένες παρά την απουσία παγκρεατίτιδας (66). Η παγκρεατίτιδα αποτελεί έναν από τους εκλυτικούς παράγοντες των οξέων υπεργλυκαιμικών διαταραχών και η πιθανότητα διάγνωσής της ενισχύεται όταν, παρά τη χορηγούμενη θεραπεία με ινσουλίνη, δεν παρατηρείται μείωση της αμυλάσης ορού και υποχώρηση του κοιλιακού άλγους.
Oι ασθενείς με ΔΚ εμφανίζουν συχνά λευκοκυττάρωση, παρά την απουσία λοίμωξης, η οποία οφείλεται τόσο στην αύξηση των αντιρροπιστικών ορμονών του stress (κορτιζόλης και κατεχολαμινών) όσο και στην αύξηση των κυτταροκινών. Η λευκοκυττάρωση είναι ανάλογη του βαθμού της κετοναιμίας, ωστόσο αριθμός λευκών αιμοσφαιρίων > 25.000 εγείρει την πιθανότητα συνύπαρξης λοίμωξης (67, 68).
Η ουρία και η κρεατινίνη, λόγω της αφυδάτωσης και του πρωτεϊνικού καταβολισμού, είναι συνήθως αυξημένες, ενώ ο αιματοκρίτης είναι αυξημένος εξαιτίας της αιμοσυμπύκνωσης. Ψευδώς υψηλές τιμές κρεατινίνης παρατηρούνται όταν ο προσδιορισμός της γίνεται με εργαστηριακές μεθόδους που επηρεάζονται από την παρουσία κετοναιμίας. Τα λιπίδια (τριγλυκερίδια, χυλομικρά, VLDL) είναι συνήθως αυξημένα ενώ τα επίπεδα τους μειώνονται σημαντικά εντός 24 ωρών από την έναρξη της χορήγησης της ινσουλίνης (69).
8. Διαφορική διάγνωση
Η διαφορική διάγνωση των οξέων επιπλοκών του ΣΔ αφορά εκείνες τις καταστάσεις στις οποίες παρατηρούνται ένα ή περισσότερα από τα τρία μεταβολικά χαρακτηριστικά της ΔΚ και της ΥΥ δηλαδή η υπεργλυκαιμία, η κέτωση και η οξέωση. Η κετοξέωση αλκοολικής αιτιολογίας και η κέτωση που εμφανίζεται μετά από νηστεία μεγάλης χρονικής διάρκειας διαφέρουν από τη ΔΚ εκτός από το ιστορικό και ως προς τα επίπεδα της γλυκόζης ορού, τα οποία είναι συνήθως φυσιολογικά, χαμηλά ή ελαφρώς αυξημένα. Κέτωση λόγω νηστείας μπορεί επίσης να παρατηρηθεί και στην εγκυμοσύνη η οποία είναι μια κατάσταση που συνδυάζεται με επιταχυνόμενη νηστεία και λιπόλυση, με αποτέλεσμα η κετογένεση να ξεκινάει νωρίς μέσα σε 6 ώρες νηστείας και να είναι έντονη. Στην αλκοολική κετοξέωση υπάρχει αρκετά σοβαρή οξέωση, ενώ στην κέτωση λόγω νηστείας τα επίπεδα των κετοξέων δεν είναι ιδιαίτερα αυξημένα (70).
Διαφορική διάγνωση της ΔΚ πρέπει επίσης να γίνει από τις καταστάσεις εκείνες στις οποίες υπάρχει μεταβολική οξέωση με αυξημένο ΧΑ όπως τη γαλακτική οξέωση, τη χρόνια νεφρική ανεπάρκεια και τη δηλητηρίαση από φάρμακα (σαλικυλικά μεθανόλη, αιθυλενγλυκόλη). Η διαφορική διάγνωση γίνεται με το ιστορικό, τη μέτρηση του γαλακτικού οξέος και της κρεατινίνης στον ορό καθώς και τον προσδιορισμό, εφόσον αυτό είναι αναγκαίο και εφικτό, των επιπέδων των φαρμάκων στο αίμα, ενώ σε καμία από τις καταστάσεις αυτές δεν παρατηρείται παρουσία κετονικών σωμάτων. Η διαφορική διάγνωση της ΔΚ και της ΥΥ από άλλες καταστάσεις με οξέωση ή κέτωση φαίνεται στον Πίνακα 4.
Πίνακας 4. Διαφορική διάγνωση της ΔΚ και της ΥΥ από άλλες καταστάσεις με οξέωση ή κέτωση.
| ΔΚ | Κέτωση νηστείας | Κέτωση κύησης | Αλκοολική κετοξέωση | Γαλακτική οξέωση |
Ουραιμική οξέωση |
Σαλικυλικά | Μεθανόλη ή αιθυλενγλυκόλη |
ΥΥ | |
| pΗ | ↓ | Φ | Φ ή ↓ | ↓ | ↓ | ↓ | ↓ ή ↑ | ↓ | Φ |
| γλυκόζη | ↑ | Φ | Φ ή ↑ | Φ ή ↓ | Φ | Φ | Φ ή ↓ | Φ | ↑↑ |
| ΧΑ | ↑ | Φ ή ↑ | Φ ή ↑ | ↑ | ↑ | ↑ | ↑ | ↑ | Φ |
| κετόνες | ↑↑ | ↑ | ↑ | ↑↑* | Φ | Φ | Φ | Φ | Φ |
| Ωσμωτικότητα ορού | Φ | Φ | Φ | Φ | Φ | ↑ | Φ | ↑↑ | ↑↑ |
Φ: φυσιολογικό
*: μεγάλη αύξηση του β – υδροξυβουτυρικού οξέος
Αναπροσαρμογή από Kitabchi A et al 2006 (35).
9. Θεραπεία
Οι ΔΚ και ΥΥ είναι επείγουσες καταστάσεις οι οποίες απαιτούν άμεση θεραπευτική αντιμετώπιση και εντατική παρακολούθηση. Η θεραπευτική προσέγγιση είναι παρόμοια και στις δύο καταστάσεις και έχει ως στόχο την αποκατάσταση του ενδαγγειακού όγκου, τη διευκόλυνση της νεφρικής άρδευσης, τη σταδιακή ελάττωση της ωσμωτικότητας, την ελάττωση των επιπέδων σακχάρου, καθώς και την αναγνώριση των εκλυτικών παραγόντων, όπως πχ λοίμωξη ή οξύ έμφραγμα του μυοκαρδίου, που οδήγησαν στην εμφάνισή τους. Στις περιπτώσεις των ασθενών που εμφανίζουν μείωση του επιπέδου συνείδησης είναι απαραίτητη η διατήρηση της βατότητας των αναπνευστικών οδών και η εξασφάλιση καλής οξυγόνωσης. Η θεραπεία της ΔΚ και της ΥΥ περιλαμβάνει την ενυδάτωση, τη χορήγηση ινσουλίνης, τη διόρθωση των ηλεκτρολυτικών διαταραχών καθώς και την αντιμετώπιση των πιθανών εκλυτικών παραγόντων.
Πίνακας 5. Προσθήκη Κ+ στα χορηγούμενα διαλύματα υγρών ανάλογα με τα επίπεδα Κ+ ορού.
| Κ+ ορού (mEq/L) | προσθήκη Κ+ στα διαλύματα υγρών |
| > 5,2 | Όχι Κ+Επανέλεγχος σε 2 ώρες |
| 3,3 – 5,2 | 20 – 30 mEq/L χορηγούμενων διαλυμάτωνώστε να το Κ+ να διατηρείται μεταξύ 4 – 5 mEq/L |
| < 3,3 | 20 – 30 mEq/ώρα έως Κ+ >3,3 mEq/L |
Αναπροσαρμογή από Kitabchi A et al. 2009 (6).
Η παρακολούθηση των ασθενών περιλαμβάνει τη μέτρηση ανά ώρα των επιπέδων της γλυκόζης ορού μέχρι τη σταθεροποίησή τους και ανάλογα με τη βαρύτητα της διαταραχής και την απάντηση στη θεραπεία, βασικό βιοχημικό έλεγχο (πχ προσδιορισμός ουρίας, κρεατινίνης και ηλεκτρολυτών) και τον προσδιορισμό της ωσμωτικότητας του πλάσματος και του pH κάθε 2 έως 4 ώρες (4, 6). Για την εκτίμηση της πορείας της ΔΚ είναι επίσης χρήσιμη η μέτρηση άμεσα του β – υδροξυβουτυρικού οξέος στο αίμα και ο υπολογισμός του ΧΑ. Για την καλύτερη παρακολούθηση των ασθενών προτείνεται να γίνεται καταγραφή των βασικών κλινικών και εργαστηριακών παραμέτρων σε ειδικό έντυπο παρακολούθησης (Πίνακας 6).
Πίνακας 6. Έντυπο παρακολούθησης ασθενών με ΔΚ ή ΥΥ.
| Ώρα | ||||||||
| Αρτηριακή Πίεση | ||||||||
| Σφύξεις | ||||||||
| Θερμοκρασία | ||||||||
| Επίπεδο συνείδησης* | ||||||||
| Αναπνοή | ||||||||
| Γλυκόζη ορού | ||||||||
| Κετόνες | ||||||||
| Κ+ ορού | ||||||||
| Νa+ ορού | ||||||||
| Ουρία | ||||||||
| Κρεατινίνη | ||||||||
| Ωσμωτικότητα ορού | ||||||||
| pH | ||||||||
| HCO3_ | ||||||||
| Προσλαμβανόμενα υγρά | ||||||||
| Αποβαλλόμενα υγρά | ||||||||
| Ινσουλίνη/ώρα |
*: Ε εγρήγορση, Υ υπνηλία, Λ λήθαργος, Κ κώμα
Η Αμερικάνικη Διαβητολογική Εταιρεία (ADA) πρότεινε το 2009 θεραπευτικούς αλγόριθμους τόσο για τη ΔΚ όσο και για την ΥΥ, ωστόσο, το σημαντικότερο είναι η εντατική παρακολούθηση καθώς και η εξατομίκευση της θεραπείας, ανάλογα με την κλινική και την εργαστηριακή εικόνα του κάθε ασθενούς (6). Η εφαρμογή θεραπευτικών αλγορίθμων βασισμένων στις συστάσεις της ADA μείωσε το χρονικό διάστημα που απαιτείται για την επίτευξη της λύσης της ΔΚ και της ΥΥ χωρίς να αυξήσει το ποσοστό της υπογλυκαιμίας ή της υποκαλιαιμίας (71).
9.1. Ενυδάτωση
Το πρώτο και κύριο βήμα στη θεραπευτική αντιμετώπιση της ΔΚ και της ΥΥ αποτελεί η ενδοφλέβια χορήγηση υγρών που αποσκοπεί στην αιμοδυναμική σταθεροποίηση του ασθενούς, την έκπτυξη του εξωκυττάριου χώρου, την άρδευση των ιστών, τη μείωση της υπερωσμωτικότητας, τη διόρθωση της νεφρικής λειτουργίας και την ελάττωση των επιπέδων των αντιρροπιστικών ορμονών (72, 73).
Το έλλειμμα των υγρών που παρατηρείται στη ΔΚ υπολογίζεται στα 3 – 6 L και στην ΥΥ στα 8 – 10 L και η διαφορά δε αυτή οφείλεται στη μεγαλύτερη ωσμωτική διούρηση που υπάρχει στην ΥΥ Το έλλειμμα των υγρών (περίπου 10 – 15% του ΣΒ) συνιστάται να διορθώνεται εντός των 24 πρώτων ωρών (4, 6). Ο ρυθμός χορήγησης των υγρών εξαρτάται από την αιμοδυναμική κατάσταση του ασθενούς το βαθμό δηλαδή της αφυδάτωσης καθώς και από την καρδιακή λειτουργία. Η μείωση της ωσμωτικότητας δεν πρέπει να γίνεται γρήγορα αλλά σταδιακά και ο ρυθμός μείωσής της να μην υπερβαίνει τα 3 mοsmol/kg/ώρα λόγω του κινδύνου εμφάνισης ανάπτυξης εγκεφαλικού οιδήματος που μπορεί να επιφέρει η ταχύτερη μείωσή της. Όταν δεν υπάρχει καρδιακή δυσλειτουργία, χορηγείται ισότονο διάλυμα ΝaCl 0,9% με ρυθμό 15 – 20 ml/Kg BΣ/ώρα ή έως 1 – 1,5 L κατά την πρώτη ώρα. Στα παιδιά χορηγούνται υγρά με ρυθμό 10 – 20 ml/Kg BΣ/ώρα κατά την πρώτη ώρα και όχι όμως περισσότερο από 50 ml/kg ΒΣ τις πρώτες 4 ώρες (6). Στη συνέχεια, το είδος και ο ρυθμός χορήγησης των υγρών εξαρτώνται από το βαθμό της αφυδάτωσης και της διούρησης και από τα επίπεδα του διορθωμένου Να+. Εάν τα επίπεδα του διορθωμένου Νa+ είναι χαμηλά χορηγείται ισότονο διάλυμα Ν/S 0,9% με ρυθμό χορήγησης 4 – 14 ml/Kg/ώρα (ή περίπου 250 – 500 ml/ώρα), ενώ εάν τα επίπεδα του διορθωμένου Νa+ είναι φυσιολογικά ή υψηλά χορηγείται υπότονο διάλυμα Ν/S 0,45% με τον ίδιο ρυθμό. Όταν τα επίπεδα της γλυκόζης προσεγγίζουν τα 200 mg/dl στη ΔΚ ή περίπου 250 – 300 mg/dl στην ΥΥ, προστίθεται διάλυμα γλυκόζης D/W 5% με ρυθμό 150 – 250 ml/ώρα (Εικόνα 4).
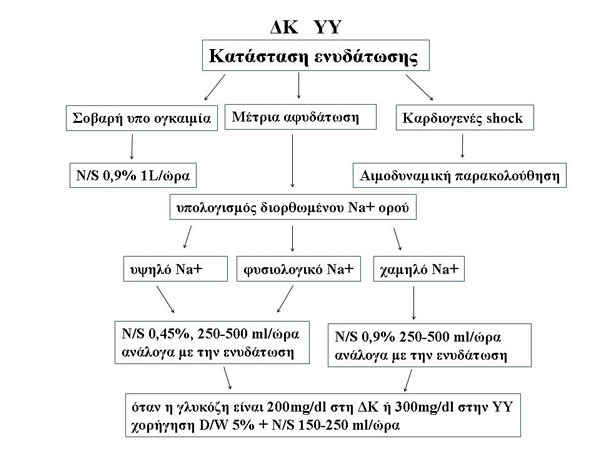
Εικόνα 4. Αναπλήρωση υγρών στη ΔΚ και την ΥΥ Αναπροσαρμογή από Kitabchi A et al 2009(6).
Η αποκατάσταση των υγρών αρχικά επιφέρει μείωση των επίπεδων γλυκόζης από 35 έως 70 mg/dL την ώρα λόγω αφενός της επιτευχθείσας αραίωσης και αφετέρου της αυξημένης νεφρικής απέκκρισής της (72). Ο ρυθμός μείωσης της γλυκόζης είναι μεγαλύτερος στην ΥΥ όπου υπάρχει και μεγαλύτερη υποογκαιμία.
Η επίτευξη της αποκατάστασης του ελλείμματος των υγρών, τόσο στα ηλικιωμένα άτομα όσο και στους ασθενείς με καρδιακή ή νεφρική ανεπάρκεια, είναι δύσκολη, λόγω της λεπτής ισορροπίας που απαιτείται μεταξύ της επίτευξης της διόρθωσης του ελλείμματος και της αποφυγής της υπερφόρτωσης με υγρά. Απαιτείται έτσι να γίνεται συχνότερος κλινικός και εργαστηριακός έλεγχος, επαναπροσδιορισμός του ελλείμματος και ενδεχομένως τροποποίηση του ρυθμού χορήγησης των υγρών (4, 72, 73).
9.2. Χορήγηση ινσουλίνης
Θεραπεία εκλογής αποτελεί η συνεχής ενδοφλέβια έγχυση ινσουλίνης ταχείας δράσης. Με τον τρόπο αυτό επιτυγχάνεται, ιδιαίτερα σε ασθενείς με υποογκαιμία και μειωμένη αιματική ροή, προβλέψιμη παροχή ινσουλίνης στους ιστούς. Η ινσουλίνη ταχείας δράσης έχει μικρό χρόνο ημίσειας ζωής στο πλάσμα (5 – 6 λεπτά) και μπορεί έτσι εύκολα να γίνει τιτλοποίηση της δόσης της. Συστήνεται η έγχυση της ινσουλίνης να γίνεται σε χαμηλές δόσεις των 6 – 10 U/ώρα. Σχήματα χορήγησης υψηλών δόσεων ινσουλίνης, της τάξεως των 20 – 30 U/ώρα, που χρησιμοποιούνταν στο παρελθόν, ενέχουν τον κίνδυνο της ταχείας μείωσης της ωσμωτικότητας και της πιθανής ανάπτυξης υπογλυκαιμίας, υποκαλιαιμίας ή εγκεφαλικού οιδήματος (74, 75). Για την ταχύτερη ενεργοποίηση των υποδοχέων ινσουλίνης χορηγείται συνήθως αρχικά μία bolus ενδοφλέβια δόση ινσουλίνης της τάξεως 0,1 – 0,15 U/Kg ΒΣ πριν από τη χορήγηση της συνεχούς έγχυσης ινσουλίνης με ρυθμό 0,1 U/Kg ΒΣ/ώρα (76, 77). Ωστόσο, η χορήγηση της αρχικής bolus δόσης ινσουλίνης δεν φαίνεται να προσφέρει σημαντικό όφελος στους ασθενείς. Η αρχική bolus δόση της ινσουλίνης μπορεί να παραλειφθεί εάν οι ασθενείς λάβουν ινσουλίνη σε συνεχή ενδοφλέβια έγχυση με μεγαλύτερο ρυθμό, δηλαδή της τάξεως των 0,14 U/Κg ΒΣ/ώρα (10 U/ώρα σε ασθενή 70 Κg) (78, 79). Και οι δύο τρόποι χορήγησης της ινσουλίνης είναι αποδεκτοί, η δε δοσολογία της ινσουλίνης είναι παρόμοια τόσο στη ΔΚ όσο και στην ΥΥ.
Η χορήγηση της ινσουλίνης πρέπει να γίνεται με την έναρξη της χορήγησης των υγρών και αφού πρώτα αποκλειστεί η παρουσία υποκαλιαιμίας (δηλαδή Κ+ < 3,3 mEq/L). Πρακτικά, η ινσουλίνη χορηγείται με ανεξάρτητο σύστημα ενδοφλέβιας έγχυσης: διαλύονται 50 U ινσουλίνης ταχείας δράσης σε 500 ml διαλύματος N/S 0,9% έτσι ώστε το διάλυμα να περιέχει 0,1 U/ml N/S 0,9% και ο ρυθμός χορήγησης να μπορεί να ρυθμιστεί με ακρίβεια. Όταν χορηγούμε πχ 70 ml/ώρα χορηγούμε 7 U ινσουλίνης/ώρα. Με τον προτεινόμενο αυτόν ρυθμό έγχυσης ινσουλίνης, ο ρυθμός πτώσης της γλυκόζης είναι της τάξης των 50 – 70mg/dL την ώρα (77, 78, 81). Αν η πτώση αυτή των τιμών γλυκόζης δεν επιτευχθεί μετά την πρώτη ώρα, χορηγούνται 0,14 U/Kg ΒΣ ινσουλίνης bolus και ακολουθείται το προηγούμενο σχήμα. Αν παρόλα αυτά δεν επιτευχθεί η επιθυμητή μείωση των επιπέδων της γλυκόζης θα πρέπει να ελεγχθεί το επίπεδο ενυδάτωσης του ασθενούς, να επαναπροσδιοριστεί και αντιμετωπιστεί ο εκλυτικός παράγοντας απορρύθμισης της γλυκόζης και να ελεγχθεί το σύστημα χορήγησης της ινσουλίνης για παρουσία πιθανού τεχνικού προβλήματος. Όταν τα επίπεδα της γλυκόζης ορού μειωθούν στα 200 mg/dL στην ΔΚ και στα 250 – 300 mg/dL στην ΥΥ προστίθεται διάλυμα γλυκόζης D/W 5% και μειώνεται ο ρυθμός έγχυσης της ινσουλίνης σε 0,02 – 0,05 U/Κg ΒΣ/ώρα (3 – 4 U/h) έτσι ώστε να επιτυγχάνονται επίπεδα γλυκόζης της τάξεως των 150 – 200 mg/dl μέχρι τη διόρθωση της οξέωσης ή 250 – 300 mg/dl μέχρι τη διόρθωση της υπερώσμωσης (4, 76). Η προσθήκη διαλύματος γλυκόζης D/W 5% είναι απαραίτητη για την αποφυγή της γρήγορης διόρθωσης της υπεργλυκαιμίας, της ταχείας πτώσης της ωσμωτικότητας και της πιθανής πρόκλησης εγκεφαλικού οιδήματος. Επίσης, με την παροχή στον οργανισμό της κατάλληλης ποσότητας γλυκόζης, γίνεται δυνατή η προαγωγή του μεταβολισμού των κετονικών σωμάτων μέχρι τον έλεγχο της οξέωσης. Η διόρθωση της οξέωσης γίνεται με βραδύτερο ρυθμό (10 – 12 ώρες) σε σχέση με την υπεργλυκαιμία (4 – 8 ώρες) και για το λόγο αυτό δεν πρέπει να διακόπτεται η χορήγηση της ινσουλίνης όταν η συγκέντρωση της γλυκόζης πλησιάζει τα φυσιολογικά επίπεδα (κίνδυνος υποτροπής). Η προτεινόμενη χορήγηση ινσουλίνης στη ΔΚ και στην ΥΥ φαίνεται στην Εικόνα 5.

Εικόνα 5. Χορήγηση ινσουλίνης στη ΔΚ και την ΥΥ Αναπροσαρμογή από Kitabchi A et al 2009(6).
Εναλλακτικά, οι ασθενείς που δεν βρίσκονται σε καταπληξία (shock) αντί της ενδοφλέβιας συνεχούς έγχυσης ινσουλίνης ταχείας δράσης μπορεί να χορηγηθεί ινσουλίνη ενδομυϊκά ή υποδορίως. Η ενδομυϊκή ή υποδόρια χορήγηση ινσουλίνης, αν και χρησιμοποιείται σπάνια στη θεραπεία της ΔΚ ή της ΥΥ είναι χαμηλότερου κόστους αλλά εξίσου αποτελεσματική με την ενδοφλέβια συνεχή έγχυση και προτείνεται η χρήση της για την αντιμετώπιση ήπιων διαταραχών σε χώρο εξωτερικών ιατρείων εξειδικευμένων κέντρων.
Επίσης, σε ασθενείς με μέτριας βαρύτητας ΔΚ χορηγήθηκαν υποδόρια ανάλογα ινσουλίνης ταχείας δράσεως κάθε 1 ώρα (lispro ή aspart) (82, 83). Οι ασθενείς οι οποίοι έλαβαν υποδόρια ανάλογα ινσουλίνης δεν εμφάνισαν διαφορές στη διάρκεια της θεραπείας μέχρι την επίτευξη της διόρθωσης της υπεργλυκαιμίας και της λύσης της ΔΚ σε σχέση με εκείνους που έλαβαν ενδοφλέβια έγχυση ινσουλίνης ταχείας δράσης.
Επιπλέον, εξετάσθηκε εάν η θεραπεία με υποδόρια ανάλογα ινσουλίνης σε διαφορετικά χρονικά διαστήματα (κάθε 1 ή 2 ώρες) είναι εξίσου αποτελεσματική με την ενδοφλέβια έγχυση ινσουλίνης ταχείας δράσης (83). Η αρχική δόση έναρξης της ινσουλίνης ήταν 0,2 U/Kg ΒΣ και στη συνέχεια η δόση ήταν 0,1 U/Kg ΒΣ κάθε 1 ώρα ή η αρχική δόση έναρξης ήταν 0,3 U/Kg ΒΣ και στην συνέχεια 0,2 U/Kg ΒΣ κάθε 2 ώρες μέχρι τα επίπεδα της γλυκόζης να φτάσουν τα 250mg/dl όπου η δόση της ινσουλίνης μειώθηκε σε 0,05 ή 0,1 U/Kg ΒΣ κάθε 1 ή 2 ώρες αντίστοιχα. Τα αποτελέσματα ήταν συγκρίσιμα με εκείνα της ενδοφλέβιας συνεχούς έγχυσης ινσουλίνης ταχείας δράσης. Ωστόσο, η θεραπεία με υποδόρια ανάλογα ινσουλίνης δεν είναι ευρέως χρησιμοποιούμενη γιατί με την υποδόρια χορήγηση αναλόγων ινσουλίνης υπάρχει δυσκολία στην τιτλοποίηση της δόσης της χορηγούμενης ινσουλίνης, ανάγκη για νοσηλευτική παρέμβαση κάθε ώρα καθώς και έλλειψη εμπειρίας του προσωπικού σε σχέση με την κλασική ενδοφλέβια έγχυση ινσουλίνης ταχείας δράσης. Σε μία άλλη μελέτη συγκρίθηκε η ενδοφλέβια έγχυση ινσουλίνης ταχείας δράσης regular με την ενδοφλέβια έγχυση ανάλογου ινσουλίνης ταχείας δράσης glulisine (84). Οι δόσεις της ινσουλίνης ήταν παρόμοιες με εκείνες που συστήνονται από την ADA, δηλαδή αρχικά 0.1 U/Κg ΒΣ ενδοφλέβια bolus, στη συνέχεια έγχυση σε δόση 0.1 U/Κg ΒΣ την ώρα. Στις δύο ομάδες δεν παρατηρήθηκαν διαφορές στη μέση διάρκεια της θεραπείας, στην ποσότητα της χορηγούμενης ινσουλίνης και στη μέση διάρκεια έγχυσης της ινσουλίνης μέχρι τη λύση της ΔΚ. Επομένως, τόσο η ινσουλίνη ταχείας δράσης όσο και το ανάλογο ταχείας δράσης είναι εξίσου δραστικά και η επιλογή του είδους της ινσουλίνης βασίζεται στην κλινική εμπειρία, το κόστος και την προτίμηση του εκάστοτε κέντρου.
9.3. Χορήγηση Καλίου
Η ένδεια του Κ+ είναι η πιο σημαντική ηλεκτρολυτική διαταραχή που παρατηρείται τόσο στη ΔΚ όσο στην ΥΥ. Αρχικά, λόγω της ανεπάρκειας της ινσουλίνης και της υπερώσμωσης, το Κ+ του ορού μπορεί να είναι φυσιολογικό ή ακόμα και αυξημένο, αλλά στη συνέχεια η χορήγηση της ινσουλίνης οδηγεί γρήγορα σε σημαντική ελάττωση των επιπέδων του Κ+ λόγω μετακίνησής του εντός των κυττάρων (63, 85). Η αναπλήρωση των ελλειμμάτων του Κ+ (20 – 30 mΕq/L) ξεκινάει όταν τα επίπεδα Κ+ στον ορό είναι μικρότερα από 5,2 mΕq/L και υπάρχει ικανοποιητική διούρηση (> 50 mL/ώρα). Εάν τα επίπεδα Κ+ ορού είναι < 3,3 mEq/L πριν από την έναρξη χορήγησης της ινσουλίνης απαιτείται πρώτα να γίνεται διόρθωση της υποκαλιαιμίας η οποία θα επιδεινωθεί περαιτέρω από την ινσουλίνη. Για την αποφυγή της εμφάνισης, λόγω της επιδείνωσης της υπάρχουσας υποκαλιαιμίας, επιπλοκών, όπως της απειλητικής για τη ζωή του ασθενούς καρδιακής αρρυθμίας ή της αδυναμίας των αναπνευστικών μυών, στα διαλύματα των χορηγούμενων υγρών προστίθεται Κ+ (86). Εάν όμως τα επίπεδα του Κ+ είναι υψηλά ή ο ασθενής είναι ανουρικός δεν χορηγείται Κ+ και τα επίπεδα του Κ+ πρέπει να επαναπροσδιοριστούν δύο ώρες μετά την έναρξη της χορήγησης της ινσουλίνης. Στόχος της θεραπείας είναι η διατήρηση επιπέδων Κ+ μεταξύ 4 – 5 mEq/L. Για την αποφυγή δε της υπερφόρτισης με χλώριο και για την πρόληψη ανάπτυξης υποφωσφοραιμίας συνίσταται η διόρθωση των ελλειμμάτων του Κ+ να γίνεται με τη χορήγηση τόσο χλωριούχου όσο και φωσφορικού Κ+, δηλαδή τα 2/3 της συνολικής χορηγούμενης δόσης Κ+ να είναι χλωριούχο Κ+ και το 1/3 φωσφορικό Κ+. Αν ο ασθενής είναι αιμοδυναμικά σταθερός είναι προτιμότερο η προσθήκη του Κ+ να γίνεται σε ημι – ισότονο διάλυμα γιατί το Κ+, το οποίο ως ωσμωτικά δρών ιόν, όταν προστίθεται σε ισότονο διάλυμα το μετατρέπει σε υπέρτονο, με αποτέλεσμα την καθυστέρηση της διόρθωσης της υπερώσμωσης. Η προτεινόμενη προσθήκη Κ+ στους ορούς βάση των επιπέδων Κ+ στον ορό φαίνονται στον Πίνακα 5.
9.4. Διττανθρακικά
Η χορήγηση διττανθρακικών στη ΔΚ παραμένει αμφιλεγόμενη καθώς είναι ελλιπή τα δεδομένα που αποδεικνύουν ότι ωφελεί η χορήγησή τους (87, 88). Στους περισσότερους ασθενείς η χορήγηση των υγρών και της ινσουλίνης επαρκούν για τη διόρθωση της οξέωσης χωρίς να απαιτείται επιπλέον η προσθήκη διττανθρακικών. Η ινσουλίνη, σε περιβάλλον με pH > 7, αρκεί από μόνη της να αναστείλει τη λιπόλυση και την παραγωγή κετοξέων. Τα κετοξέα που έχουν ήδη παραχθεί, οξειδώνονται στους περιφερικούς ιστούς με αποτέλεσμα την παραγωγή ΗCO3 – . Ωστόσο, η σοβαρή μεταβολική οξέωση συνδέεται με ενδοκυττάρια οξέωση, η οποία έχει αρνητικές επιδράσεις σε διάφορα όργανα (καρδιά, ΚΝΣ, ήπαρ) προκαλώντας, λόγω αρνητικής ινότροπης δράσης στο μυοκάρδιο, βραδυκαρδία, αρρυθμία, υπόταση, καθώς και περιφερική και εγκεφαλική αγγειοδιαστολή. Η χορήγηση όμως διττανθρακικών έχει πολλές αρνητικές επιδράσεις και μπορεί να προκαλέσει: α) επιδείνωση της υποκαλιαιμίας, λόγω αλκάλωσης και μετακίνησης του Κ+ εντός των κυττάρων, οδηγώντας έτσι σε εμφάνιση καρδιακής αρρυθμίας, β) παράδοξη ενδοκυττάρια οξέωση καθώς και οξέωση του ΚΝΣ, λόγω αυξημένης παραγωγής και διάχυσης του CO2 στο εγκεφαλονωτιαίο υγρό το οποίο περνάει γρήγορα τον αιματοεγκεφαλικό φραγμό, γ) καθυστέρηση της λύσης της κέτωσης, δ) ιστική υποξία, λόγω ελαττωμένης απελευθέρωσης Ο2 από την αιμοσφαιρίνη στους ιστούς και ε) βαριές τοπικές νεκρώσεις εάν φτάσει από λάθος στον υποδόριο ιστό επειδή το διάλυμα των διττανθρακικών είναι εξαιρετικά ερεθιστικό.
Τα διττανθρακικά χορηγούνται μόνο σε περιπτώσεις που υπάρχει σοβαρή οξέωση, δηλαδή pH < 6,90 και πιθανότητα επομένως επιδείνωσης της κλινικής κατάστασης χωρίς τη χορήγησή τους. Επειδή όμως η χορήγηση των διττανθρακικών μπορεί να ελαττώσει τα επίπεδα του Κ+ συστήνεται, εάν τα επίπεδα Κ+ είναι < 5,3 mEq/L, η σύγχρονη προσθήκη Κ+ (20 mEq) στο διάλυμα χορηγήσεως των διττανθρακικών. Έτσι, χορηγούνται ενδοφλέβια 100 ml NaHCO3 (1fl) + 20 mEq KCl σε 400 ml υγρών (water for injection), με ρυθμό χορήγησης 200 ml/ώρα για 2 ώρες, γίνεται έλεγχος του pH σε 2 ώρες και επανάληψη της χορήγησης εάν το pH παραμένει < 7,0.
9.5. Φωσφόρος
Η συγκέντρωσή του φωσφόρου μειώνεται ταχέως με τη θεραπεία με ινσουλίνη με αποτέλεσμα την υποφωσφοραιμία όπως συμβαίνει και με το Κ+. Η υποφωσφοραιμία αυτή είναι συνήθως ασυμπτωματική και αυτοπεριοριζόμενη και στους περισσότερους ασθενείς δεν είναι απαραίτητη η συμπληρωματική χορήγηση φωσφόρου. Σπάνια, η υποφωσφοραιμία μπορεί να οδηγήσει σε μυϊκή αδυναμία, μειωμένη καρδιακή παροχή, αδυναμία αναπνευστικών μυών, ραβδομυόλυση, αιμόλυση, καθώς και ιστική υποξία λόγω δυσχέρειας αποδέσμευσης του Ο2 από την Ηb (μείωση του 2,3 – διφωσφογλυκερικoύ οξέος των ερυθροκυττάρων) (89). Προοπτικές τυχαιοποιημένες μελέτες δεν έδειξαν ιδιαίτερο όφελος από τη χορήγηση με φωσφόρου στους ασθενείς με ΔΚ η οποία μπορεί να οδηγήσει σε υπασβεστιαιμία και υπομαγνησιαιμία (90, 91).
Δεν συστήνεται επομένως η συστηματική χορήγηση φωσφόρου στη θεραπεία της ΔΚ, ενώ δεν υπάρχουν επαρκή δεδομένα για τη χορήγηση φωσφόρου σε ασθενείς με ΥΥ (6). Η χορήγηση του φωσφόρου στη ΔΚ γίνεται σε συμπτωματικούς ασθενείς οι οποίοι εμφανίζουν καρδιακή δυσλειτουργία, καταστολή του αναπνευστικού ή συμμετοχή των σκελετικών μυών, αναιμία, καθώς και σε ασθενείς με φυσιολογικό ασβέστιο ορού και επίπεδα φωσφόρου μικρότερα από 1,0 mg/dl. Προστίθενται στα ήδη χορηγούμενα διαλύματα αναπλήρωσης υγρών 20 – 30 mΕq/L φωσφορικού καλίου με μέγιστο ρυθμό χορήγησης τα 4,5 mmol/ώρα (1,5 ml/ώρα). Παράλληλα, για την αποφυγή της εμφάνισης υπασβεστιαιμίας κρίνεται απαραίτητη η παρακολούθηση των επιπέδων του ασβεστίου και του μαγνησίου ορού και η προσθήκη τους όπου κρίνεται απαραίτητο.
9.6. Λοιμώξεις
Αντιμικροβιακή θεραπεία δεν δίνεται σε όλους τους ασθενείς με ΔΚ ή ΥΥ. Όταν υπάρχει όμως λοίμωξη ή υπόνοια λοίμωξης χορηγούνται αντιβιοτικά ευρέως φάσματος εν αναμονή των αποτελεσμάτων του εργαστηριακού ελέγχου και των καλλιεργειών των βιολογικών υγρών.
10. Λύση της διαβητικής κετοξέωσης και της υπεργλυκαιμικής υπερώσμωσης
Κριτήρια λύσης της ΔΚ θεωρούνται η επίτευξη επιπέδων γλυκόζης ≤ 200 mg/dl, διττανθρακικών ≥ 18 mEq/L, pΗ > 7,3 και χάσματος ανιόντων < 12 mEq/L, ενώ της ΥΥ η επίτευξη ωσμωτικότητας < 320 mosm/Kg, επιπέδων γλυκόζης ≤ 300 mg/dl καθώς και ικανοποιητικού επιπέδου συνείδησης. Εάν επέλθει λύση της ΔΚ ή της ΥΥ και ο ασθενής μπορεί να σιτιστεί, τότε μπορεί να αρχίσει η υποδόρια χορήγηση ινσουλίνης σε πολλαπλές δόσεις. Όμως η απότομη διακοπή της ενδοφλέβιας χορήγησης ινσουλίνης πριν από την έναρξη της υποδόριας χορήγησής της μπορεί να επιδεινώσει τη γλυκαιμική ρύθμιση, γιατί η δράση της υποδορίως χορηγούμενης ινσουλίνης δεν είναι άμεση και έτσι η ενδοφλέβια χορήγηση ινσουλίνης πρέπει να διακόπτεται 1 – 2 ώρες μετά την έναρξη της υποδόριας χορήγησή της. Στους ασθενείς με γνωστό ιστορικό ΣΔ, οι οποίοι πριν από τη ΔΚ ή την ΥΥ ελάμβαναν θεραπεία με ινσουλίνη και είχαν καλή ρύθμιση, χορηγείται ινσουλίνη στις ίδιες δόσεις που ελάμβαναν πριν από το επεισόδιο της ΔΚ ή της ΥΥ. Στους ασθενείς, που θα χορηγηθεί ινσουλίνη για πρώτη φορά, πρωτοεμφανιζόμενος ΣΔ, συνιστάται η εφαρμογή σχήματος πολλαπλών ενέσεων ταχείας και μακράς δράσης ινσουλίνης με μέση ημερήσια δόση ινσουλίνης της τάξεως των 0,5 – 0,8 U/Kg ΒΣ.
11. Επιπλοκές κατά τη διάρκεια της θεραπείας
Οι πιο συχνές επιπλοκές της ΔΚ και ΥΥ είναι:
11.1. Υπογλυκαιμία και υποκαλιαιμία
Η υπογλυκαιμία και η υποκαλιαιμία, λόγω της χορήγησης μεγάλων δόσεων ινσουλίνης και της γρήγορης αναπλήρωσης των υγρών, ήταν στο παρελθόν συχνές επιπλοκές κατά τη διάρκεια της θεραπείας. Η εφαρμογή όμως πρωτοκόλλων χορήγησης χαμηλών δόσεων ινσουλίνης σε συνδυασμό με το συχνό προσδιορισμό τόσο της γλυκόζης στο τριχοειδικό αίμα όσο και του καλίου στον ορό, είχαν ως αποτέλεσμα τη σημαντική μείωση τόσο της υπογλυκαιμίας όσο και της υποκαλιαιμίας ως επιπλοκών της θεραπείας της ΔΚ και της ΥΥ (74).
11.2. Υπεργλυκαιμία
Μετά τη διόρθωση των επιπέδων της γλυκόζης εξαιτίας της πρόωρης διακοπής της ενδοφλέβιας χορήγησης ινσουλίνης κατά την έναρξη της υποδόριας χορήγησης ινσουλίνης, μπορεί να επανεμφανιστεί υπεργλυκαιμία.
11.3. Υπερχλωραιμική μεταβολική οξέωση
Υπερχλωραιμική μεταβολική οξέωση με φυσιολογικό χάσμα ανιόντων μπορεί να εμφανιστεί σε ασθενείς με φυσιολογική νεφρική λειτουργία και ικανοποιητική χορήγηση διαλυμάτων NaCl. Αυτό συμβαίνει γιατί το χλώριο που περιέχεται στα ενδοφλέβια διαλύματα αντικαθιστά τα ανιόντα κετοξέων τα οποία απεκκρίνονται ως άλατα Να+ και Κ+ με την ωσμωτική διούρηση. Οι ασθενείς με καλή νεφρική λειτουργία κατά τη διάρκεια της θεραπείας θα αποκαταστήσουν φυσιολογικό ΧΑ λόγω της νεφρικής αποβολής των κετοξέων (57, 92). Η διαταραχή αυτή είναι συνήθως παροδική και χωρίς ιδιαίτερη κλινική σημασία εκτός κι αν συνυπάρχει οξεία νεφρική ανεπάρκεια ή σοβαρή ολιγουρία.
11.4. Εγκεφαλικό οίδημα
Το εγκεφαλικό οίδημα είναι μία σπάνια και σοβαρή επιπλοκή της θεραπείας της ΔΚ και της ΥΥ η οποία παρατηρείται κυρίως σε παιδιά με ΔΚ (0,3 – 1% των περιπτώσεων) (94). Η θνητότητα των παιδιών εξαιτίας εγκεφαλικού οιδήματος είναι μεγάλη, ανέρχεται περίπου στο 20 – 40% των περιπτώσεων και ευθύνεται για το 57 – 87% όλων των θανάτων λόγω ΔΚ στα παιδιά (93, 94).
Εμφανίζεται συνήθως τις πρώτες 12 – 24 ώρες μετά την έναρξη της θεραπείας, ωστόσο μπορεί να προϋπάρχει σε υποκλινική μορφή και πριν από την έναρξη της θεραπείας. Υποψία παρουσίας εγκεφαλικού οιδήματος τίθεται όταν, ενώ η υπεργλυκαιμία και η οξέωση υποχωρούν, υπάρχει ταχύτατη επιδείνωση της κλινικής εικόνας και παρουσία συμπτωμάτων και σημείων όπως κεφαλαλγίας, λήθαργου, επιληπτικών σπασμών, οιδήματος οπτικών θηλών, ακράτειας, βραδυκαρδίας, αναπνευστικής ανακοπής ή εγκατάστασης κώματος. Σε ορισμένες περιπτώσεις η εγκατάσταση των συμπτωμάτων γίνεται τόσο ταχέως ώστε να μην παρατηρείται οίδημα οπτικής θηλής.
Διάφοροι παθογενετκοί μηχανισμοί έχουν προταθεί ως υπεύθυνοι για την εμφάνιση του εγκεφαλικού οιδήματος ως επιπλοκής της θεραπείας της ΔΚ και της ΥΥ. Ενοχοποιούνται η γρήγορη, με τη θεραπεία, πτώση της ωσμωτικότητας στον εξωκυττάριο σε σχέση με τον ενδοκυττάριο χώρο που έχει ως αποτέλεσμα την είσοδο ύδατος στα εγκεφαλικά κύτταρα, η αυξημένη εγκεφαλική αιμάτωση, η εγκεφαλική ισχαιμία και υποξία, και η δημιουργία διάφορων φλεγμονωδών μεσολαβητών. Ένας άλλος πιθανός παθογενετικός μηχανισμός αφορά την ενεργοποίηση στη ΔΚ του συστήματος της διαμεμβρανικής μεταφοράς Νa+/Η+. Τα υψηλά επίπεδα Η+ επιτρέπουν τη μεγαλύτερη είσοδο Νa+ ενδοκυττάρια προκαλώντας έτσι την είσοδο περισσότερου ύδατος στα κύτταρα. Επίσης, τα κετονικά σώματα φαίνεται ότι επηρεάζουν τόσο την ακεραιότητα όσο και τη διαπερατότητα των αγγείων συντελώντας έτσι στην ανάπτυξη του οιδήματος (95, 96).
Παρόλο που διάφορες μελέτες υποδηλώνουν ότι η χορήγηση με την έναρξη της θεραπείας μεγάλων ποσοτήτων ινσουλίνης καθώς και η ταχεία διόρθωση της αφυδάτωσης με τη χρησιμοποίηση υπότονων διαλυμάτων οδηγούν σε αύξηση του κινδύνου εμφάνισης εγκεφαλικού οιδήματος, μία μεγάλη καλά σχεδιασμένη μελέτη δεν αναγνώρισε το ρυθμό χορήγησης των υγρών ή της ινσουλίνης ως παράγοντα κινδύνου εμφάνισης του εγκεφαλικού οιδήματος (97).
Παρά τα αντικρουόμενα δεδομένα των μελετών, σύμφωνα με τις κατευθυντήριες οδηγίες της ADA (2009) για την αποφυγή ανάπτυξης εγκεφαλικού οιδήματος συστήνεται να γίνεται: α) Σταδιακή διόρθωση της υπερώσμωσης με σταδιακή αποκατάσταση του ύδατος και του Νa+. Ο συνήθης ρυθμός χορήγησης των υγρών πρέπει να είναι τα 10 – 15 ml/kg ΒΣ/ώρα και ο μέγιστος ρυθμός < 50 mL/kg ΒΣ/ώρα τις πρώτες ώρες. Ως μέγιστος ρυθμός μείωσης της ωσμωτικότητας του πλάσματος θεωρούνται τα 3 mosmol/Kg ΒΣ/ώρα. β) Αποφυγή της ταχείας μείωσης των επιπέδων της γλυκόζης και προσθήκη διαλύματος γλυκόζης στα χορηγούμενα διαλύματα υγρών όταν τα επίπεδα της γλυκόζης προσεγγίζουν τα 200 mg/dl στη ΔΚ ή τα 250 – 300 mg/dl στην ΥΥ. Τα επίπεδα γλυκόζης θα πρέπει να διατηρούνται γύρω στα 250 – 300 mg/dl μέχρι να βελτιωθεί η υπερωσμωτικότητα και το επίπεδο συνείδησης του ασθενούς. γ) η χορήγηση μανιτόλης και η εφαρμογή μηχανικού αερισμού μπορεί να βοηθήσουν στην αντιμετώπιση του εγκεφαλικού οιδήματος (6).
11.5. Μη καρδιογενές πνευμονικό οίδημα
Η υποξαιμία και σπάνια το μη καρδιογενές πνευμονικό οίδημα ή σύνδρομο αναπνευστικής δυσχέρειας των ενηλίκων (ARDS) μπορεί να αποτελέσουν επίσης επιπλοκές της θεραπείας της ΔΚ (98). Όπως και στο εγκεφαλικό οίδημα, στην εμφάνισή τους προδιαθέτει η ταχεία χορήγηση μεγάλης ποσότητας υγρών που προκαλεί μείωση της ενδαγγειακής ωσμωτικής πίεσης με αποτέλεσμα την αύξηση της συγκέντρωσης ύδατος και μείωση της διατασιμότητας του πνεύμονα. Αυξημένο κίνδυνο ανάπτυξης πνευμονικού οιδήματος φαίνεται να έχουν οι ασθενείς με ΔΚ οι οποίοι παρουσιάζουν αυξημένη αρτηριο – κυψελιδική διαφορά όπως αυτή υπολογίζεται με τα αέρια του αίματος ή μουσικούς και μη μουσικούς ήχους στην κλινική εξέταση κατά την ακρόαση.
11.6. Θρομβοεμβολικά επεισόδια
Τόσο στη ΔΚ όσο και στην ΥΥ έχουν βρεθεί αυξημένα επίπεδα φλεγμονωδών κυτταροκινών όπως του Tumor Necrosis Factor – alpha (TNF – α), των ιντερλευκινών (IL) – 1B, IL – 6, και IL – 8, πηκτικών παραγόντων όπως του αναστολέα του ενεργοποιητή του πλασμινογόνου – 1 (PAI – 1) και της C – αντιδρώσας πρωτεΐνης (CRP) καθώς και δεικτών υπεροξείδωσης των λιπιδίων (99). Η θεραπεία με ινσουλίνη και η διόρθωση της υπεργλυκαιμίας ομαλοποιούν τα επίπεδα των παραγόντων αυτών. Η φλεγμονώδης και πηκτική αυτή κατάσταση φαίνεται να είναι υπεύθυνη για την αυξημένη επίπτωση για θρομβώσεις που εμφανίζουν οι ασθενείς με ΔΚ και ΥΥ ενώ συμβάλει επίσης και στην αυξημένη νοσηρότητα και θνητότητα των διαταραχών αυτών. H προφυλακτική χορήγηση ηπαρίνης φαίνεται να είναι ευεργετική στους ασθενείς με ΔΚ ή ΥΥ που δεν παρουσιάζουν διαταραχές πήξεως ή άλλες αντενδείξεις. Σε ασθενείς υψηλού κινδύνου για εμφάνιση θρομβώσεων όπως τα ηλικιωμένα άτομα και ασθενείς που βρίσκονται σε κωματώδη κατάσταση για την αποφυγή εμφάνισης θρομβοεμβολικών επεισοδίων χορηγείται συνήθως ηπαρίνη χαμηλού μοριακού βάρους.
12. Πρόληψη
Κύριοι εκλυτικοί παράγοντες που ευθύνονται για την εμφάνιση της ΔΚ και ΥΥ είναι οι λοιμώξεις, η ανεπαρκής θεραπεία με ινσουλίνη καθώς και η μη συμμόρφωση των ασθενών στη θεραπεία. Για την αποφυγή της ΔΚ και της ΥΥ απαιτείται να υπάρχει σωστή εκπαίδευση, τόσο των ίδιων των ασθενών όσο και των μελών της οικογένειάς τους, συχνή επικοινωνία των ασθενών με το ιατρικό και νοσηλευτικό προσωπικό καθώς και η εύκολη πρόσβαση των ασθενών σε φορείς ιατρικής περίθαλψης. Είναι επίσης σημαντικό να υπάρχει κατάλληλη και συνεχιζόμενη εκπαίδευση του εξειδικευμένου ιατρικού και λοιπού προσωπικού που είναι υπεύθυνο για την παρακολούθηση των διαβητικών ασθενών. Οι διαβητικοί ασθενείς θα πρέπει να γνωρίζουν ότι σε κάθε περίπτωση ασθένειας θα πρέπει αυξάνουν τη δόση της ινσουλίνης, να τροποποιούν τη διατροφή τους με λήψη άφθονων υγρών και δίαιτας πλούσιας σε υδατάνθρακες και νάτριο και για προβαίνουν σε συχνές μετρήσεις του σακχάρου τριχοειδικού αίματος ή ακόμη και των κετονών αίματος ή ούρων. Η ινσουλίνη δεν θα πρέπει να διακόπτεται και θα πρέπει να αναζητείται έγκαιρα ιατρική βοήθεια. Ο συχνός αυτοέλεγχος, η σωστή γλυκαιμική ρύθμιση καθώς και η τακτική ιατρική παρακολούθηση συνθέτουν τον ακρογωνιαίο λίθο για της πρόληψης και της αποφυγής τόσο της ΔΚ όσο και της ΥΥ.
13. Συμπεράσματα
Η ΔΚ και η ΥΥ αποτελούν δύο επείγουσες και συχνά επικίνδυνες για τη ζωή καταστάσεις, οι οποίες απαιτούν έγκαιρη διάγνωση και πολύπλευρη αντιμετώπιση. Στις μέρες μας, λόγω της πληρέστερης κατανόησης των παθογενετικών μηχανισμών και της έγκαιρης θεραπευτικής παρέμβασης, η πρόγνωση τόσο της ΔΚ όσο και της ΥΥ είναι καλύτερη σε σχέση με το παρελθόν. Απαιτείται όμως πάντοτε να υπάρχει άμεση κλινική εκτίμηση και σωστή χορήγηση υγρών, ινσουλίνης και ηλεκτρολυτών, ενώ είναι επίσης απαραίτητη η συνεχής κλινική και εργαστηριακή παρακολούθηση του ασθενούς και η ανάλογη τροποποίηση του εφαρμοζόμενου θεραπευτικού σχήματος. Η πρόληψη και των δύο καταστάσεων είναι εφικτή αφενός με την επίτευξη σωστής γλυκαιμικής ρύθμισης και αφετέρου με την τακτική παρακολούθηση και εκπαίδευση των ασθενών με σακχαρώδη διαβήτη.
Βιβλιογραφία
1. Wyckoff J Abrahamson MJ. Diabetic Ketoacidosis and Hyperosmolar Hyperglycemic state. In Joslin’s Diabetes Mellitus. (14th ed) Edited by Kahn CR, King GL, Moses AC, Weir GC, Jacobson AM, Smith RJ 2004; 888 – 899.
2. Wachtel TJ, Tetu – Mouradjian LM, Goldman DL, Ellis SE, O’Sullivan PS. Hyperosmolarity and acidosis in diabetes mellitus: a three – year experience in Rhode Island. J Gen Intern Med 1991; 6:495 – 502.
3. Kitabchi AE, Umpierrez GE, Murphy MB, Kreisberg RA. Hyperglycemic crises in adult patients with diabetes: a consensus statement from the American Diabetes Association. Diabetes Care 2006; 29:2739 – 2748.
4. Kitabchi AE, Umpierrez GE, Fisher JN, Murphy MB, Stentz FB. Thirty years of personal experience in hyperglycemic crises: diabetic ketoacidosis and hyperglycemic hyperosmolar state. J Clin Endocrinol Metab 2008; 93:1541 – 1552.
5. Steenkamp DW, Alexanian SM, McDonnell ME. Adult hyperglycemic crisis: a review and perspective. Curr Diab Rep 2013; 13:130 – 137.
6. Kitabchi AE, Umpierrez GE, Miles JM, Fisher JN. Hyperglycemic crises in adult patients with diabetes. Diabetes Care 2009; 32:1335 – 1343.
7. Kitabchi AE, Nyenwe EA. Hyperglycemic crises in adult patients with diabetes mellitus. In Oxford Textbook of Endocrinology and Diabetes (2ed) Edited by Wass JAH, Stewart PM, Amiel SA, Davies MJ. 2011; 1874 – 1888.
8. Umpierrez GE, Smiley D, Kitabchi AE. Narrative review: ketosis – prone type 2 diabetes mellitus. Ann Intern Med 2006; 144:350 – 357.
9. Balasubramanyam A, Nalini R, Hampe CS, Maldonado M. Syndromes of ketosis – prone diabetes mellitus. Endocr Rev 2008; 29:292 – 302.
10. Johnson DD, Palumbo PJ, Chu CP. Diabetic ketoacidosis in a community – based population.Mayo Clin Proc 1980; 55:83 – 88.
11. Faich GA, Fishbein HA, Ellis SE. The epidemiology of diabetic acidosis: a population – based study. Am J Epidemiol 1983; 117:551 – 558.
12. Henriksen OM, Røder ME, Prahl JB, Svendsen OL. Diabetic ketoacidosis in Denmark Incidence and mortality estimated from public health registries. Diabetes Res Clin Pract 2007; 76:51 – 56.
13. National hospital discharge survey http://www.cdc.gov/diabetes/statistics/hospitalization_national.htm (Accessed on December 28, 2013)
14. Kitabchi AE, Umpierrez GE, Murphy MB, Barrett EJ, Kreisberg RA, Malone JI, Wall BM. Management of hyperglycemic crises in patients with diabetes. Diabetes Care 2001; 24:131 – 153.
15. National hospital discharge survey http://www.cdc.gov/diabetes/statistics/complications _national.htm (Accessed on December 28, 2013)
16. Wang J, Williams DE, Narayan KM, Geiss LS. Declining death rates from hyperglycemic crisis among adults with diabetes, US, 1985 – 2002. Diabetes Care 2006; 29:2018 – 2022.
17. Chen HF, Wang CY, Lee HY, See TT, Chen MH, Jiang JY, et al. Short – term case fatality rate and associated factors among inpatients with diabetic ketoacidosis and hyperglycemic hyperosmolar state: a hospital – based analysis over a 15 – year period.Intern Med 2010; 49:729 – 737.
18. Wolfsdorf J, Craig ME, Daneman D, Dunger D, Edge J, Lee W, et al. Diabetic ketoacidosis in children and adolescents with diabetes. Pediatr Diabetes 2009; Suppl 12:118 – 133.
19. Rosenbloom AL. Hyperglycemic hyperosmolar state: an emerging pediatric problem. J Pediatr 2010; 156:180 – 184.
20. Malone ML, Gennis V, Goodwin JS. Characteristics of diabetic ketoacidosis in older versus younger adults. J Am Geriatr Soc. 1992; 40:1100 – 1104.
21. Wachtel TJ, Silliman RA, Lamberton P. Prognostic factors in the diabetic hyperosmolar state. J Am Geriatr Soc 1987; 35:737 – 741.
22. Polonsky WH, Anderson BJ, Lohrer PA, Aponte JE, Jacobson AM, Cole CF. Insulin omission in women with IDDM. Diabetes Care 1994; 17:1178 – 1185.
23. Randall L, Begovic J, Hudson M, Smiley D, Peng L, Pitre N, et al. Recurrent diabetic ketoacidosis in inner – city minority patients: behavioral, socioeconomic, and psychosocial factors. Diabetes Care 2011; 34:1891 – 1896.
24. Peden NR, Braaten JT, McKendry JB. Diabetic ketoacidosis during long – term treatment with continuous subcutaneous insulin infusion. Diabetes Care 1984; 7:1 – 5.
25. Weissberg – Benchell J, Antisdel – Lomaglio J, Seshadri R. Insulin pump therapy: a meta – analysis. Diabetes Care 2003; 26:1079 – 1087.
26. Nyenwe EA, Loganathan RS, Blum S, Ezuteh DO, Erani DM, Wan JY, et al. Active use of cocaine: an independent risk factor for recurrent diabetic ketoacidosis in a city hospital. Endocr Pract 2007; 13:22 – 29.
27. Katz JR, Edwards R, Khan M, Conway GS. Acromegaly presenting with diabetic ketoacidosis. Postgrad Med J 1996; 72:682 – 683.
28. Gooch BR. Cushing’s syndrome manifesting as pseudo – central hypothyroidism and hyperosmolar diabetic coma. Endocr Pract 2002; 8:119 – 123.
29. Bridgman JF, Pett S. Simultaneous presentation of thyrotoxic crisis and diabetic ketoacidosis. Postgrad Med J 1980; 56:354 – 355.
30. Isotani H, Fujimura Y, Furukawa K, Morita K. Diabetic ketoacidosis associated with the pheochromocytoma of youth. Diabetes Res Clin Pract 1996; 34: 57 – 60.
31. Chupin M, Charbonnel B, Chupin F. C – peptide blood levels in keto – acidosis and in hyperosmolar non – ketotic diabetic coma. Acta Diabetol Lat 1981; 18:123 – 128.
32. Zierler KL, Rabinowitz D. Effect of very small concentrations of insulin on forearm metabolism. Persistence of its action on potassium and free fatty acids without its effect on glucose. J Clin Invest 1964; 43:950 – 962.
33. Unger RH, Orci L. Glucagon and the A cell: physiology and pathophysiology (first two parts). N Engl J Med 1981; 304:1518 – 1524.
34. Barnes AJ, Bloom SR, Goerge K, Alberti GM, Smythe P, Alford FP, et al. Ketoacidosis in pancreatectomized man. N Engl J Med 1977; 296:1250 – 1253.
35. Kitabchi AE, Nyenwe EA Hyperglycemic crises in diabetes mellitus: diabetic ketoacidosis and hyperglycemic hyperosmolar state. Endocrinol Metab Clin North Am 2006; 35:725 – 751.
36. Miles JM, Rizza RA, Haymond MW, Gerich JE. Effects of acute insulin deficiency on glucose and ketone body turnover in man: evidence for the primacy of overproduction of glucose and ketone bodies in the genesis of diabetic ketoacidosis. Diabetes 1980; 29:926 – 930.
37. Exton JH. Mechanisms of hormonal regulation of hepatic glucose metabolism. Diabetes Metab Rev 1987; 3:163 – 183.
38. Meyer C, Stumvoll M, Nadkarni V, Dostou J, Mitrakou A, Gerich J. Abnormal renal and hepatic glucose metabolism in type 2 diabetes mellitus. J Clin Invest 1998; 102:619 – 624.
39. Taborsky GJ Jr. The physiology of glucagon. J Diabetes Sci Technol. 2010; 4:1338 – 1344.
40. Carlson MG, Snead WL, Campbell PJ. Regulation of free fatty acid metabolism by glucagon. J Clin Endocrinol Metab 1993; 77:11 – 15.
41. Nurjhan N, Consoli A, Gerich J. Increased lipolysis and its consequences on gluconeogenesis in non – insulin – dependent diabetes mellitus. J Clin Invest 1992; 89:169 – 175.
42. McGarry JD, Woeltje KF, Kuwajima M, Foster DW. Regulation of ketogenesis and the renaissance of carnitine palmitoyltransferase. Diabetes Metab Rev. 1989; 5:271 – 284.
43. Laffel L. Ketone bodies: a review of physiology, pathophysiology and application of monitoring to diabetes. Diabetes Metab Res Rev 1999; 15:412 – 426.
44. Chiasson JL, Aris – Jilwan N, Bélanger R, Bertrand S, Beauregard H, Ekoé JM, Fournier H, Havrankova J. Diagnosis and treatment of diabetic ketoacidosis and the hyperglycemic hyperosmolar state. CMAJ. 2003; 168:859 – 866.
45. Umpierrez G, Freire AX. Abdominal pain in patients with hyperglycemic crises. J Crit Care 2002; 17:63 – 67.
46. Guisado R, Arieff AI. Neurologic manifestations of diabetic comas: correlation with biochemical alterations in the brain. Metabolism 1975; 24:665 – 79.
47. Lorber D. Nonketotic hypertonicity in diabetes mellitus. Med Clin North Am 1995; 79:39 – 52.
48. Daugirdas JT, Kronfol NO, Tzamaloukas AH, Ing TS. Hyperosmolar coma: cellular dehydration and the serum sodium concentration. Ann Intern Med 1989; 110:855 – 857.
49. Nyenwe EA, Razavi LN, Kitabchi AE, Khan AN, Wan JY Acidosis: the prime determinant of depressed sensorium in diabetic ketoacidosis. Diabetes Care 2010; 33:1837 – 1839.
50. Tzamaloukas AH, Ing TS, Siamopoulos KC, Raj DS, Elisaf MS, Rohrscheib M, et al. Pathophysiology and management of fluid and electrolyte disturbances in patients on chronic dialysis with severe hyperglycemia. Semin Dial 2008; 21:431 – 439.
51. Popli S, Sun Y, Tang HL, Kjellstrand CM, Tzamaloukas AH, Ing TS. Acidosis and coma in adult diabetic maintenance dialysis patients with extreme hyperglycemia. Int Urol Nephrol 2013; 45:1687 – 1692.
52. Chico M, Levine SN, Lewis DF. Normoglycemic diabetic ketoacidosis in pregnancy. J Perinatol 2008; 28:310 – 312.
53. Csako G, Elin RJ. Unrecognized false – positive ketones from drugs containing free – sulfhydryl group(s) JAMA 1993; 269:1634.
54. Meas T, Taboulet P, Sobngwi E, Gautier JF. Is capillary ketone determination useful in clinical practice? In which circumstances? Diabetes Metab 2005; 31:299 – 303.
55. Arora S, Henderson SO, Long T, Menchine M. Diagnostic accuracy of point – of – care testing for diabetic ketoacidosis at emergency – department triage: {beta} – hydroxybutyrate versus the urine dipstick. Diabetes Care 2011; 34:852 – 854.
56. Kelly AM, McAlpine R, Kyle E. Venous pH can safely replace arterial pH in the initial evaluation of patients in the emergency department. Emerg Med J 2001; 18:340 – 342.
57. Adrogué HJ, Wilson H, Boyd AE 3rd, Suki WN, Eknoyan G. Plasma acid – base patterns in diabetic ketoacidosis. N Engl J Med 1982; 307:1603 – 1610.
58. Adrogué HJ, Eknoyan G, Suki WK. Diabetic ketoacidosis: role of the kidney in the acid – base homeostasis re – evaluated. Kidney Int 1984; 25:591 – 598.
59. Owen OE, Licht JH, Sapir DG. Renal function and effects of partial rehydration during diabetic ketoacidosis. Diabetes 1981; 30:510 – 518.
60. Hillier TA, Abbott RD, Barrett EJ. Hyponatremia: evaluating the correction factor for hyperglycemia. Am J Med. 1999; 106:399 – 403.
61. Weisberg LS. Pseudohyponatremia: a reappraisal. Am J Med 1989; 86:315 – 318.
62. Liamis G, Gianoutsos C, Elisaf MS. Hyperosmolar nonketotic syndrome with hypernatremia: how can we monitor treatment? Diabetes Metab 2000; 26:403 – 405.
63. Adrogué HJ, Lederer ED, Suki WN, Eknoyan G. Determinants of plasma potassium levels in diabetic ketoacidosis. Medicine (Baltimore) 1986; 65:163 – 172.
64. Uribarri J, Oh MS, Carroll HJ. Hyperkalemia in diabetes mellitus. J Diabet Complications 1990; 4:3 – 7.
65. Kebler R, McDonald FD, Cadnapaphornchai P. Dynamic changes in serum phosphorus levels in diabetic ketoacidosis. Am J Med 1985; 79:571 – 576.
66. Yadav D, Nair S, Norkus EP, Pitchumoni CS. Nonspecific hyperamylasemia and hyperlipasemia in diabetic ketoacidosis: incidence and correlation with biochemical abnormalities. Am J Gastroenterol 2000; 95:3123 – 3128.
67. Karavanaki K, Kakleas K, Georga S, Bartzeliotou A, Mavropoulos G, Tsouvalas M, et al. Plasma high sensitivity C – reactive protein and its relationship with cytokine levels in children with newly diagnosed type 1 diabetes and ketoacidosis. Clin Biochem 2012; 45:1383 – 1388.
68. Slovis CM, Mork VG, Slovis RJ, Bain RP. Diabetic ketoacidosis and infection: leukocyte count and differential as early predictors of serious infection. Am J Emerg Med 1987; 5:1 – 5.
69. Weidman SW, Ragland JB, Fisher JN Jr, Kitabchi AE, Sabesin SM. Effects of insulin on plasma lipoproteins in diabetic ketoacidosis: evidence for a change in high density lipoprotein composition during treatment. J Lipid Res 1982; 23:171 – 182.
70. Wrenn KD, Slovis CM, Minion GE, Rutkowski R. The syndrome of alcoholic ketoacidosis. Am J Med 1991; 91:119 – 128.
71. Hara JS, Rahbar AJ, Jeffres MN, Izuora KE. Impact of a hyperglycemic crises protocol. Endocr Pract 2013; 19:953 – 962.
72. Waldhäusl W, Kleinberger G, Korn A, Dudczak R, Bratusch – Marrain P, Nowotny P. Severe hyperglycemia: effects of rehydration on endocrine derangements and blood glucose concentration. Diabetes 1979; 28:577 – 584.
73. Hillman K. Fluid resuscitation in diabetic emergencies – a reappraisal. Intensive Care Med 1987; 13:4 – 8.
74. Kitabchi AE, Ayyagari V, Guerra SM. The efficacy of low – dose versus conventional therapy of insulin for treatment of diabetic ketoacidosis. Ann Intern Med 1976; 84:633 – 638.
75. Padilla AJ, Loeb JN. “Low – dose” versus “high – dose” insulin regimens in the management of uncontrolled diabetes. A survey. Am J Med 1977; 63:843 – 848.
76. Brown PM, Tompkins CV, Juul S, Sönksen PH. Mechanism of action of insulin in diabetic patients: a dose – related effect on glucose production and utilisation. Br Med J 1978; 1:1239 – 1242.
77. Rosenthal NR, Barrett EJ. An assessment of insulin action in hyperosmolar hyperglycemic nonketotic diabetic patients. J Clin Endocrinol Metab 1985; 60:607 – 610.
78. Kitabchi AE, Murphy MB, Spencer J, Matteri R, Karas J. Is a priming dose of insulin necessary in a low – dose insulin protocol for the treatment of diabetic ketoacidosis? Diabetes Care 2008; 31:2081 – 2085.
79. Goyal N, Miller JB, Sankey SS, Mossallam U. Utility of initial bolus insulin in the treatment of diabetic ketoacidosis. J Emerg Med 2010; 38:422 – 427.
80. Page MM, Alberti KG, Greenwood R, Gumaa KA, Hockaday TD, Lowy C, et al. Treatment of diabetic coma with continuous low – dose infusion of insulin. Br Med J 1974; 2:687 – 690.
81. Luzi L, Barrett EJ, Groop LC, Ferrannini E, DeFronzo RA. Metabolic effects of low – dose insulin therapy on glucose metabolism in diabetic ketoacidosis. Diabetes. 1988; 37:1470 – 1477.
82. Umpierrez GE, Latif K, Stoever J, Cuervo R, Park L, Freire AX, et al. Efficacy of subcutaneous insulin lispro versus continuous intravenous regular insulin for the treatment of patients with diabetic ketoacidosis. Am J Med 2004; 117: 291 – 296.
83. Umpierrez GE, Cuervo R, Karabell A, Latif K, Freire AX, Kitabchi AE. Treatment of diabetic ketoacidosis with subcutaneous insulin aspart. Diabetes Care 2004; 27:1873 – 1878.
84. Umpierrez GE, Jones S, Smiley D, Mulligan P, Keyler T, Temponi A, et al. Insulin analogs versus human insulin in the treatment of patients with diabetic ketoacidosis: a randomized controlled trial. Diabetes Care 2009; 32:1164 – 1169.
85. Unwin RJ, Luft FC, Shirley DG.Pathophysiology and management of hypokalemia: a clinical perspective. Nat Rev Nephrol. 2011; 7:75 – 84.
86. Beigelman PM. Potassium in severe diabetic ketoacidosis. Am J Med. 1973; 54: 419 – 420.
87. Viallon A, Zeni F, Lafond P, Venet C, Tardy B, Page Y, Bertrand JC. Does bicarbonate therapy improve the management of severe diabetic ketoacidosis? Crit Care Med 1999; 27: 2690 – 2693.
88. Latif KA, Freire AX, Kitabchi AE, Umpierrez GE, Qureshi N. The use of alkali therapy in severe diabetic ketoacidosis. Diabetes Care 2002; 25: 2113 – 2114.
89. Amanzadeh J, Reilly RF Jr. Hypophosphatemia: an evidence – based approach to its clinical consequences and management. Nat Clin Pract Nephrol. 2006; 2:136 – 148
90. Wilson HK, Keuer SP, Lea AS, Boyd AE 3rd, Eknoyan G. Phosphate therapy in diabetic ketoacidosis. Arch Intern Med 1982; 142:517 – 520.
91. Fisher JN, Kitabchi AE. A randomized study of phosphate therapy in the treatment of diabetic ketoacidosis. J Clin Endocrinol Metab 1983; 57:177 – 1780.
92. Oh MS, Carroll HJ, Goldstein DA, Fein IA. Hyperchloremic acidosis during the recovery phase of diabetic ketosis. Ann Intern Med 1978; 89:925 – 927.
93. Wolfsdorf J, Glaser N, Sperling MA; American Diabetes Association. Diabetic ketoacidosis in infants, children, and adolescents: A consensus statement from the American Diabetes Association. Diabetes Care 2006; 29:1150 – 1159.
94. Marcin JP, Glaser N, Barnett P, McCaslin I, Nelson D, Trainor J, et al; American Academy of Pediatrics. The Pediatric Emergency Medicine Collaborative Research Commitee. Factors associated with adverse outcomes in children with diabetic ketoacidosis – related cerebral edema. J Pediatr 2002; 141:793 – 797.
95. Silver SM, Clark EC, Schroeder BM, Sterns RH. Pathogenesis of cerebral edema after treatment of diabetic ketoacidosis. Kidney Int 1997; 51:1237 – 1244.
96. Glaser NS, Wootton – Gorges SL, Marcin JP, Buonocore MH, Dicarlo J, Neely EK, et al. Mechanism of cerebral edema in children with diabetic ketoacidosis. J Pediatr 2004; 145:164 – 171.
97. Glaser N, Barnett P, McCaslin I, Nelson D, Trainor J, Louie J, et al. Pediatric Emergency Medicine Collaborative Research Committee of the American Academy of Pediatrics. Risk factors for cerebral edema in children with diabetic ketoacidosis. The Pediatric Emergency Medicine Collaborative Research Committee of the American Academy of Pediatrics. N Engl J Med 2001; 344:264 – 269.
98. Brun – Buisson CJ, Bonnet F, Bergeret S, Lemaire F, Rapin M. Recurrent high – permeability pulmonary edema associated with diabetic ketoacidosis. Crit Care Med 1985; 13:55 – 56.
99. Stentz FB, Umpierrez GE, Cuervo R, Kitabchi AE. Proinflammatory cytokines, markers of cardiovascular risks, oxidative stress, and lipid peroxidation in patients with hyperglycemic crises. Diabetes 2004; 53:2079 – 2086.
Created: April 27, 2015
Last update: April 27, 2015