Αικατερίνη Μόρτογλου, Αναστάσιος Μόρτογλου
Τομέας Μεταβολισμού Ιατρικού Κέντρου Αθηνών
1. Εισαγωγή
Υπερκορτιζολαιμία ή σύνδρομο Cushing μπορεί να προκληθεί από αύξηση της ενδογενούς παραγωγής κορτικοειδών ή από παρατεταμένη εξωγενή χορήγηση για θεραπευτικούς λόγους.
Αύξηση της ενδογενούς έκκρισης κορτικοειδών έχουμε επί:
- Αδενώματος της υπόφυσης με υπερέκριση ACTH. Πρόκειται για τη Νόσο Cushing.
- Όγκων των επινεφριδίων, μονήρων ή πολλαπλών, ετερόπλευρων ή αμφοτερόπλευρων, καλοήθων συνήθως αλλά και κακοήθων, που εκκρίνουν αυτόνομα κορτικοστεροειδή.
- Παρανεοπλασματικών εκδηλώσεων, συνηθέστερα από όγκους του πνεύμονα και του παγκρέτος που εκκρίνουν αυτόνομα αυξημένα ποσά ACTH.
Μακροχρόνια εξωγενής λήψη κορτικοειδών, συνήθως per os, γίνεται από πάσχοντες από χρόνιες φλεγμονώδεις νόσους όπως η ρευματοειδής αρθρίτις, κολλαγονώσεις όπως ο συστηματικός ερυθηματώδης λύκος, αλλεργικό βρογχικό άσθμα, μετά από μεταμόσχευση οργάνων κτλ. Να σημειωθεί εδώ ότι ακόμα και η παρατεταμένη χρήση ψεκασμών κορτικοειδών για αλλεργικό άσθμα ή δερματικών σκευασμάτων κορτικοειδών μπορεί να προκαλέσουν σύνδρομο Cushing (1).
Παρά το ότι το ενδογενές σύνδρομο Cushing είναι σπάνιο, η υπερκορτιζολαιμία που οφείλεται σε μακροχρόνια θεραπευτική λήψη κορτικοειδών μπορεί να φτάσει ακόμα και στο 2.5% του γενικού πληθυσμού (2), γεγονός που την καθιστά σημαντικό πρόβλημα δημόσιας υγείας. Και βέβαια, στις παραπάνω περιπτώσεις υπερκορτιζολαιμίας θα πρέπει να προσθέσουμε και αυτές που οφείλονται σε χρόνιο στρες και τις περιπτώσεις απλής παχυσαρκίας όπου, όπως είναι γνωστό, έχουμε αυξημένη εξωαδενική παραγωγή δραστικής κορτιζόλης (εικόνα 1).
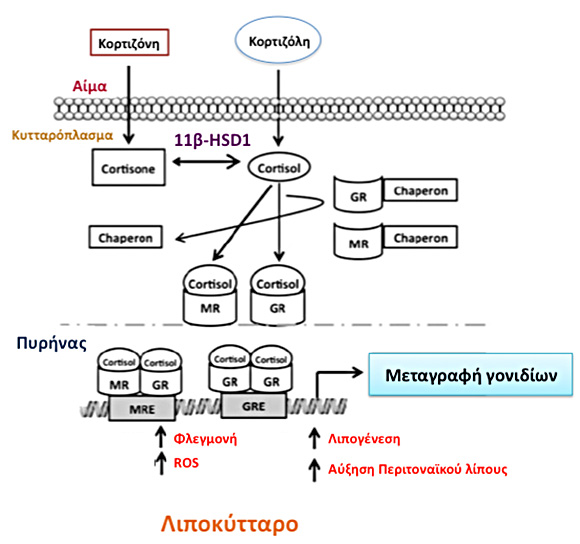
Εικόνα 1. Η 11β-Υδροξυστεροειδική αφυδρογονάση τύπου 1 (11β-HSD1) είναι το κύριο ένζυμο μετατροπής της κορτιζόνης σε κορτιζόλη στο λιπώδη ιστό. Η 11β-HSD1 καταλύει κυρίως τη μετατροπή της κορτιζόνης σε κορτιζόλη, ωστόσο και η αντίστροφη αντίδραση μπορεί να συμβεί. Τα αυξημένα επίπεδα κορτιζόλης συνδέονται με τον υποδοχέα γλυκοκορτικοειδών (GR) αλλά και αλατοκτοκορτικοειδών (MR). Στον πυρήνα (διακεκομμένη γκρι γραμμή), τα σύμπλοκα μπορεί να συνδεθούν με συγγενή στοιχεία απόκρισης (MRE ή GRE) στις ρυθμιστικές αλληλουχίες των γονιδίων-στόχων και να έχουμε την έναρξη της μεταγραφής του γονιδίου. Με το μηχανισμό αυτό, η ενεργοποίηση της 11β-HSD1 επάγει την αύξηση του περιτοναϊκού λίπους, την αύξηση των ελεύθερων ριζών οξογόνου (ROS) και τη χρόνια φλεγμονώδη αντίδραση στις λιπαποθήκες.
Οι επιπτώσεις της υπερκορτιζολαιμίας από τη μακροχρόνια λήψη στεροειδών per os είναι πολλές και σημαντικές (πίνακας 1), οι περισσότερες όμως από αυτές μπορεί να αμβλυνθούν, ακόμα και να ανασταλλεί η εμφάνισή τους με ορθές διαιτητικές πρακτικές. Οι επιπτώσεις του πίνακα 1 που εκφέρονται με κόκκινους χαρακτήρες είναι αυτές που οι διαιτητικές παρεμβάσεις μπορεί να έχουν ευνοϊκές απιδράσεις.
| Πίνακας 1.Επιπτώσεις υπερκορτιζολαιμίας. | |
| Επίπτωση | Συχνότητα % |
| Κοιλιακή παχυσαρκία | 79-97 |
| Πανσεληνοειδές προσωπείο | 50-94 |
| Διαταραχή μεταβολισμού γλυκόζης | 39-90 |
| Υπέρταση | 74-87 |
| Μεταβολές θυμικού | 31-86 |
| Αυτόματες εκχυμώσεις | 23-84 |
| Υπερτρίχωση στις γυναίκες | 64-81 |
| Διαταραχές περιόδου | 55-80 |
| Ακμή | 26-80 |
| Λιπαρότητα δέρματος | 55-80 |
| Ερυθρές ραβδώσεις | 51-71 |
| Οιδήματα | 28-60 |
| Οστεοπόρωση – Κατάγματα | 40-50 |
| Νεφρολιθίαση | 15-19 |
| Μυοπάθεια | 20-40 |
| Λοιμώξεις | 30 |
| Γαστρεντερικές διαταραχές | 21 |
Η πιο σημαντική όμως επίπτωση της υπερκορτιζολαιμίας είναι η αύξηση της θνησιμότητας στο 4πλάσιο και αυτή οφείλεται κύρια στην παχυσαρκία και στην ινσουλινοαντίσταση (3).
Σημαντική είναι και η γνώση πως, το μεταβολικό σύνδρομο που προκαλεί η μακροχρόνια έκθεση σε κορτικοστεροειδή δεν υποχωρεί μετά τη διακοπή τους. Έχει βρεθεί ότι μετά την υποχώρηση της υπερκορτιζολαιμίας δεν αποκαθίστανται τα επίπεδα της CRP, της μεγαλομοριακής αντιπονεκτίνης (4), αλλά ούτε και οι λοιποί μείζονες παράγοντες του μεταβολικού συνδρόμου (5). Τα παραπάνω λοιπόν κάνουν περισσότερο επιβεβλημένες τις διατροφικές παρεμβάσεις στα άτομα με μακροχρόνια έκθεση σε κορτικοστεροειδή, ενδογενή ή εξωγενή.
Στην εξωγενή χορήγηση κορτικοειδών σημαντικό είναι:
- H δόση και η διάρκεια της θεραπείας να είναι οι μικρότερες δυνατές.
- Η χορήγηση βραχείας διάρκειας κορτικοειδών (υδροκορτιζόνη) είναι προτιμότερη για θεραπεία υποκατάστασης σε περιπτώσεις χρόνιας επινεφριδικής ανεπάρκειας.
- Είναι σκόπιμο, όπου βέβαια υπάρχει ένδειξη, να χρησιμοποιούνται παράλληλα και άλλα ανοσοκατασταλτικά φάρμακα (π.χ cyclophosphamide, methotrexate, cyclosporine) ώστε η δόση των κορτικοειδών να είναι η μικρότερη δυνατή.
- Η χρήση ισχυρών και μακράς δράσης κορτικοειδών (π.χ δεξαμεθαζόνη) αντενδείκνυται για μακροχρόνια θεραπεία και θα πρέπει να χρησιμοποιούνται μόνο σε οξείες καταστάσεις.
- Η χορήγηση μεγάλων εφ’άπαξ δόσεων κορτικοειδών θα πρέπει να γίνεται μόνο σε περιπτώσεις όπου υπάρχει απόλυτη ένδειξη.
- Φαίνεται ότι το καταλληλότερο κορτικοειδές για μακροχρόνια θεραπεία και είναι σκόπιμο αυτό να χρησιμοποιείται, είναι η πρεδνιζολόνη.
2. Γλυκοκορτικοειδή, ινσουλινοαντίσταση και υπεργλυκαιμία
Η αντίσταση στην ινσουλίνη, ο συνδετικός κρίκος μεταξύ της παχυσαρκίας, του μεταβολικού συνδρόμου και του διαβήτη 2, ορίζεται ως η μειωμένη ικανότητα της ινσουλίνης να ελέγχει την ποσοτική πρόσληψη των μακροστοιχείων από τα όργανα-στόχους. Στο λιπώδη ιστό, η ινσουλίνη δεν αναστέλει τη λιπόλυση και δεν αυξάνει την πρόσληψη γλυκόζης, στο ήπαρ δεν μπορεί να αναστείλει τη νεογλυκογένεση και τη γλυκογονόλυση και στους μύες αδυνατεί να επάγει την πρόσληψη της γλυκόζης.
Μια σημαντική λειτουργία των γλυκοκορτικοειδών είναι να ελευθερώνουν από τους ιστούς θρεπτικά συστατικά (γλυκόζη, αμινοξέα και λιπαρά οξέα) ώστε να υπάρχει επαρκής διαθεσιμότητα για μιτοχονδριακή οξείδωση σε συνθήκες έκτακτης ανάγκης. Έτσι, έχουμε αύξηση του καταβολισμού των μυϊκών πρωτεϊνών, αύξηση της λιπόλυσης και της ηπατική νεογλυκογένεσης με ταυτόχρονη μείωση της χρησιμοποίησης της γλυκόζης από τους ιστούς με τελικό αποτέλεσμα την υπεργλυκαιμία.
Χρόνια έκθεση σε μεγάλες δόσεις γλυκοκορτικοειδών μεταβάλλει τη σύσταση του σώματος και την κατανομή του λίπους με αποτέλεσμα την κεντρική κατανομή του λίπους, αύξηση του περιτοναϊκού λίπους, μείωση της δράση της ινσουλίνης και με τελικό αποτέλεσμα την υπεργλυκαιμία και τη δυσλιπιδαιμία.
Τα γλυκοκορτικοειδή λοιπόν είναι η συχνότερη αιτία φαρμακευτικού διαβήτη.Οι δυσμενείς τους επιπτώσεις στο μεταβολισμό της γλυκόζης εμφανίζονται λίγες μόνο ώρες από την άναρξη της θεραπείας με κορτικοειδή και φαίνεται ότι είναι δοσο-εξαρτώμενες.Περισσότερο επηρεάζεται η μεταγευματική γλυκόζη παρά η γλυκόζης νηστείας (6) και μετά τη διακοπή τους επανέρχεται στο φυσιολογικό πρώτα η γλυκόζη νηστείας και αργότερα η μεταγευματική (7).
2.1. Θεραπεία της εκ των κορτικοειδών υπεργλυκαιμίας
Όλοι οι ασθενείς που πρόκειται να λάβουν μακροχρόνια θεραπεία με κορτοκοειδή θα πρέπει να είναι ενήμεροι για τα σημεία και συμπτώματα της υπεργλυκαιμίας, ώστε να μπορούν να διαγνώσουν το πρόβλημα έγκαιρα.
Ο γλυκαιμικός στόχος για ασθενείς με σακχαρώδη διαβήτη εκ κορτικοειδών πρέπει να εξατομικεύεται, αλλά για τους περισσότερους ασθενείς, η γλυκόζη νηστείας θα πρέπει να είναι 72-126mg/dl και 2 ώρες μετά γεύμα 90-180 mg/dl (8).
Θεραπευτικά, η πρώτη προσέγγιση θα πρέπει να είναι η τροποποίηση της διατροφικής συμπεριφοράς και η αύξηση της σωματικής δραστηριότητας.
Αν παρ’ όλα αυτά η υπεργλυκαιμία επιμένει, θα πρέπει να χορηγούνται per os αντιδιαβητικά αν τα επίπεδα γλυκόζης είναι έως 270 mg/dl ή ινσουλίνη επί επιπέδων γλυκόζης >270 mg/dl. Η μετφορμίνη μπορεί να χορηγηθεί και στις δύο περιπτώσεις, εφ΄όσον δεν υπάρχουν αντενδείξεις για τη λήψη της.
Αναφορικά με τη διαιτητική θεραπεία, μπορεί κανείς να ανατρέξει στο ανάλογο κεφάλαιο του βιβλίου. Μερικές βασικές αρχές που θα πρέπει να ακολουθηθούν είναι:
- Ισοθερμιδική δίαιτα σε νορμοβαρή άτομα ή ήπια ολιθερμιδική σε υπέρβαρα άτομα. Η μείωση του σωματικού λίπους, εκτός των άλλων, μειώνει και τη δραστηριότητα της 11β-HSD1
- Ποσοστό υδατανθράκων 45-50% της συνολικής ενεργειακή πρόσληψης, αλλά με υδατάνθρακες χαμηλού γλυχαιμικού δείκτη.
- Αύξηση φυτικών ινών
- Πλήρης αποφυγή προστιθέμενων ενεργεικών σακχάρων
- Αποφυγή καφέ, μπορεί όμως να γίνεται χρήση καφέ χωρίς καφείνη
- Αποφυγή αλκοολούχων ποτών, τα οποία, αν και αυξάνουν την ευαισθησία στην ινσουλίνη, αυξάνουν σημαντικά τη δράση των κορτικοειδών.
- Η σωματική δραστηριότητα θα πρέπει να περιλαμβάνει και ασκήσεις αντίστασεις ώστε να αποφύγουμε τον εκ των κορτικοειδών μυϊκό καταβολισμό.
3. Γλυκοκορτικοειδή και μυοσκελετικό σύστημα
Χρόνια λήψη κορτικοειδών επηρεάζει το μυοσκελετικό σύστημα σε πολλά επίπεδα:
- Προκαλεί οστεοπόρωση
- Μπορεί να προκαλέσει οστεονέκρωση
- Προκαλεί άλλοτε άλλου βαθμού μυοπάθεια
Αναφορικά με την οστεοπόρωση, τα κορτικοειδή καταστέλουν το σχηματισμό οστού και αυτό είναι το κύριο αίτιο πρόκλησης ή επιδείνωσης της οστεοπόρωσης. Αυξάνουν το ρυθμό απορρόφησης οστού από τους οστεοκλάστες (9). Το πρόβλημα εμφανίζεται μόλις μετά τους πρώτους 3 μήνες θεραπείας με κορτικοειδή, κορυφώνεται στους 6 μήνες και μετά έχουμε μια αργή αλλά προοδευτική απώλεια οστού. Το πρόβλημα επιδεινούται και από την καταστολή των γονάδων και του άξονα GH – IGF1.
Αναφέρεται αυξημένος κίνδυνος σπονδυλικών καταγμάτων, τα οποία είναι συχνά ασυμπτωματικά και μη-σπονδυλικών καταγμάτων ακόμα και με δόσεις πρεδνιζολόνης 2.5 mg/ημέρα, ιδίως σε ηλικιωμένους ασθενείς, οι οποίοι και λόγω της εκ των κορτικοειδών μυοπάθειας έχουν συχνότερες πτώσεις (10,11).
Τα κορτικοστεροειδή ασκούν άμεση καταβολική δράση στους σκελετικούς μύες λόγω ατροφίας των τύπου 2 μυικών ινών. Η μυϊκή αδυναμία εμφανίζεται συνήθως μετά από αρκετές εβδομάδες από την έναρξη της θεραπείας και εντοπίζεται κυρίως στις εγγύς και μεγάλες μυικές ομάδες με αποτέλεσμα τη σχετική δυσκολία έγερσης.
Η διάγνωση τίθεται κυρίως από την κλινική εικόνα, γιατί ο έλεγχος των ενζύμων ή ο ηλεκτροφυσιολογικός έλεγχος δίνουν σπάνια διαγνωστικά ευρήματα (12).
Αν και δεν υπάρχει ειδική θεραπεία για τη μυοπάθεια, καλό θα είναι να αποφεύγονται παράγοντες που μπορεί να την επιδεινώσουν, όπως π.χ η ακινητοποίηση ή η θεραπεία με στατίνες. Πάντως, πρόσφατη πειραματική μελέτη σε άτομα που προκλήθηκε μυοπάθεια από μακροχρόνια ακινητοποίηση, φαίνεται ότι υπήρξε σημαντικό θεραπευτικό αποτέλεσμα όταν χορηγήθηκαν 16 γρ/ημ. διαλύμματος αμινοξέων (Ιστιδίνη, Ισολευκίνη, Λευκίνη, Λυσίνη, Μεθιονίνη, Φαινυλαλανίνη, Θρεονίνη, Βαλίνη, Τρυπτοφάνη, Γλυκίνη) (13). Αυτό σημαίνει ότι διατροφή πλούσια σε λευκώματα υψηλής βιολογικής αξίας, ασκεί πιθανώς προληπτική ή/και θεραπευτική επίδραση.
Η θεραπεία με κορτικοειδή είναι η συχνότερη αιτία μη τραυματικής οστεονέκρωσης και μπορεί να συμβεί ακόμη και χωρίς οστεοπόρωση. Αν και ο κίνδυνος φαίνεται να αυξάνει με μεγάλες δόσεις και μακροχρόνια θεραπεία, εν τούτοις μπορεί να συμβεί ακόμα και με μικρές δόσεις ή μετά βραχείας διάρκειας θεραπεία.
Αν και η άσηπτη νέκρωση μπορεί να προσβάλλει πολλαπλές αρθρώσεις, οι συχνότερες είναι οι αρθρώσεις του ισχίου και του γόνατος (14, 15).
3.1. Πρόληψη/ θεραπεία της εκ των κορτικοειδών οστεοπόρωσης
Πριν από τη χορήγηση κορτικοειδών θα πρέπει να γίνεται προσδιορισμός της οστικής πυκνότητας (BMD) καθώς και μέτρηση του ύψους και θα πρέπει να επαναλαμβάνονται σε ετήσια βάση. Πάντως, οστεοπορωτικό κάταγμα λόγω των κορτικοειδών μπορεί να συμβεί ακόμα και πριν από τη μείωση της BMD σε παθαλογικά όρια (16).
Για το λόγο αυτό, εκτός από τον προσδιορισμό της BMD, θα πρέπει να υπολογίζεται και το FRAX score και με βάσει το στατιστικό κίνδυνο θα πρέπει να λαμβάνονται τα ανάλογα προληπτικά μέτρα.Σε όλους, άσχετα από τον στατιστικό κίνδυνο, τη δόση και τη διάρκεια της θεραπείας θα πρέπει να συστήνεται (17):
- Ημερήσια πρόσληψη ασβεστίου 1200 mg/ημέρα
- Χορήγηση βιταμίνης D3 1000 IU/ημέρα
- Ασκήσεις με βάρη
- Διακοπή καπνίσματος
- Περιορισμός των αλκοολούχων ποτών (λιγότερο από 2 ποτά την ημέρα)
- Γενικές διατροφικές οδηγίες που μπορείτε να βρείτε στο ανάλογο κεφάλαιο
Σε άτομα με χαμηλό και μέτριο στατιστικό κίνδυνο – FRAX score <10% και 10-20% για μεγάλο κάταγμα στα επόμενα 10 χρόνια: Χορήγηση διφοσφωνικών αν η διάρκεια της θεραπείας είναι μεγαλύτερη από 3 μήνες και η δόση της πρεδνιζολόνης είναι ≥ 7,5 mg/ημέρα.
Σε άτομα με μεγάλο στατιστικό κίνδυνο – FRAX score >20% για μεγάλο κάταγμα στα επόμενα 10 χρόνια ή T στη BMD ≤ 2,5: Χορήγηση διφοσφωνικών άσχετα από τη διάρκεια της θεραπείας και τη δόση της πρεδνιζολόνης.
Σε προεμμηνοπαυσικές γυναίκες, σε άνδρες <50 ετών, σε παιδιά καθώς και σε άτομα που κάνουν μακροχρόνια λήψη εισπνεόμενων κορτικοειδών, η αντιμετώπιση θα πρέπει να εξατομικεύεται γιατί δεν υπάρχουν αρκετά στοιχεία γιαυτές τις κατηγορίες πασχόντων (17).
4. Γλυκοκορτικοειδή και αλάτι
Όταν ο γιατρός, άσχετα από την ειδικότητα, συστήσει θεραπεία με κορτικοειδή, συνήθως προσθέτει στο τέλος λακωνικά: ‘κόψτε το αλάτι και τη ζάχαρη’.
Κατά κανόνα, ο μέσος ασθενής διακόπτει την προσθήκη αλατιού, αλλά συνεχίζει να λαμβάνει μεγάλες ποσότητες ‘κρυμένου’ νατρίου σε διάφορα τρόφιμα και ποτά.Θα πρέπει εδώ να υπενθυμίσουμε ότι τα γλυκοκορτικοειδή έχουν μεγάλη συγγένεια με τον υποδοχέα αλατοκορτικοειδών (εικόνα 1) και ότι κάποια γλυκοκορτικοειδή που χρησιμοποιούνται μακροχρόνια (υδροκορτιζόνη, πρεδνιζολόνη) έχουν ισχυρότερη αλατοκορτικοειδική δράση. Αυτό έχει ως αποτέλεσμα την κατακράτηση νερού, την αύξηση του όγκου του κυκλοφορούντος αίματος, την αύξηση του σωματικού βάρους, την πρόκληση ή επιδείνωση προϋπάρχουσας υπέρτασης, επιδείνωση της ινσουλινοαντίστασης και συχνά υποκαλιαιμία.
Ευτυχώς, όλα τα παραπάνω αποκαθίστανται πλήρως 2 βδομάδες μετά τη διακοπή των κορτικοειδών.
Να θυμίσουμε εδώ ότι τοαλάτιείναιμίαχημικήένωση πουαποτελείταιαπόΝάτριο (Να) καιΧλώριο (Cl). 5 γρ. αλατιούισοδυναμούνμε 1 κουταλάκιτουγλυκού. Ένακουταλάκιτουγλυκούμαγειρικόαλάτι περιέχει περίπου 2.300 mgνατρίου.
Το νάτριο είναι ένα θρεπτικό συστατικό απαραίτητο για τη διατήρηση του όγκου του πλάσματος, της οξεοβασικής ισορροπίας, της μετάδοσης των νευρικών ερεθισμάτων, και της κανονικής λειτουργίας των κυττάρων ενώ το ελάχιστο επίπεδο που απαιτείται ως ημερήσια πρόσληψη είναι μόλις 200-500 mg (18). Αν και η σύσταση για υγιείς ενήλικες είναι να καταναλώνουν < 5 γραμμάρια αλάτι την ημέρα, συμπεριλαμβανομένου και αυτού που περιέχεται στα τρόφιμα, η συνήθης μέση κατανάλωση κυμαίνεται απο 9-12 γρ,/ημ. Βεβαίως, τα άτομα σε θεραπεία με κορτικοειδή θα πρέπει να παίρνουν το λιγότερο δυνατό, αφού ότι και να φάει κανείς θα υπερκαλύψει τις ελάχιστες ημερήσιες ανάγκες.
Περίπου το 80% της μέσης κατανάλωσης χωριούχου νατρίου είναι ‘κρυμμένη’ σε τροφές όπως το ψωμί, το τυρί, οι ελιές, τα έτοιμα φαγητά, η μαργαρίνη, τα δημητριακά, οι κονσέρβες, οι πίκλες, οι σούπες, το παστό κρέας και ψάρι, όλα τα αλαντικά, η σόδα και το φαγητό έξω από το σπίτι, άσχετα αν είναι ταχυφαγία ή βραδυφαγία. Το αποτέλεσμα είναι η πρόσληψη νατρίου να είναι σχεδόν πάντα πολύ μεγαλύτερη της επιτρεπτής (19).
Ενδεικτικά να αναφέρουμε για 100 γρ. ψωμιού ημερησίως, που είναι μια σχετικά μικρή κατανάλωση, η πρόσληψη σε νάτριο είναι:
- Άσπρο ψωμί 296 mg
- Κριθαρένιο ψωμί 274 mg
- Ψωμί σικάλεως 350 mg
- Ψωμί ολικής άλεσης 397 mg
Η περιεκτικότητα σε νάτριο των συνήθων τυριών φαίνεται στον πίνακα 2.Επίσης, ενδεικτικά να αναφέρουμε την περιεκτικότητα σε Να σε μερικά ακόμα τρόφιμα:
- Ταραμοσαλάτα 480 mg Na/100 γρ.
- Τζατζίκι 204 mg Na/100 γρ.
- Τυρόπιτα με σφολιάτα 571 mg Na/100 γρ.
- Σπανακόπιτα 1050 mg Na/100 γρ.
- Κύβοι βοδινού 10300 mg Na/100 γρ.
- Σκόνη κακάο 950 mg Na/100 γρ.
- Κορν Φλέικς 1160 mg Na/100 γρ.
- Βούτυρο αλατισμένο 870 mg Na/100 γρ.
- Μπισκότα Κρημ-κράκερς 610 mg Na/100 γρ.
Μερικές χρήσιμες συμβουλές για περιορισμό της πρόσληψης νατρίου:
- Προτιμάτε σπιτικά φαγητά όπου μπορείτε να ελέγξετε την ποσότητα αλατιού και μη χρησιμοποιείτε καθόλου αλάτι. Αντί για αλάτι χρησιμοποιείστε μυρωδικά όπως άνηθο, ρίγανη, δεντρολίβανο, βασιλικό, δυόσμο, δάφνη, θυμάρι, αποξηραμένο σέλινο ή ξύδι, λεμόνι, σκόρδο, κρεμμύδι, για την ενίσχυση της γεύσης των φαγητών. Μπορείτε να χρησιμοποιείτε και υποκατάστατα αλατιού (χλωριούχο κάλιο ή γαλακτικό κάλιο) που δίνει σχετικά παρόμοια γεύση με το επιτραπέζιο αλάτι. Προσοχή στα άτομα που παίρνουν ταυτόχρονα φάρμακα της κατηγορίας των α-ΜΕΑ, ανταγωνιστές της αλδοστερόνης και διουρητικά που κατακρατούν κάλιο.
- Φροντίστε να προμηθεύεστε ψωμί χωρίς αλάτι και αν αυτό είναι δύσκολο μπορείτε να ζυμώσετε μια ικανή ποσότητα μόνοι σας. Φυλάξτε το στην κατάψυξη και καθημερινά βγάζετε την ποσότητα που θα καταναλώσετε.
- Μη βάζετε την αλατιέρα στο τραπέζι.
- Επιλέξτε τρόφιμα χωρίς προστιθέμενο αλάτι ή με πολύ χαμηλή περιεκτικότητα σε νάτριο. Συμβουλευτείτε τις ετικέτες της συσκευασίας των τροφίμων, συγκρίνετε την περιεκτικότητα των τροφίμων σε νάτριο και αγοράστε αυτά με τη χαμηλότερη περιεκτικότητα. Οι ετικέτες της συσκευασίας των τροφίμων μας ενημερώνουν για την περιεκτικότητα τους τόσο σε νάτριο (πίνακας διαθρεπτικής επισήμανσης), όσο και σε αλάτι (στη λίστα των συστατικών). Σύμφωνα με τις νομοθετικές διατάξεις του ΕΦΕΤ (ΕΦΕΤ 2010) ανάλογα με την περιεκτικότητά του σε νάτριο/αλάτι ένα τρόφιμο χαρακτηρίζετα ιως:
- Υψηλό σε νάτριο/αλάτι: ότανστα 100 γραμ. περιέχει περισσότεροαπό 0,6 γραμ. νατρίου (ή 1,5 γραμ. αλατιού).
- Χαμηλό σε νάτριο/αλάτι: ότανστα 100 γραμ. περιέχει 0,1 γραμ. νατρίου (ή 0,3 γραμ. αλατιού) ήλιγότερο.
- Μέτριο σε νάτριο/αλάτι: ότανστα 100 γραμ. περιέχει 0,3 γραμ. έως 0,6 γραμ. νατρίου
- Πολύ χαμηλό σε νάτριο/αλάτι: ότανστα 100 γραμ. ή 100 ml περιέχειόχι περισσότεροαπό 0,04 γραμ. νατρίουήισοδύναμη ποσότητααλατιού.
- Ελεύθερο νατρίου/αλατιού: ότανστα 100 γραμ. ή 100 ml περιέχειόχι περισσότεροαπό 0,005 γραμ. νατρίουήισοδύναμη ποσότητααλατιούανά 100 γραμ. ή ανά 100 ml
- Όταν τρώτε εκτός σπιτιού ζητείστε να μην αλατίσουν το φαγητό σας.
- Προτιμήστε την κατανάλωση τυριών με χαμηλή περιεκτικότητα σε αλάτι (πίνακας 2)
- Πριν την κατανάλωση, τοποθετείστε τα λευκά τυριά που έχουν υψηλή περιεκτικότητα σε αλάτι (π.χ. φέτα) καθώς και τις ελιές μέσα σε νερό, ώστε να απομακρυνθεί το πλεονάζον αλάτι (ξαρμύρισμα).
- Αποφύγετετηνκατανάλωσηλαχανικώνσεάλμη (τουρσί).
- Περιορίστετηνκατανάλωσηκονσερβοποιημένων, επεξεργασμένωνκαι παστώνκρεάτων, αλλαντικώνκαιψαριών, γιατί περιέχουν πολύαλάτι.
- Αποφύγετε τις έτοιμες σάλτσες, τη σάλτσα σόγιας και τη μουστάρδα.
- Επειδή πρόβλημα είναι το νάτριο και όχι το χλωριούχο νάτριο, αποφύγετε και τος τροφές που έχουν σόδα (διτανθρακικό νάτριο) και γλουταμινικό μονονάτριο.
- Καταναλώνετε μόνοανάλατουςξηρούςκαρπούς.
- Η κατανάλωση νερού, τρεχούμενου ή εμφιαλωμένου, θα πρέπει να περιορίζεται σε αυτά που η περιεκτικότητα σε νάτριο είναι <10 mg/λίτρο.
- Και βέβαια μη ξεχνάτε: Η αυξημένη πρόσληψη καλίου προλαβαίνει την πιθανή εκ των κορτικοειδών υποκαλιαιμία και ταυτόχρονα ανταγωνίζεται τη δράση του νατρίου.
| Πίνακας 2. Περιεκτικότητα σε νάτριο συνήθων τυριών που καταναλώνονται από τον Ελληνικό πληθυσμό. | |
| Τρόφιμο | Νάτριο(mg/100g) |
| Ανθότυρο Κρήτης | 116 |
| Μυζήθρα Θεσσαλίας | 179 |
| Μυζήθρα Κρήτης | 191 |
| Ανθότυρο Μακεδονίας | 224 |
| Ανθότυρο Ηπείρου | 251 |
| Έμενταλ | 260 |
| Μανούρι Μακεδονίας | 281 |
| Cottage cheese (Κότατζ τσιζ) | 330 |
| Μυζήθρα Μακεδονίας | 409 |
| Κεφαλογραβιέρα Πελοπονήσου | 425 |
| Γραβιέρα Νάξου | 461 |
| Γραβιέρα Κρήτης | 473 |
| Κασέρι Νήσων Αιγαίου | 485 |
| Κασέρι Μακεδονίας | 487 |
| Φέτα Θεσσαλίας | 493 |
| Κασέρι Ηπείρου | 511 |
| Φέτα Πελοπονήσου | 556 |
| Φέτα Μακεδονίας | 558 |
| Τελεμές Θεσσαλίας | 575 |
| Φέτα Στερεάς Ελλάδας | 596 |
| Μοτσαρέλα από πλήρες γάλα | 627 |
| Μετσοβόνε | 636 |
| Καλαθάκι Λήμνου | 645 |
| Τελεμές Θράκης | 652 |
| Κεφαλογραβιέρα Στερεάς Ελλάδας | 754 |
| Τσένταρ | 819 |
| Γκούντ) | 819 |
| Κεφαλογραβιέρα Ηπείρου | 863 |
| Κεφαλοτύρι Ηπείρου | 868 |
| Ένταμ | 965 |
| Χαλούμι | 1100 |
| Παρμεζάνα | 1602 |
| Ροκφόρ | 1809 |
Πίνακες σύνθεσης ελληνικών τροφίμων- Καφάτος & Χασαπίδου, 2013, http://nutrition.med.uoc.gr/greektables/Main/main.htm
Βιβλιογραφία
1. Tempark T, Phatarakijnirund V, Chatproedprai S. et al. Exogenous Cushing’s syndrome due to topical corticosteroid application: case report and review literature. Endocrine 2010;38:328-34.
2. Van Staa TP, Leufkens HG, Abenhaim L, et al. Use of oral corticosteroids in the United Kingdom. QJM 2000;93:105-11.
3. Etxabe J, Vazquez JA. Morbidity and mortality in Cushing’s disease: an epidemiological approach. Clin Endocrinol (Oxf) 1994;40:479-84.
4. Geer EB, Shen W, Strohmayer E, et al. Body composition and cardiovascular risk markers after remission of Cushing’s disease: a prospective study using whole-body MRI. J Clin Endocrinol Metab 2012;97:1702-11.
5. Calao A, Pivonello R, Spiezia S, et al. Persistence of increased cardiovascular risk in patients with Cushing’s disease after five years of successful cure. J Clin Endocrinol Metab. 1999;84:2664-72.
6. Burt MG, Roberts GW, Aguilar-Loza NR, Frith P, Stranks SN. Continuous monitoring of circadian glycemic patterns in patients receiving prednisolone for COPD. J Clin Endocrinol Metab 2011;96:1789-96.
7. Lansang MC, Hustak LK. Glucocorticoid-induced diabetes and adrenal suppression: How to detect and manage them. Cleve Clin J Med 2011;78:748-56.
8. Canadian Diabetes Association Clinical Practice Guidelines Expert Committee: Canadian Diabetes Association 2013 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes. 2013;37(Suppl 1):S1–212.
9. Canalis E, Mazziotti G, Giustina A, Bilezikian JP. Glucocorticoid-induced osteoporosis: Pathophysiology and therapy. Osteoporos Int 2007;18:1319-28.
10. Shah SK, Gecys GT. Prednisone-Induced Osteoporosis: An Overlooked and Undertreated Adverse Effect. J Am Osteopath Assoc 2006;106:653-7.
11. Angeli A, Guglielmi G, Dovio A, Capelli G, de Feo D, Giannini S, et al. High prevalence of asymptomatic vertebral fractures in post-menopausal women receiving chronic glucocorticoid therapy: A cross-sectional outpatient study. Bone 2006;39:253–9.
12. Perrot S, Le Jeunne C. Steroid-induced myopathy. Presse Med 2012;41:422–6.
13. Fitts R, Romatowski J, Peters J et al. The deleterious effects of bed rest on human skeletal muscle fibers are exacerbated by hypercortisolemia and ameliorated by dietarysupplementation. Am J Physiol – Cell Physiol 2007;293:C313-C320.
14. Weinstein RS. Glucocorticoid-induced osteonecrosis. Endocrine 2012;41:183-90.
15. Caramaschi P, Biasi D, Dal Forno I, Adami S. Osteonecrosis in systemic lupus erythematosus: An early, frequent, and not always symptomatic complication. Autoim Dis 2012; 2012:725249.
16. Kanis JA, Johansson H, Oden A, Johnell O, de Laet C, Melton LJ, III, et al. A meta-analysis of prior corticosteroid use and fracture risk. J Bone Miner Res. 2004;19:893-9.
17. Grossman JM, Gordon R, Ranganath VK, Deal C, Caplan L, Chen W, et al. American College of Rheumatology 2010 recommendations for the prevention and treatment of glucocorticoid-induced osteoporosis. Arthritis Care Res (Hoboken) 2010;62:1515-26.
18. Holbrook JT, Patterson KY, Bodner JE, Douglas LW et al. Sodium and potassium intake and balance in adults consuming self-selected diets. Am J Clin Nutr 1984;40:786-93.
19. Cobiac L, Vos T, Veerman J. Cost-effectiveness of interventions to reduce dietary salt intake. Heart 2010; 96:1920-1925.
Created: September 18, 2016
Last update: September 18, 2016