Αθανάσιος Παπανικολάου
Συντονιστής Δ/ντής Γ.Ν.Θ. «Γ. Γεννηματάς – Άγιος Δημήτριος»
Η πρώτη εφαρμογή της ανοιχτής βιοψίας των όρχεων στη διερεύνηση του υπογόνιμου άνδρα έγινε από τους Charny και Hotchkiss στη δεκαετία του ‘40 (1). Ήδη από τις αρχικές αυτές αναφορές, το σκεπτικό του διαχωρισμού της απόφραξης των εκφορητικών οδών του σπέρματος από την εσωτερική δυσλειτουργία των όρχεων και της συγγενούς από την επίκτητη βλάβη της σπερματογένεσης είχε εκφραστεί ξεκάθαρα. Οι αρχικές περιγραφές των χειρουργικών τεχνικών, της μονιμοποίησης των ιστών και της ταξινόμησης των ιστολογικών ευρημάτων είναι αισθητά παρόμοιες με τη σημερινή πρακτική.
Η σωστή αξιολόγηση της βιοψίας των όρχεων προϋποθέτει συσχέτιση των ιστολογικών ευρημάτων με τα λοιπά κλινικοεργαστηριακά ευρήματα του υπογόνιμου άνδρα. Ποτέ μια βιοψία δεν θα πρέπει να αξιολογείται χωρίς την γνώση τουλάχιστον του σπερμοδιαγράμματος και την FSH του ορού. Η προϋπόθεση αυτή είναι σημαντική, όχι διότι θα αλλάξει την αξιολόγηση της βιοψίας, αλλά διότι θα προσφέρει σημαντικές πληροφορίες ερμηνείας των ιστολογικών αλλοιώσεων που ενδεχόμενα θα βοηθήσουν σε προγνωστικές αξιολογήσεις.
1. Ενδείξεις της βιοψίας των όρχεων
Ενώ παλαιότερα διενεργείτο βιοψία των όρχεων σε όλους τους υπογόνιμους άνδρες με αζωοσπερμία και ολιγοασθενοτερατοσπερμία (ΟΤΑ) σήμερα οι ενδείξεις έχουν σημαντικά περιοριστεί. Σύμφωνα με την Επιτροπή Ανδρικής Υπογονιμότητας της Αμερικανικής Ουρολογικής Εταιρείας και την Επιτροπή της Αμερικανικής Εταιρείας Αναπαραγωγικής Ιατρικής η βιοψία των όρχεων έχει ένδειξη στις ακόλουθες μόνο περιπτώσεις: (α) σε άνδρες με αζωοσπερμία και φυσιολογική FSH για να γίνει διαχωρισμός της αποφρακτικής από την μη αποφρακτική αζωοσπερμία και (β) σε άνδρες με χαμηλό όγκο σπέρματος και ψηλαφητό σπερματικό πόρο για την επιβεβαίωση απόφραξης στην άπω εκφορητική οδό του σπέρματος (2).
2. Τεχνικές της βιοψίας των όρχεων
Η λήψη υλικού από τον όρχι για ιστολογική εξέταση μπορεί να γίνει εφαρμόζοντας δύο τεχνικές : 2.1. Την ανοιχτή βιοψία, και 2.2. Τη βιοψία με μεγάλου διαμετρήματος βελόνη. Θα πρέπει να διευκρινίσουμε εδώ ότι οι τεχνικές που κάνουν χρήση της βιοψίας με βελόνη χρησιμοποιούν ποικίλου διαμετρήματος βελόνες από 18 έως 23 G. Οι μέθοδοι με μεγάλου διαμετρήματος βελόνες (G 18-19, Vim Silverman, Tru Cut, Biopty gyn) επιτυγχάνουν τη λήψη ορχικών ιστοτεμαχίων ενώ στις μεθόδους με μικρή διάμετρο βελόνης ( G 23, Fine Needle Aspiration FNA) το υλικό είναι κυτταρολογικό.
2.1. Ανοιχτή βιοψία
Η βιοψία των όρχεων με τομή δια μαχαιριδίου (ανοιχτή βιοψία, Standar Open Surgical Biopsi) έχει επικρατήσει από την εποχή της πρώτης της εφαρμογής πειραματικά από τον Engle το 1939 και κλινικά από τους Carny το 1940 και Hotchkiss το1942.
Η μέθοδος είναι απλή, μπορεί να εφαρμοσθεί με τοπική νάρκωση που δεν απαιτεί νοσοκομειακή περίθαλψη ή υπό γενική αναισθησία, όταν στον ίδιο χειρουργικό χρόνο έχει προγραμματιστεί να γίνει ευρεία διερεύνηση του οσχέου με ενδεχόμενη μικροχειρουργική αποκατάσταση παθολογικών ευρημάτων.
Υπάρχουν δύο τεχνικές διατομής του οσχέου: α) η « τεχνική του παραθύρου» και β) η μέση διατομή. Η πρώτη εφαρμόζεται, όταν έχει προγραμματιστεί μόνο βιοψία του όρχι και η δεύτερη όταν απαιτείται διερεύνηση και του οσχέου. Στην «τεχνική του παραθύρου» γίνεται μία εγκάρσια διατομή του οσχέου, μήκους 1-2 εκ. και μία μικρότερη της κάψας των όρχεων, μήκους 0,5 εκ. Η μέση διατομή του οσχέου επιτρέπει την προσπέλαση για λήψη βιοψίας και από τους δύο όρχεις (3).
Χρειάζεται μεγάλη προσοχή στην τεχνική λήψεως του δείγματος με σκοπό την αποφυγή και της παραμικρής κάκωσης στον ευαίσθητο ορχικό ιστό. Καλό είναι το δείγμα χωρίς τη χρησιμοποίηση λαβίδας να τοποθετείται αμέσως στο μονιμοποιητικό υγρό. Η χρησιμοποίηση λαβίδας προκαλεί αποδιοργάνωση και απόπτωση «disorganization and sloughing» του σπερματικού επιθηλίου στον αυλό των σπερματικών σωληναρίων.
Μολονότι η ετερόπλευρη βιοψία στις περισσότερες των περιπτώσεων είναι επαρκής, η αμφοτερόπλευρη σε μερικές περιπτώσεις είναι τελείως απαραίτητη (4). Αμφοτερόπλευρη βιοψία διενεργείται στις περιπτώσεις με υπόνοια ασύμμετρης ορχικής βλάβης. Τέτοιες υπόνοιες εγείρουν οι ανισομεγέθεις όρχεις, η μη ψηλάφηση του ενός των σπερματικών πόρων ή η σκλήρυνση της επιδιδυμίδας. Όταν επιλέγεται, ανεξαρτήτως των ενδείξεων η ετερόπλευρη βιοψία θα πρέπει πάντα να επιλέγεται ο υγιέστερος μακροσκοπικά όρχις. Σε μία αναδρομική μελέτη 192 υπογόνιμων ανδρών παρατηρήθηκε ότι η βιοψία του ενός μόνο των όρχεων είναι επαρκής να δώσει ικανοποιητικές πληροφορίες για τον τύπο και το βαθμό της ορχικής βλάβης, όταν μία αμφοτερόπλευρη συμμετρική βλάβη είχε προηγηθεί (5).
Ο όγκος του δείγματος πρέπει να είναι ανάλογος με τους στόχους της διερεύνησης. Η ιστολογική εξέταση συνήθως απαιτεί όγκο ορχικού ιστού 0,2-0,5 κ.εκ. από κάθε όρχι, ποσότητα ικανή για την εκτίμηση 100-120 τουλάχιστον σπερματικών σωληναρίων. Τα ιστοτεμάχια για το ηλεκτρονικό μικροσκόπιο πρέπει να έχουν μέγεθος 1 κ.χιλ. και να τοποθετούνται σε κρύο διάλυμα γλουταραλδεύδης 4%.
Η επιλογή του μονιμοποιητικού υγρού παίζει σημαντικό ρόλο στη σωστή εκτίμηση και ερμηνεία της ιστολογίας του ορχικού ιστού. Η χρησιμοποίηση φορμόλης 10%, που είναι το σύνηθες μονιμοποιητικό υγρό, είναι καταστρεπτική για τον ορχικό ιστό και εκμηδενίζει την προσπάθεια της όλης διαδικασίας. Η φορμόλη δε διατηρεί τις λεπτομέρειες της μορφολογίας των πυρήνων, που είναι πολύ σημαντικές στην αναγνώριση των διάφορων κυττάρων του σπερματικού επιθηλίου. Κατάλληλα μονιμοποιητικά υγρά είναι το διάλυμα Buin, το διάλυμα Stives,το διάλυμα Cleland, όπως επίσης και το διάλυμα Heller. Η πείρα με αυτά απέδειξε ότι προκαλούν τη μικρότερη δυνατή ρίκνωση του κυττάρου και επιτρέπουν τη διατήρηση και κατάδειξη μορφολογικών στοιχείων του πυρήνα που είναι απαραίτητα για την πλήρη ιστολογική μελέτη. Σήμερα το μονιμοποιητικό επιλογής είναι το διάλυμα Bouin (3).
Η περαιτέρω διαδικασία απαιτεί ανάλογη φροντίδα σε όλες τις βαθμίδες επεξεργασίας του ιστού- αφυδάτωση, έγκλιση, διατομή, χρώσεις- αποφεύγοντας κάθε τεχνική πλημμέλεια που μπορεί να αποδειχθεί τελείως επιβαρυντική στην έκφραση των αποτελεσμάτων μας.
Οι χρώσεις που χρησιμοποιούνται συνήθως είναι α) αιματοξυλίνη-εωσίνη β) Masson-τροχρωμική γ) P.A.S. και δ) Verhoef elastica-Van Gieson. Η πρώτη είναι απαραίτητη για κάθε ιστολογική εξέταση. Η Masson καταδεικνύει τις κυτταρικές μεμβράνες, την περισωληνώδη ίνωση, τα κύτταρα Leydig και τους κρυστάλλους Reinke. Η P.A.S. κάνει πιο εμφανή τη βασική μεμβράνη και τα κοκκία γλυκογόνου. Η Verhof elastica χρησιμεύει για την εκτίμηση των ελαστικών ινών του τοιχώματος των σπερματικών σωληναρίων.
Συχνά εκφράζονται φόβοι για τους κινδύνους που μπορεί να έχει η βιοψία των όρχεων ως χειρουργική επέμβαση. Οι πιθανότητες τραυματισμού ή αιματώματος σχεδόν αποκλείονται από τη σωστή τεχνική. Επί 1000 βιοψιών, ο Tillinger αναφέρει δύο δερματίτιδες του όσχεου και ένα ενδοοσχεϊκό αιμάτωμα, χωρίς αυτές να έχουν επίπτωση επί της ποιότητας του σπέρματος. Εξάλλου, η πιθανότητα εκλύσεως αυτοάνοσου μηχανισμού από τον τραυματισμό του ορχικού ιστού δε φαίνεται να είναι συχνό φαινόμενο ( 6)
2.2. Βιοψία με μεγάλου διαμετρήματος βελόνη
Η βιοψία με βελόνη ως μέθοδος διερεύνησης των όρχεων για την παρουσία ή απουσία σπερματοζωαρίων προτάθηκε για πρώτη φορά το 1904. Αργότερα η αμφοτερόπλευρη ανοιχτή βιοψία έγινε η μέθοδος επιλογής στη μελέτη της μορφολογίας και της λειτουργίας των όρχεων. Σήμερα διάφορες μελέτες επαναξιολογούν τα πλεονεκτήματα της διαδερμικής βιοψίας συγκριτικά με την ανοικτή βιοψία. Οι προτείνοντες τη μέθοδο της διαδερμικής βιοψίας υποστηρίζουν ότι μπορεί να εφαρμοσθεί ως πρακτική ιατρείου με ελάχιστο πόνο και ελάχιστες επιπλοκές παρέχοντας σημαντικές πληροφορίες σε επιλεγμένα περιστατικά. Οι τεχνικές που περιγράφηκαν χρησιμοποιούν ποικίλου διαμετρήματος βελόνες από 18 έως 23 G. Οι μέθοδοι με μεγάλου διαμετρήματος βελόνες (G 18-19, Vim Silverman, Tru Cut, Biopty gyn) επιτυγχάνουν τη λήψη ορχικών ιστοτεμαχίων με ικανοποιητικό αριθμό σπερματικών σωληναρίων ( πάνω από 20 ) γεγονός που επιτρέπει την αξιολόγηση των όρχεων με τις συνήθεις ιστολογικές μεθόδους της ανοιχτής βιοψίας. Υστερούν ελάχιστα στην αξιολόγηση των όρχεων συγκριτικά με την ανοιχτή βιοψία, ωστόσο δεν έτυχαν ευρείας κλινικής εφαρμογής, διότι θεωρήθηκαν έντονα τραυματικές ( 7 – 9 ).
3. Ιστολογία του παθολογικού όρχεως
Η εξέταση της βιοψίας των όρχεων αρχικά θα πρέπει να γίνεται με μικρή μεγέθυνση κατά την οποία θα εκτιμάται η ποσότητα του υλικού που διαθέτουμε, η αρχιτεκτονική δομή του ορχικού παρεγχύματος και σε γενικές γραμμές η σχέση του διάμεσου συνδετικού ιστού προς τα σπερματικά σωληνάρια. Στη συνέχεια, με μεγαλύτερες μεγεθύνσεις, θα εκτιμάται: 3.1. Ο διάμεσος συνδετικός ιστός και 3.2. Τα σπερματικά σωληνάρια.
3.1. Αλλοιώσεις του διάμεσου συνδετικού ιστού
Ο όγκος του διάμεσου συνδετικού ιστού αυξάνει γρήγορα σε περιπτώσεις κιρσοκήλης λόγω οιδήματος και πάχυνσης του τοιχώματος των αγγείων (10). Τα διάμεσα κύτταρα αποτελούν μέρος του διάμεσου ιστού και εντοπίζονται στις γωνίες των ορχικών σωληναρίων συμβάλλοντας, κατά προσέγγιση στο 3% της έκτασης της βιοψίας. Υπάρχουν αρκετοί τρόποι αξιολόγησης του αριθμού των διάμεσων κυττάρων(11), ωστόσο ο αριθμός τους δύσκολα μπορεί να συσχετιστεί με τα επίπεδα της τεστοστερόνης στο αίμα. Τα επίπεδα της Τ επηρεάζονται μόνο όταν παρατηρείται σχεδόν πλήρης εξαφάνιση των διάμεσων κυττάρων ή όταν παρουσιάζουν έντονη οζώδη υπερπλασία. Τα διάμεσα κύτταρα συχνά παρουσιάζουν οζώδη υπερπλασία σε παιδιά με σύνδρομο Klinefelter, ενώ ελαττώνονται στους ενήλικες ασθενείς (12). Διάφορα νοσήματα των όρχεων, μεταξύ των οποίων η απλασία του σπερματικού επιθηλίου και η κιρσοκήλη, μπορούν να συνδυασθούν με υπερπλασία των διάμεσων κυττάρων (13). Τα διάμεσα κύτταρα είναι λίγα και εκφυλισμένα, με παρουσία λίγων κυτταροπλασματικών λιποειδών εγκλείστων και λίγων κρυστάλλων του Reinke, στη συστροφή των όρχεων και στην κρυψορχία (14).
3.2. Αλλοιώσεις των σπερματικών σωληναρίων
Οι αλλοιώσεις των σπερματικών σωληναρίων περιλαμβάνουν: 3.2.1.) την σωληναριακή υποπλασία, 3.2.2.) την ελάττωση της διαμέτρου, 3.2.3.) τη πάχυνση του τοιχώματος και 3.2.4.) τις αλλοιώσεις της κυτταρικής σύνθεσης του σπερματικού επιθηλίου
3.2.1. Σωληναριακή υποπλασία
Η σωληναριακή υποπλασία αποτελεί αδυναμία διεύρυνσης του σπερματικού σωληναρίου, μία διαδικασία που φυσιολογικά συνοδεύει την εφηβεία. Τα υποπλαστικά σπερματικά σωληνάρια επενδύονται από σπερμογόνια και από ανώριμα σερτόλια κύτταρα. Αυτό μπορεί να αποτελεί μορφολογική έκφραση του υπογοναδοτρόπου υπογοναδισμού (15).
3.2.2. Ελάττωση της διαμέτρου των σπερματικών σωληναρίων
Η ελάττωση της διαμέτρου των σπερματικών σωληναρίων θα πρέπει να εκτιμάται πάντα, και εάν είναι δυνατόν με ακριβείς μετρήσεις και όχι με γενικούς περιγραφικούς όρους. Στις περισσότερες των περιπτώσεων συνδυάζεται τόσο με ελάττωση του κυτταρικού πληθυσμού του σπερματικού επιθηλίου όσο και με πάχυνση του τοιχώματος του αντίστοιχου σωληναρίου (16). Οι μεγάλες διαφορές στη διάμετρο γειτονικών σπερματικών σωληναρίων υποδηλώνουν εστιακή βλάβη, συχνό εύρημα της ορχικής ατροφίας που ακολουθεί τις ορχίτιδες (17).
3.2.3. Πάχυνση του τοιχώματος των σπερματικών σωληναρίων
Η πάχυνση του τοιχώματος του σπερματικού σωληναρίου εκδηλώνεται είτε με υαλοειδοποίηση της βασικής μεμβράνης είτε με περισωληναριακή ίνωση.
Η υαλοειδοποίηση της βασικής μεμβράνης αποτελεί ομόκεντρη πάχυνση της βασικής μεμβράνης οφειλόμενη σε εναπόθεση υαλίνης. Η αλλοίωση μπορεί να είναι «ελάχιστη» (παρατηρούμενη μόνο με τις ειδικές χρώσεις και συνήθως συνδυάζεται με φυσιολογικό σπερματικό επιθήλιο) έως «πλήρης» (αντικατάσταση του σπερματικού επιθηλίου με πλήρωση του αυλού από το εωσινόφιλο υλικό). Η έντονη διάχυτη υαλοειδοποίηση (σωληναριακή σκλήρυνση) μπορεί να οφείλεται σε ορμονικές ανωμαλίες όπως σε υπεργοναδοτρόπο ή υπογοναδοτρόπο υπογοναναδισμό ή σε εξωγενή χορήγηση οιστρογόνων (3). Οι όρχεις των ενηλίκων σε ένα ποσοστό 60% παρουσιάζουν περιοχές σκλήρυνσης των σωληναρίων, πιθανόν οφειλόμενες σε αρτηριοσκλήρυνση (18). Αυτό το φυσιολογικό εύρημα δεν θα πρέπει να ερμηνευτεί εσφαλμένα σαν εστιακή σωληναριακή σκλήρυνση.
Η περισωληναριακή ίνωση αποτελεί ινώδη πάχυνση του μυοϊνοβλαστικού στρώματος του περισωληνώδη υμένα. Το υλικό που προκαλεί την πάχυνση αποτελείται από κολλαγόνες ίνες και υλικό παρόμοιο με εκείνο της βασικής μεμβράνης. Η πάχυνση πολύ συχνά συνυπάρχει και ακολουθεί τις βλάβες του σπερματικού επιθηλίου. Μεταξύ των παραγόντων που μπορούν να την προκαλέσουν περιλαμβάνονται η κατάχρηση οινοπνεύματος, οι τοξίνες και η φλεγμονή του διάμεσου συνδετικού ιστού. Οι ήπιες αλλοιώσεις μπορεί να συνδυάζονται με χορήγηση οιστρογόνων ή ανδρογόνων ή με κιρσοκήλη (18). Στις προχωρημένες περιπτώσεις μπορεί να παρατηρηθεί σύγκλιση γειτονικών αλλοιώσεων με πλήρη ίνωση του διάμεσου συνδετικού ιστού. Η ταυτόχρονη παρουσία σωληναριακής σκλήρυνσης και ίνωσης του διάμεσου συνδετικού ιστού αποτελεί το τελικό στάδιο της ορχικής ατροφίας (19). Μολονότι η ποιοτική εκτίμηση του βαθμού της ίνωσης είναι γενικά εύκολη από έναν έμπειρο παθολογοανατόμο, τελευταία αναπτύχθηκαν εξειδικευμένες τεχνικές παρατήρησης που επιτρέπουν την αντικειμενική και ποσοτική εκτίμηση αυτού του ευρήματος (20).
3.2.4. Αλλοιώσεις της κυτταρικής σύνθεσης του σπερματικού επιθηλίου
Η κυτταρική σύνθεση του σπερματικού επιθηλίου στον υπογόνιμο άνδρα μπορεί να είναι φυσιολογική 3.2.4.1) φυσιολογική σπερματογένεση ή αλλοιωμένη. Οι αλλοιώσεις της κυτταρικής σύνθεσης μπορούν να ταξινομηθούν, σύμφωνα με την επικρατέστερη μέθοδο ταξινόμησης κατά Levin, στις ακόλουθες ομάδες: 3.2.4.2. Υποσπερματογένεση, 3.2.4.3. Διακοπή της σπερματογένεσης ή ωρίμανσης (maturation arrest), 3.2.4.4. Απλασία του σπερματικού επιθηλίου (germinal cell aplasia or Sertoli cell only syndrome). 3.2.4.5. Απλασία του σπερματικού επιθηλίου και εστιακή σπερματογένεση (germinal cell aplasiα and focal spermatogenesis) και 3.2.4.6. Σωληναριακή και περισωληναριακή σκλήρυνση (όρχις τελικού σταδίου) (23).
Φυσιολογική σπερματογένεση
Όταν σε μια βιοψία όλα τα ορχικά σωληνάρια παρουσιάζουν φυσιολογική σύνθεση των κυττάρων του σπερματικού επιθηλίου η σπερματογένεση χαρακτηρίζεται ως φυσιολογική (Εικόνα 1). Η σύνθεση των κυττάρων του σπερματικού επιθηλίου έχει περιγραφή λεπτομερώς στην κλασσική μελέτη των Heller και Clermont από την δεκαετία του ΄60 (21). Πρακτικής σημασίας είναι η γνώση ότι σε μία εγκάρσια διατομή ορχικού σωληναρίου δε φαίνονται όλα τα στάδια διαφοροποίησης των σπερματικών κυττάρων. Ώριμα σπερματοζωάρια και ώριμες σπερματίδες μπορούν να βρεθούν σε μία ζώνη ενός σπερματικού σωληναρίου, ενώ η γειτονική ζώνη μπορεί να παρουσιάζει ωρίμανση μόνο μέχρι το επίπεδο της πρώιμης σπερματίδης. Αυτό το φυσιολογικό εύρημα δεν θα πρέπει να ερμηνευτεί εσφαλμένα σαν διακοπή της σπερματογένεσης (22).
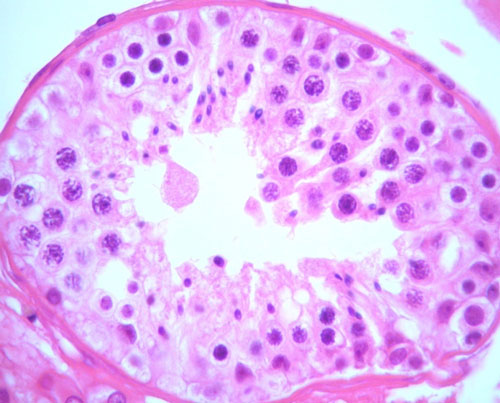
Εικόνα 1. Φυσιολογική σπερματογένεση (Α-Ε 400x). Πηγή: Προσωπικό αρχείο συγγραφέως.
Όταν η βιοψία παρουσιάζει φυσιολογική σπερματογένεση θα πρέπει να γίνεται πάντα συσχέτιση των ιστολογικών ευρημάτων με τα υπόλοιπα κλινικοεργαστηριακά ευρήματα του ασθενούς. Φυσιολογική σπερματογένεση παρουσιάζουν οι υπογόνιμοι άνδρες με απόφραξη των εκφορητικών οδών του σπέρματος ή οι άνδρες με φυσιολογικό αριθμό και χαμηλή κινητικότητα σπερματοζωαρίων στο σπέρμα (23).
Υποσπερματογένεση (υποπλασία του σπερματικού επιθηλίου)
Ως υποσπερματογένεση ορίζεται η συμμετρική ελάττωση όλων των κυττάρων του σπερματικού επιθηλίου. Διαβαθμίζεται σε ελαφρά, μέτρια και έντονη. Η ελαφρά χαρακτηρίζεται από ήπια ελάττωση του αριθμού των κυττάρων του σπερματικού επιθηλίου η οποία γίνεται αντιληπτή σε λίγα μόνο ορχικά σωληνάρια. Η μέτρια χαρακτηρίζεται από εντονότερη ελάττωση των κυττάρων του σπερματικού επιθηλίου και γίνεται αντιληπτή σε μεγάλο αριθμό σπερματικών σωληναρίων (Εικόνα 2). Στην έντονη, έχουμε εκτεταμένη και έντονη ελάττωση των κυττάρων του σπερματικού επιθηλίου που σε μερικές θέσεις μπορεί να προσομοιάζει στην πλήρη απλασία του σπερματικού επιθηλίου. Μερικοί συγγραφείς ωστόσο υποστηρίζουν ότι, σαν όρος υπό την στενή έννοια, δύσκολα θα μπορούσε να χρησιμοποιηθεί δεδομένου ότι η συμμετρική ελάττωση των κυττάρων του σπερματικού επιθηλίου συχνά συνυπάρχει με ανώμαλη ωρίμανση στο ίδιο ορχικό σωληνάριο. Εξαίρεση θα μπορούσαν να αποτελέσουν οι πολύ ήπιες αλλοιώσεις, όπου δεν παρατηρείται συνύπαρξη υποσπερματογένεσης και ανώμαλης ωρίμανσης (3). Συχνά συνυπάρχουν επίσης αλλοιώσεις στο τοίχωμα των ορχικών σωληναρίων και στον διάμεσο συνδετικό ιστό οι οποίες εστιακά μπορούν να εκδηλωθούν και με σωληναριακή σκλήρυνση.

Εικόνα 2. Μέτρια υποσπερματογένεση (Α-Ε 200x). Πηγή: προσωπικό αρχείο συγγραφέως.
Η υποσπερματογένεση δεν αποτελεί αλλοίωση ενός συγκεκριμένου αιτιολογικού παράγοντα. Μεταξύ των άλλων υποσπερματογένεση προκαλεί: α) η υπερβολική έκθεση σε τοξίνες και ζέστη, β) η κιρσοκήλη και γ) ο υποθυρεοειδισμός (23).
Διακοπή σπερματογένεσης ή ωρίμανσης (maturation arrest)
Στην διακοπή της σπερματογένεσης το σπερματικό επιθήλιο παρουσιάζει απότομη διακοπή της φυσιολογικής διαδοχής των κυττάρων της σπερματογένεσης σε κάποιο στάδιο αυτής, συνήθως στο στάδιο του σπερμογονίου ή του σπερμοκυττάρου πρώτης τάξεως (Εικόνα 3) και σπανιότερα στο στάδιο της στρογγύλης σπερματίδης (24). Τα δύο πρώτα επίπεδα διακοπής της σπερματογένεσης αποδίδονται και με τον όρο πρώιμη (early) και το τρίτο με τον όρο όψιμη (late). Ο όρος «ατελής διακοπή της σπερματογένεσης» αποτελεί σημείο διχογνωμιών. Αυτοί που τον χρησιμοποιούν (Levin) περιγράφουν με αυτόν τις περιπτώσεις εκείνες όπου παρατηρείται ελάττωση των κυττάρων στις ωριμότερες μορφές χωρίς να παρατηρείται κάτι ανάλογο στα πρώτα στάδια της σπερματογένεσης (Εικόνα 4) (19). Σύμφωνα με άλλους ωστόσο, οι αλλοιώσεις αυτές θα πρέπει να αποδίδονται με τον όρο της υποσπερματογένεσης (24). Και στις δύο μορφές διακοπής της σπερματογένεσης – πλήρη ή ατελή – η διάμετρος των σωληναρίων είναι ελαττωμένη, χωρίς ωστόσο ιστολογικές αλλοιώσεις στο τοίχωμα των σωληναρίων, στον διάμεσο ιστό και στα διάμεσα κύτταρα (23).
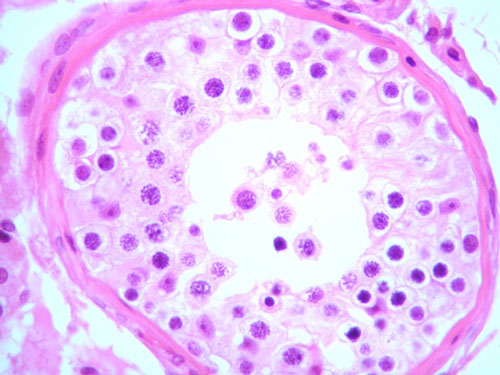
Εικόνα 3. Πλήρης διακοπής της σπερματογένεσης στο επίπεδο του σπερματοκυττάρου 1ης τάξεως (Α-Ε 400x). Πηγή: προσωπικό αρχείο συγγραφέως.
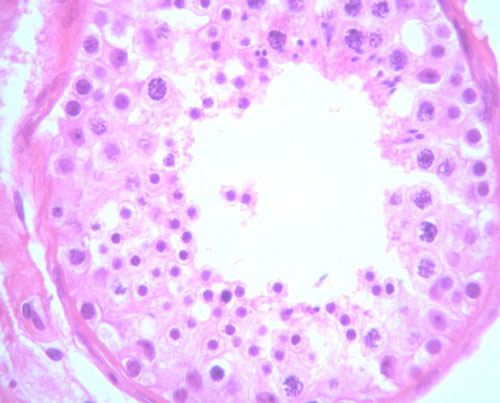
Εικόνα 4. Ατελής διακοπής της σπερματογένεσης στο επίπεδο της στρογγύλης σπερματίδας (Α-Ε 400x). Πηγή: προσωπικό αρχείο συγγραφέως.
Η διακοπή της σπερμκατογένεσης δεν αποτελεί αλλοίωση ενός συγκεκριμένου αιτιολογικού παράγοντα. Μάλιστα, ο ίδιος βλαπτικός παράγοντας, ανάλογα με την διάρκεια και την ένταση της προσβολής, προκαλεί διακοπή της σπερματογένεσης ή υποσπερματογένεση. Μεταξύ των άλλων διακοπή της σπερματογένεσης προκαλεί: α) ο υπογοναδοτρόφος υπογοναδισμός των ενηλίκων β) η ακτινοθεραπεία και γ) η χημειοθεραπεία.
Στην διακοπή της σπερματογένεσης η συσχέτιση των ιστολογικών ευρημάτων με τον αριθμό των σπερματοζωαρίων του σπέρματος είναι συνήθως καλή. Στην πλήρη διακοπή ο αριθμός των σπερματοζωαρίων του σπέρματος είναι συνήθως μηδενικός. Όταν λίγα σπερματοζωάρια αναγνωρίζονται στο σπέρμα τότε σίγουρα η βιοψία δεν είναι αντιπροσωπευτική του ορχικού παρεγχύματος και σίγουρα μια δεύτερη βιοψία από κάποια άλλη θέση του όρχεως θα έδειχνε λίγες επιμήκεις σπερματίδες σε κάποια ορχικά σωληνάρια. Όταν σε πολλαπλές βιοψίες νωπού ορχικού παρεγχύματος αναζητήθηκαν σπερματοζωάρια, σε ασθενείς που υποβλήθηκαν σε τεχνικές υποβοηθούμενης αναπαραγωγής, σε κάποιους από αυτούς ανευρέθηκαν σπερματοζωάρια, μολονότι η ιστολογική διάγνωση ήταν πλήρης διακοπή της σπερματογένεσης. Οι ασθενείς με ατελή διακοπή της σπερματογένεσης έχουν συνήθως ολιγοσπερμία (23).
Απλασία του σπερματικού επιθηλίου (germinal cell aplasia, Sertoli cell only syndrome)
Με τον όρο «απλασία του σπερματικού επιθηλίου» περιγράφεται η ορχική αλλοίωση στην οποία τα σπερματικά σωληνάρια παρουσιάζουν ελάττωση της διαμέτρου και επένδυση μόνο από μετεφηβικά κύτταρα Sertoli (Εικόνα 5). Διακρίνονται δύο μορφές: α) η ιδιοπαθής απλασία του σπερματικού επιθηλίου και β) η επίκτητη. Στην ιδιοπαθή, η βασική μεμβράνη και ο περισωληνώδης υμένας δεν παρουσιάζουν πάχυνση και η διάμετρος των σωληναρίων είναι φυσιολογική ή ελαφρά ελαττωμένη. Τα διάμεσα κύτταρα είναι φυσιολογικά. Στο ιστορικό των ασθενών δεν αναφέρεται νόσημα ή κάποια άλλη αιτία (ακτινοβολία κ.λ.π.) που θα μπορούσε να βλάψει το σπερματικό επιθήλιο (25). Στην επίκτητη μορφή, που οφείλεται σε βλαπτική δράση διαφόρων παραγόντων (τοξίνες, χημειοθεραπευτικά φάρμακα, ακτινοβολία), παρατηρείται εκτός από την καταστροφή των σπερματικών κυττάρων, πάχυνση του τοιχώματος των σπερματικών σωληναρίων και ίνωση του διάμεσου συνδετικού ιστού. Στις επίκτητες μορφές, στα πρώτα στάδια, σε βάθος χρόνου, η αλλοίωση είναι αναστρέψιμη, όταν ο βλαπτικός παράγοντας απομακρυνθεί. Είναι κρίσιμο εδώ να τονιστεί ότι, μολονότι η αρχική – διαγνωστική – βιοψία δείχνει πλήρη απλασία του σπερματικού επιθηλίου, είναι πιθανή η ανεύρεση σπερματοζωαρίων, σε πολλαπλές λήψεις ορχικού ιστού από τον όρχι, με την μέθοδο (TESE) της υποβοηθούμενης αναπαραγωγής (23).

Εικόνα 5. Πλήρης απλασία του σπερματικού επιθηλίου (Α-Ε 400x). Πηγή: προσωπικό αρχείο συγγραφέως.
Μερικές φορές μια βιοψία παρουσιάζει αλλοιώσεις πλήρους απλασίας του σπερματικού επιθηλίου με διάσπαρτα σπερμογόνια. Την αλλοίωση αυτή ο Levin την χαρακτηρίζει ως υποπλασία των γεννητικών κυττάρων και επισημαίνει ότι θα πρέπει να αξιολογείται με ιδιαίτερη προσοχή για πιθανή κακοήθη εξαλλαγή των σπερμογονίων (Ca in situ) (23).
Απλασία του σπερματικού επιθηλίου και εστιακή σπερματογένεση (germinal cell aplasia and focal spermatogenesis)
Από παλιά ακόμη είχε παρατηρηθεί ότι σε μερικές περιπτώσεις απλασίας του σπερματικού επιθηλίου μερικά σπερματικά σωληνάρια παρουσιάζουν σπερματογενετική δραστηριότητα, συνήθως ελαττωμένη. Τις περιπτώσεις αυτές ο Levin τις ταξινόμησε ως «απλασία του σπερματικού επιθηλίου με εστιακή σπερματογένεση» (Germinal cell aplasia and focal spermatogenesis). Οι ασθενείς με απλασία του σπερματικού επιθηλίου και εστιακή σπερματογένεση παρουσιάζουν έντονη ελάττωση των σπερματοζωαρίων του σπέρματος (23).
Η απλασία του σπερματικού επιθηλίου με εστιακή σπερματογένεση, δεν αποτελεί αλλοίωση ενός συγκεκριμένου αιτιολογικού παράγοντα (23).
Σωληναριακή και περισωληναριακή σκλήρυνση
Η σκλήρυνση αποτελεί το τελικό αποτέλεσμα δράσης ενός βλαπτικού παράγοντα που προσβάλλει τον όρχι (19). Παρατηρείται εξαφάνιση των σπερματικών κυττάρων από τα υαλοειδοποιημένα σπερματικά σωληνάρια και των διάμεσων κυττάρων από τον διάμεσο σκληρυντικό συνδετικό ιστό. Οι όρχεις είναι μικροί, και τα επίπεδα της LH και FSH υψηλά. Στο κατάλληλο κλινικό υπόστρωμα, η σκλήρυνση των σωληναρίων με τους υπερπλαστικούς όζους των διάμεσων κυττάρων υποδηλώνει σύνδρομο του Klinefelter. Η αναζήτηση με ειδικές χρώσεις των ελαστικών ινών στον περισωληνώδη χιτώνα βοηθάει στην ταξινόμηση των όρχεων με σωληναριακή σκλήρυνση. Εάν η σκλήρυνση έγινε πριν την εφηβεία, όπως στο σύνδρομο του Klinefelter, τότε παρατηρείται απουσία ελαστικών ινών από τον περισωληνώδη χιτώνα (18). Όταν η σκλήρυνση είναι καθολική και αφορά και τους δύο όρχεις τότε η αλλοίωση μπορεί λειτουργικά να χαρακτηρισθεί ως «όρχεις τελικού σταδίου» (23).
4. Μέθοδοι ποσοτικού προσδιορισμού των ιστολογικών αλλοιώσεων της βιοψίας των όρχεων
Για τις ανάγκες της ακριβούς περιγραφής των ιστολογικών αλλοιώσεων σε διάφορες δημοσιεύσεις, της σύγκρισης διαφόρων ομάδων ασθενών και της δυνατότητας πρόβλεψης ή επανεκτίμησης των αποτελεσμάτων της θεραπείας, επινοήθηκαν ακριβείς ποσοτικές μέθοδοι περιγραφής της σπερματογένεσης και των άλλων δομικών στοιχείων των όρχεων.
Οι πρώτες προσπάθειες έγιναν τη δεκαετία του 1950 και του 1960 χρησιμοποιώντας υψηλής αναπαραγωγιμότητας αλλά έντονα χρονοβόρες τεχνικές, μερικές από τις οποίες απαιτούσαν πολύπλοκες ογκομετρικές μετρήσεις και άλλες τη μέτρηση όλων των κυττάρων από ένα μεγάλο αριθμό σπερματικών σωληναρίων (26 – 28). Στη συνέχεια προτάθηκαν διάφορες άλλες απλούστερες μέθοδοι ωστόσο καμία δεν έτυχε καθολικής αποδοχής.
Σήμερα από τις νεότερες μεθόδους, εκείνες με την ευρύτερη αποδοχή είναι: 4.1. Κυρίως η μέθοδος Levin, τα βασικά χαρακτηριστικά της οποίας περιγράφηκαν ήδη στην προηγηθείσα ταξινόμηση των αλλοιώσεων του σπερματικού επιθηλίου. 4.2. Η μέθοδος Johnsen και 4.3. Η μέθοδος Silber και Rodriguez- Rigau. Για την πληρότητα της περιγραφής παραθέτουμε κάποια στοιχεία από τις μεθόδους Johnsen και Silber.
4.2. Μέθοδος Johnsen
Η μέθοδος Johnsen βασίζεται στην προϋπόθεση ότι κατά την αλλοίωση του σπερματικού επιθηλίου, παρατηρείται μία διαδοχική εξαφάνιση των κυττάρων της σπερματικής σειράς, ξεκινώντας από την εξαφάνιση των ωριμοτέρων μορφών (σπερματοζωάρια) και καταλήγοντας στα αωρότερα κύτταρα της σπερματικής σειράς (σπερμογόνια) με εξαφάνιση στο τέλος και των κυττάρων του Sertoli. Κάθε σωληνάριο θα πρέπει να εξετάζεται χωριστά και να καταγράφεται η ωριμότερη μορφή κυττάρου που αναγνωρίζεται στο σπερματικό του επιθήλιο, η οποία προσδιορίζει και την ποιότητα του σπερματικού επιθηλίου. Η ποιότητα του επιθηλίου διαβαθμίζεται με μία κλίμακα από το 1 έως το 10, όπως αναλυτικά περιγράφεται στον πίνακα 1. Η τελική εικόνα της βλάβης του όρχι βγαίνει από το μέσο όρο (mean score) της βλάβης του συνόλου των σωληναρίων ο οποίος υπολογίζεται ως εξής: Ο αριθμός των σωληναρίων κάθε βαθμίδας πολλαπλασιάζεται με τον αριθμό της βαθμίδας. Το άθροισμα των γινομένων όλων των βαθμίδων διαιρείται με το άθροισμα του αριθμού των σωληναρίων από κάθε βαθμίδα. Το εξαγόμενο είναι o μέσος όρος ( Mean Scor, MS).
Πίνακας 1. Ταξινόμηση του σπερματικού επιθηλίου με την μέθοδο Johnsen
| Score | Περιγραφή των ευρημάτων |
| 10 | Πλήρης σπερματογένεση με πολλά σπερματοζωάρια, σπερματικό επιθήλιο ισοπαχές, αυλός ανοικτός. |
| 9 | Πολλά σπερματοζωάρια, σπερματικό επιθήλιο αποδιοργανωμένο με απόπτωση και πλήρωση του αυλού |
| 8 | Λίγα σπερματοζωάρια (< 5-10) |
| 7 | Απουσία σπερματοζωαρίων, πολλές σπερματίδες |
| 6 | Απουσία σπερματοζωαρίων, λίγες σπερματίδες ( < 5-10 ) |
| 5 | Απουσία σπερματοζωαρίων, απουσία σπερματίδων, πολλά σπερματοκύτταρα |
| 4 | Απουσία σπερματοζωαρίων, απουσία σπερματίδων, λίγα σπερματοκύτταρα ( < 5 ) |
| 3 | Τα σπερμογόνια και τα Sertoli είναι τα μόνα κύτταρα του σπερματικού επιθηλίου |
| 2 | Παρουσία μόνο κυττάρων Sertoli |
| 1 | Απουσία κυττάρων από το ορχικό σωληνάριο |
Πηγή: Johnsen S.G.: Testicular biopsy score count- a method for registration of spermatogenesis in human testis: normal values and results in 335 hypogonadal males. Hormones 1970;1:2.
Εκτός από την αξιολόγηση του σπερματικού επιθηλίου, ανάλογη αξιολόγηση θα πρέπει να γίνεται και για τα διάμεσα κύτταρα. Όταν ο αριθμός των κυττάρων του Leydig είναι φυσιολογικός, το score είναι 3 (Leydig Score, LS 3). Στις βαθμίδες 2 και 1 έχουμε λίγα ή καθόλου κύτταρα, στην 4 ελαφρά έως μέτρια υπερπλασία, στην 5 έντονη υπερπλασία και στην 6 την μέγιστη δυνατή υπερπλασία, συνήθως κατά όζους. Όταν τα κύτταρα του Leydig είναι φυσιολογικά, καταλαμβάνουν το 3% του οπτικού πεδίου της βιοψίας των όρχεων. Θα πρέπει επίσης να υπολογίζεται η εσωτερική διάμετρος, 10 εγκάρσια κομμένων σωληναρίων, χρησιμοποιώντας προσοφθάλμιο μικρομετρικό φακό (29).
Η αρχική εφαρμογή της μεθόδου από τον Jonhsen έγινε σε 352 βιοψίες από 335 ασθενείς η κάθε μια από της οποίες περιείχε κατά μέσο όρο 113 σπερματικά σωληνάρια. Ο μέσος όρος (mean score) στις διάφορες ομάδες ασθενών παρουσιάζεται στον Πίνακα 2.
Πίνακας 2. Μέσος όρος σε 113 ασθενείς όπως αξιολογήθηκαν από τον Johnsen.
| Μέσος όρος (Mean Score) | |
| Φυσιολογικός όρχις | 9,38 |
| Όρχις ευνούχου | 3,80 |
| Επίκτητη ανεπάρκεια υπόφυσης | 6,09 |
| Σύνδρομο του Klinefelter | 1,25 |
| Απλασία του σπερματικού επιθηλίου | 2,0 |
| Έντονη υποσπερματογένεση | 5,32 |
| Μέτρια υποσπερματογένεση | 7,80 |
Πηγή: Johnsen SG: Testicular biopsy score count- a method for registration of spermatogenesis in human testis: normal values and results in 335 hypogonadal males. Hormones 1970;1:2.
Μολονότι η μέθοδος κατά Johnsen επιτρέπει την αξιολόγηση πολλών σπερματικών σωληναρίων με διαφορετική ωρίμανση του σπερματικού επιθηλίου, η χρήση της μεθόδου είναι μάλλον χρονοβόρος και η προϋπόθεση ότι η εξαφάνιση των κυττάρων ακολουθεί την προηγούμενα περιγραφείσα σειρά θα μπορούσε να μην είναι πάντοτε ακριβής. Ωστόσο, η μέθοδος έχει πολλά πλεονεκτήματα όπως την αντικειμενική αξιολόγηση του κυτταρικού πληθυσμού των σπερματικών σωληναρίων, που την καθιστά μία από τις ευρύτερα αποδεκτές μεθόδους.
4.3. Μέθοδος Silber and Rodriguez- Rigau
Το 1981, οι Silber και Rodrigyez- Rigau πρότειναν μία καινούρια μέθοδο ποσοτικής αξιολόγησης τα πλεονεκτήματα της οποίας είναι η απλότητα και η ταχύτητα της εφαρμογής της. Στη μελέτη τους συμμετείχαν: α) 21 ασθενείς με κλινικά διαπιστωμένη απουσία απόφραξης των πόρων, β)δύο ολιγοσπερμικοί ασθενείς με «μερική απόφραξη της επιδιδυμίδας» και γ) δύο αζωοσπερμικοί ασθενείς με απόφραξη. Η μέθοδος περιελάμβανε αξιολόγηση 10 ορχικών σωληναρίων από κάθε όρχι, δηλαδή μία συνολική αξιολόγηση 20 σωληναρίων από κάθε ασθενή. Μετρήθηκαν μόνο οι «ώριμες, επιμήκεις σπερματίδες» (εκείνες με τις ωοειδείς κεφαλές). Οι πρωϊμότερες κυτταρικές μορφές του σπερματικού επιθηλίου και τα κύτταρα του Sertoli δεν αξιολογήθηκαν. Οι ασθενείς χωρίς την απόφραξη και με λιγότερα από 10 εκατομμύρια σπερματοζωάρια ανά κυβικό εκατοστό σπέρματος είχαν πάντοτε λιγότερες από 20 ώριμες σπερματίδες ανά ορχικό σωληνάριο. Οι ασθενείς με περισσότερα από 10 εκατομμύρια σπερματοζωάρια ανά κ. εκ. σπέρματος είχαν πάντοτε περισσότερες από 20 σπερματίδες ανά ορχικό σωληνάριο. Παρατηρήθηκε δηλαδή στενή σχέση των σπερματίδων με την πυκνότητα του σπέρματος γεγονός που επιτρέπει την πρόβλεψη της πυκνότητας του σπέρματος, που θα επιτευχθεί μετά από αποκατάσταση μιας αποφρακτικής βλάβης. Στους δύο ολιγοσπερμικούς ασθενείς με «τη μερική απόφραξη της επιδιδυμίδας» , η βιοψία έδειξε άφθονη παρουσία σπερματίδων ανά ορχικό σωληνάριο.
Συμπερασματικά οι συγγραφείς πρότειναν ότι στους έντονα ολιγοσπερμικούς ασθενείς, η παρουσία περισσοτέρων από 20 ώριμων σπερματίδων ανά ορχικό σωληνάριο είναι ενδεικτική μερικής απόφραξης της επιδιδυμίδας. Ένα μειονέκτημα αυτής της μεθόδου είναι η αδυναμία αναγνώρισης της όψιμης διακοπής της σπερματογένεσης στην οποία η άφθονη παρουσία ώριμων σπερματίδων στη βιοψία μπορεί να συνδυάζεται με έντονη ολιγοσπερμία ή άζωοσπερμία χωρίς την παρουσία μερικής απόφραξης των πόρων. Η μέθοδος αυτή επίσης δεν αξιολογεί τις έντονες αλλοιώσεις υποσπερματογένεσης και ως εκ τούτου εφαρμόζεται μόνο σε μία υποομάδα βιοψιών των όρχεων. Συμπερασματικά, μολονότι η μέθοδος είναι λιγότερο χρονοβόρος συγκριτικά με όλες τις προηγούμενες μεθόδους, παρουσιάζει το σοβαρό μειονέκτημα της αδυναμίας εφαρμογής σε όλες τις βιοψίες των όρχεων και της ανακρίβειας σε ορισμένες περιπτώσεις (30).
Βιβλιογραφία
1. Charny CW. Testicular biopsy: its value in male sterility. JAMA 1940; 115(17):1429-33.
2. Male Infertility Best Practice Policy of the American Urological Association. Practice Committee of the American Society for Reproductive Medicine. Report on evaluation of the azoospermic male. Fertil Steril 2006; 86(Suppl 5): s210-s5.
3. Coburn M, Wheeler TM.: Testicular Biopsy in Male Infertility Evaluation. In: Lipshultz L. I., and Howards S.S. (eds). Infertility in the Male, 2nd Edition1991, Mosby Year Book, St Louis, 223-253.
4. Ibrahim AA, Award HA, El-Hagar S et al. Bilateral testicular biopsy in men with varicocele. Fertil. Steril 1977; 28(6):663-7.
5. Posinovec J. The necessity for bilateral biopsy in oligo and azoospermia. Int J Fertil 1976; 21:189-191.
6. Tillnger KG. Testicular morphology; a histo-pathological study with special reference to biopsy findings in hypogonadism with mainly endocrine disorders and in gynecomastia. Acta Endocrinol 1957; 24(Suppl 30):1-192.
7. Netto NR. Needle method of testicular biopsy. Int Surg 1974; 59:172-172.
8. Cohen MS, Frye S, Warner RS, Leiter E. Testicular needle biopsy in diagnosis of infertility. Urology 1984; 24(5):439-42
9. Raifer J, Binder S. Use of biopsy gun for transcutaneus testicular biopsy. J Urol 1989; 142(4):1021-2.
10. Pesce CM, Reale A. Testis morphometry in varicocele. Arch Androl 1985; 15(2-3):193-197.
11. Trainer TD. Testis and escretory duct system. In Mills SE. ed. Histology for Pathologist. 3rd edition. Philadelphia : Lippincott Williams & Wilkins, 2007:943-953
12. Nistal M, Paniagua R, Lopez-Pajares I. Ultrastructure of Leydig cells in Klinefelter’s syndrome with 48, XXYY karyotype. Virchows Arch B Cell Pathol. 1978; 28(1):39-46
13. Paniagua R, Nistal M, Bravo MP. Leydig cell types in primary testcular disorders. Hum Pathol 1984;15(2):181-90
14. Horica C, Hadziselimovic F, Kreutz G, Bandhauer K. Ultrastructural studies of the contorted and contralateral testicle in unilateral testicular torsion. Eur Urol 1981; 8(6):358-62.
15. Krester D.M., Burger H.G.:Ultrastructure studies of the man Sertoli cell in normal men and males with hypogonadotrophic hypogonadism before and after gonadotropic treatment. In: Saxen B.B., Berlin C.G., Gandy H.M. (eds) 1972;. Gonadotropins. New York.
16. Pesce C. The testicular biopsy in the evaluation of male infertility. Seminars in diagnostic pathology, 1987; 4(4):264-274.
17. Connolly NK. Mumps Orchitis without Parotitis in Infants. Lancet 1953; 264(10):69-70.
18. Nistal M., Pagniagua R.: Testicular biopsy, basic testicular lesions. In: Testicular and Epididimal Pathology, New York, Thiema –Stratton 1984.
19. Levin HS. Testicular biopsy in the study of male infertility: its current usefulness, histologic techniques, and prospects for the future. Hum Pathol. 1979; 10(5):569-84.
20. Guerin JF, Rozycka M, Lenczowski S, Dziedzic-Goclawska A, Ostrowski K, Czyba JC, et al. Objective evaluation of fibrosis in human testicular biopsies by analysis based on optical diffractometry. Acta Anat 1986; 125(2):88-92.
21. Heller CG. Clermont Y, Kinetics of the germinal epithelium in man. Recent Prog Horm Res 1964; 20:545-75.
22. Trainer T. Testis and excretory duct system. In: Sternberg S. (Eds) 1992. Histology for pathologists. Raven Press Ltd, New York, pp731-747
23. Levin H.S. Nonneoplastic Diseases of the Testis. In Mills SE. ed. 2010; Stenberg ‘s Diagnostic Surgical Pathology. 5rd edition. Philadelphia : Lippincott Williams & Wilkins, pp 1914-1943
24. Coburn M, Wheeler T, Lipshultz LI. Testicular Biopsy – Its Use and Limitations. Urol Clin N Am. 1987; 14(3):551-61.
25. Del Castilo EB, Trabucco A, de la Balze FA. Syndrome produced by absence of the germinal epitelium without impairment of the Sertoli or Leydig Cell. J Clin Endocrin 1947; 7(7):493-502
26. Mancini RE, Rosemberg E, Cullen M, Lavieri JC, Vilar O, Bergada C, et al. Cryptorchid and Scrotal Human Testes. I. Cytological, Cytochemical and Quantitative Studies. J clin Endocrinol 1965; 25(7):927-42.
27. Roosen-Runge EC. Quantitative investigations on human testicular biopsies. I. Normal testis. Fertil Steril. 1956; 7(3):251-61.
28. Steinberger E, Tjioe DY. A method for quantitative analysis of human seminiferous epithelium 1968; Fertil Steril 19:960-970.
29. Johnsen S. Testicular biopsy score count–a method for registration of spermatogenesis in human testes: normal values and results in 335 hypogonadal males. Horm Res in Paediatr 1970; 1(1):2-25.
30. Silber SJ, Rodriguez-Rigau LJ, Quantitative analysis of testicle biopsy: determination of partial obstruction and prediction of sperm count after surgery for obstruction. Fertil Steril 1981; 36(4):480-5.
Created: 28 August 2015
Last update: 28 August 2015