Αναστάσιος Μόρτογλου
Ενδοκρινολόγος
Τομέας Μεταβολισμού Ιατρικού Κέντρου Αθηνών
1. Εισαγωγή
Πρόσφατες μελέτες έχουν δείξει ότι αμέσως μετά και ανάλογα με τη φύση του γεύματος δημιουργούνται στον οργανισμό προφλεγμονώδεις αντιδράσεις οι οποίες ευθύνονται σε μεγάλο βαθμό για τα καρδιο-αγγειακά νοσήματα, την παχυσαρκία, τα χρόνια φλεγμονώδη νοσήματα, την ινσουλινοαντίσταση και το διαβήτη2 (1, 2). Μάλιστα, πρόσφατο εξώφυλλο του περιοδικού TIME χαρακτήρισε αυτές τις ιδιότητες των τροφών σαν το “μυστικό δολοφόνο”.
Οι μηχανισμοί που ελέγχουν το ενεργειακό ισοζύγιο και το ανοσοποιητικό σύστημα είναι ίσως οι πιο σημαντικές προϋποθέσεις για την επιβίωση του ανθρώπου, αν και ανάλογα συστήματα έχουν αναπτυχθεί εξελικτικά και σε πολλά άλλα είδη. Η αρμονική συνεργασία των 2 αυτών συστημάτων είναι απαραίτητη για τη σωστή λειτουργία ενός εκάστου εξ αυτών.
Αν και η οξεία απάντηση του ανοσοποιητικού συστήματος σε κάποια μικροβιακή φλεγμονή ή σε καταστάσεις οξείας καταστροφής ιστών είναι λίαν ωφέλιμη αντίδραση, η χρόνια συστηματική ήπιας έντασης φλεγμονή ασκεί επιβαρυντικές αντιδράσεις αφού μια μεγάλη ποικιλία αυτοάνοσων νόσων εξαρτάται σε μεγάλο βαθμό από αυτή.
Τα χαρακτηριστικά της ήπιας έντασης χρόνιας φλεγμονής είναι (3):
- Εκλυτικοί παράγοντες: Μεταβολικές διαταραχές, χρόνιες φλεγμονές
- Εμπλεκόμενες κυτταρικές σειρές: Μονοκύτταρα, μακροφάγα, Τ- και Β-κύτταρα, λιποκύτταρα
- Κύριοι διαμεσολαβητές: Κυτταροκίνες, Χυμοκίνες, Λιποκυτταροκίνες, εικοσανοειδή, ROS, υδρολυτικά ένζυμα
- Έναρξη: Επιβραδυνόμενη
- Διάρκεια: Απεριόριστη
- Επιπτώσεις: Αν και δεν υπάρχουν οξέα κλινικά φαινόμενα, δημιουργούνται σιωπηρές αγγειακές βλάβες, ινσουλινοαντίσταση και ενδοκυττάρια εναπόθεση λίπους
Η χρόνια συστηματική προφλεγμονώδης αντίδραση εξαρτάται κατά κύριο λόγο από την αυξημένη πρόσληψη θερμίδων και μακροθρεπτικών συστατικών και αυτά ενεργοποιούν τις ίδιες οδούς σηματοδότησης με αυτές που ενεργοποιούνται στις κλασικές φλεγμονές. Οι παράγοντες που ενεργοποιούνται μεταγευματικά ανάλογα με την ποιότητα και την ποσότητα της τροφής είναι (3):
- Κυτταροκίνες: TNFα, IL-6, IL-1β, IFN-γ
- Χυμοκίνες: MCP-1, MIP-1α,
- Πρωτεΐνες οξείας φάσης: CRP, SAA, Ινωδογόνο
- Μόρια προσκόλλησης: VCAM-1, ICAM-1, P-selectin, E-selectin
- Λιποκυτταροκίνες: Λεπτίνη, Αντιπονεκτίνη
- Λευκά αιμοσφαίρια: (μονοπύρηνα, ηωσινόφιλα).
Θα πρέπει να τονισθεί στο σημείο αυτό ότι υπάρχουν σημαντικές ατομικές διαφορές στο συνολικό αριθμό και στον τύπο των λευκοκυττάρων καθώς και στους δείκτες φλεγμονής αφού μέχρι σήμερα δεν έχουν καθορισθεί γενικώς αποδεκτά φυσιολογικά όρια για αυτούς. Επιπλέον, εκτός από τους παράγοντες ενεργοποίησης της φλεγμονώδους αντίδρασης, υπάρχει ένας σημαντικός αριθμός τροποποιητών αυτής της αντίδρασης. Οι παράγοντες αυτοί είναι: η ηλικία, το σωματικό λίπος, το επίπεδο σωματικής δραστηριότητας, το φύλο, η κληρονομικότητα, το κάπνισμα, η εντερική χλωρίδα, η διατροφή, η χρήση φαρμάκων, το στρες, η ρύπανση του περιβάλλοντος, ιογενείς λοιμώξεις και διαταραχές ύπνου (εικόνα 1).
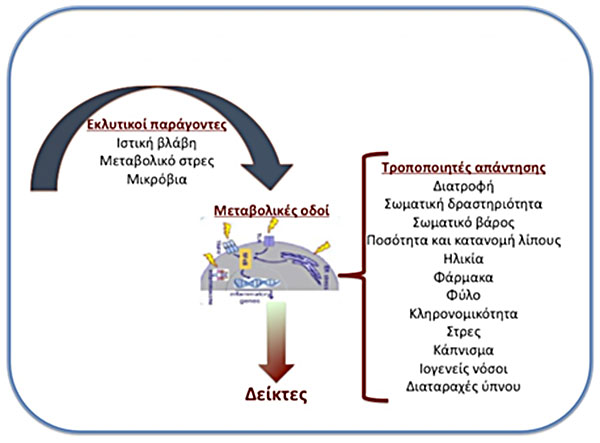
Εικόνα 1. Μηχανισμοί χρόνιας συστηματικής ήπιας φλεγμονής
Τα νοσήματα που συνδέονται με χρόνια χαμηλής έντασης φλεγμονώδη αντίδραση είναι (4):
- Η παχυσαρκία
- Η καρδιο-αγγειακή νόσος
- Η ατοπική δερματίτις
- Οι ιδιοπαθείς φλεγμονώδεις νόσοι του εντέρου (N.Crohn, ελκώδης κολίτις)
- Η ψωρίαση
- Αλλεργίες του αναπνευστικού συστήματος (ρινίτις, άσθμα)
- Η δυσανεξία στη γλουτένη (κοιλιοκάκη)
- Η ρευματοειδής αρθρίτις
Στο κεφάλαιο αυτό θα ασχοληθούμε αποκλειστικά με την επίδραση των τροφών, αφού θα υπάρξουν ανάλογες αναφορές και σε άλλα κεφάλαια.
Τα τρόφιμα μπορεί να έχουν σημαντικές φλεγμονώδεις αλλά και αντιφλεγμονώδεις επιδράσεις μέσω της θετικής ενίσχυσης των ρυθμιστικών μονοπατιών που ελέγχουν την έναρξη, την ένταση και τη διάρκεια της φλεγμονής. Μεταξύ των ποικίλων μεταβολικών οδών που οι οι τροφές επιδρούν στην ανοσολογική απάντηση, καθοριστικός είναι ο ρόλος των ρυθμιστικών Τ-λεμφοκυττάρων (Tregs) (5) (Εικόνα 2).

Εικόνα 2. Οξειδωτικό στρες και φλεγμονή
Η διατροφή του ανθρώπου έχει ‘μικτό’ χαρακτήρα, αποτελείται δηλαδή σχεδόν πάντα από πρωτεΐνες φυτικής ή ζωικής προέλευσης, λίπη και υδατάνθρακες. Ανάλογα όμως από τη διαθεσιμότητα των τροφίμων στους διάφορους πληθυσμούς, αλλά και τις γεωγραφικές περιοχές, τις συνήθειες και το κόστος, επικρατεί κάποιος τύπος διατροφικής ‘συμπεριφοράς’, από την οποία εξαρτάται σε μεγάλο βαθμό και το είδος της νοσηρότητας στους πληθυσμούς αναφοράς.
Για καθαρά διδακτικούς λόγους θα αναλυθούν ξεχωριστά οι επιδράσεις των κύριων μακροθρεπτικών στοιχείων της διατροφής στη χρόνια χαμηλής έντασης φλεγμονή.
Δε θα πρέπει βέβαια να ξεχνάμε και τη σημαντική επίπτωση του παράγοντα “ποσότητα”. Η αυξημένη πρόσληψη τροφής, εκτός από την παχυσαρκία και την εξ αυτής προερχόμενη φλεγμονή, προκαλεί και δυσλειτουργία των μιτοχονδρίων με απότοκο αυξημένο ρυθμό απόπτωσης, μεταβολικές διαταραχές και νόσους συνδεόμενες με το γήρας (6, εικόνα 3).

Εικόνα 3. Ενεργειακή πρόσληψη και μιτοχονδριακή λειτουργία
2. Πρωτεϊνούχες τροφές
Το κόκκινο κρέας, τα πουλερικά και τα ψάρια περιέχουν 20-35% πρωτεΐνες υψηλής βιολογικής αξίας, έχουν όμως σημαντικές διαφορές στην ποσότητα και ποιότητα του λίπους.
Το λίπος που περιέχεται στο κρέας κυμαίνεται από λιγότερο από 4% κατά βάρος στα άπαχα πουλερικά έως 30-40% σε λιπαρά μέρη κρέατος από οικόσιτα ζώα, το 50% του οποίου είναι κορεσμένο λίπος. Τα πουλερικά περιέχουν μικρότερο ποσοστό κορεσμένων λιπαρών οξέων (30-35%) και υψηλότερο ποσοστό πολυακόρεστων λιπαρών οξέων (15-30%).
Στα ψάρια, το ποσοστό σε λίπος κυμαίνεται από 0.5% έως 20% στα λιπαρά ψάρια. Το λίπος των ψαριών περιέχει πολύ μικρότερο ποσοστό κορεσμένων λιπαρών οξέων (20-25%) ενώ υπάρχουν και ποικίλες ποσότητες ω-3 λιπαρών οξέων μακράς αλύσου.
Η παροχή κρέατος στον Ελληνικό πληθυσμό έχει αυξηθεί από το 1961 (21 κιλά/άτομο/έτος), στα 86,3 κιλά/άτομο/έτος το 2001. Ευτυχώς όμως, τα τελευταία χρόνια υπάρχουν πτωτικές τάσεις αφού το 2009 η μέση παροχή ήταν 74.8 κιλά/άτομο/έτος.
Η χρόνια χαμηλής έντασης φλεγμονή έχει συνδεθεί αιτιολογικά με το μεταβολικό σύνδρομο, το διαβήτη2, τη στεφανιαία νόσο καθώς και με κάποιες κακοήθεις νεοπλασίες.
Η μελέτη CARDIO2000 στον Ελληνικό πληθυσμό έδειξε ότι η αυξημένη κατανάλωση κόκκινου κρέατος αυξάνει την πιθανότητα εμφάνισης οξέος στεφανιαίου συνδρόμου κατά 4,9 φορές και του λευκού κρέατος κατά 3,7 φορές (7).
Η πλειοψηφία των επιστημονικών δεδομένων συγκλίνει ότι η συνολική πρόσληψη κρέατος ή κόκκινου κρέατος, αυξάνει την πιθανότητα εμφάνισης διαβήτη 2 (8). H μελέτη MEDIS στον Ελληνικό πληθυσμό έδειξε ότι για κάθε 5% αύξηση της κατανάλωσης πρωτεΐνης από κρέας και τα προϊόντα του υπήρξε 34% μεγαλύτερη πιθανότητα ύπαρξης διαβήτη 2 (9).
Σε άλλη πρόσφατη μελέτη που έγινε σε μεγάλο δείγμα του Ελληνικού πληθυσμού (10), τα επίπεδα της συστάτιν C μειώθηκαν αντιστρόφως ανάλογα με την κατανάλωση κόκκινου κρέατος, ενώ τα επίπεδα της αιμοσφαιρίνης και του αιματοκρίτη αυξήθηκαν. Αντίθετα, η αυξημένη κατανάλωση ζωικής πρωτεΐνης χωρίς αίμη μείωσε τα επίπεδα των τριγλυκεριδίων, του σιδήρου και της αιμοσφαιρίνης, ενώ η αυξημένη κατανάλωση φυτικής πρωτεΐνης μείωσε τα επίπεδα των αιμοπεταλίων.
Σε πανευρωπαϊκό επίπεδο, μεγάλη επιδημιολογική μελέτη έδειξε ότι η αυξημένη κατανάλωση κόκκινου κρέατος χαρακτηρίζεται από αύξηση των κυκλοφορούντων επιπέδων γGT και hsCRP (11), αλλά και στις ΗΠΑ, σε 3690 γυναίκες χωρίς διαβήτη που συμμετείχαν στη Nurses’ Health Study, δείχθηκε ότι η μεγαλύτερη κατανάλωση κρέατος, επεξεργασμένου ή όχι, συνοδευόταν από αύξηση της CRP, της φεριτίνης, της ινσουλίνης νηστείας και της ΗbA1c, ενώ ήταν χαμηλότερα τα επίπεδα της αντιπονεκτίνης (12).
Οι προτεινόμενοι μηχανισμοί της δυσμενούς επίδρασης στην υγεία του κόκκινου κρέατος φαίνονται στην εικόνα 4.
Εικόνα 4. Πιθανοί μηχανισμοί επίδρασης του κόκκινου κρέατος στην υγεία
3. Λίπη και έλαια
Πρόκειται για ουσίες αδιάλυτες στο νερό, διαλυτές σε οργανικούς διαλύτες και είναι εστέρες λιπαρών οξέων ή λιπαρά οξέα που μπορούν να εστεροποιηθούν. Στη φύση υπάρχουν πάνω από 40 είδη λιπαρών οξέων. Άλλα από αυτά είναι κορεσμένα-SFA, άλλα μονοακόρεστα-MUFA και άλλα πολυακόρεστα-PUFA (πίνακας 1). Η σύσταση της διατροφής σε λιπαρά οξέα επηρεάζει σημαντικά τη χρόνια χαμηλής έντασης φλεγμονή μέσω της βιοσύνθεσης δραστικών διαμεσολαβητών.
Πίνακας 1. Τα σημαντικότερα φυσικά λιπαρά οξέα.
| Όνομα |
Δομή, άτομα C:ακόρεσ.δεσμοί |
Xαρακτηρισμός | Kύρια φυσική πηγή |
| Kορεσμένα λιπαρά οξέα | |||
| Bουτυρικό |
C4:0 |
Bραχεία άλυσος | Γαλακτοκομικά προΐντα |
| Kαπροϊκό |
C6:0 |
Bραχεία άλυσος | Γαλακτοκομικά προΐντα |
| Kαπρυλικό |
C8:0 |
Bραχεία άλυσος | Γαλακτοκομικά προΐντα |
| Kαπρικό |
C10:0 |
Mέση άλυσος | Γαλακτοκομικά προΐντα |
| Δαφνικό |
C12:0 |
Mέση άλυσος | Γαλακτοκομικά προΐντα |
| Mυριστικό |
C14:0 |
Mέση άλυσος | Γαλακτοκομικά προΐντα |
| Παλμιτικό |
C16:0 |
Mακρά άλυσος | Βαμβακέλαιο, Bούτυρο, λίπος του κρέατος |
| Στεαρικό |
C18:0 |
Mακρά άλυσος | Λίπος του κρέατος, βούτυρο, σοκολάτα |
| Aραχιδικό |
C20:0 |
Mακρά άλυσος | Σπορέλαια, ξηροί καρποί |
| Bεχενικό |
C22:0 |
Mακρά άλυσος | Φυστίκια, φυστικέλαιο |
| Mονο-ακόρεστα λιπαρά οξέα | |||
| Παλμιτολεϊκό |
C16:1 |
Ιχθυέλαια, λίπος κρέατος, ψάρια | |
| Oλεϊκό |
C18:1 |
Eλαιόλαδο, αβοκάντο, αυγό, βούτυρο, σπορέλαια | |
| Eρουσικό οξύ |
C22:1 |
Rapeseed oil | |
| Πολυ-ακόρεστα λιπαρά οξέα | |||
| Λινολεϊκό |
C18:2 |
Φυτικά έλαια, ξηροί καρποί, άπαχο κρέας, αυγό | |
| α- και γ-Λινολενικό οξύ |
C18:3n3, C18:3n6 |
Σογιέλαιο, rapeseeds oil | |
| Aραχιδονικό οξύ |
C20:4n6 |
Εντόσθια, κυνήγι, άπαχο κρέας, αυγό | |
| Eïκοσαπεντανοϊκό οξύ (EPA) |
20:5n3 |
Ψάρια | |
| Nτοκοσαεξανοϊκό οξύ |
22:6n3 |
Ψάρια, συκώτι, αυγό |
O αριθμός δίπλα στο ‘C’ εκφράζει τα άτομα άνθρακος του λιπαρού οξέος. O αριθμός μετά το ‘:’ εκφράζει τον αριθμό των ακόρεστων δεσμών. O αριθμός μετά το ‘n’ (‘n’ σημαίνει ότι και το ‘ω’), δηλώνει την θέση από την αρχή του μορίου του λιπαρού οξέος που βρίσκεται ο πρώτος ακόρεστος χημικός δεσμός.
Τα λίπη και τα έλαια αποτελούν σημαντικό διατροφικό στοιχεία για το σύνολο του παγκόσμιου πληθυσμού λόγω της υψηλής περιεκτικότητας σε θερμίδες και της σχετικά χαμηλής τους τιμής. Καταναλώνονται ως συστατικό των τροφίμων ζωικής και φυτικής προέλευσης, περιέχονται σε βιομηχανοποιημένα τρόφιμα, χρησιμοποιούνται για το μαγείρεμα και μπορεί να προστεθούν στο έτοιμο φαγητό και στις σαλάτες.
Οι ιδιότητες των μορίων του λίπους καθορίζονται από το μήκος και τη δομή των λιπαρών οξέων από τα οποία αποτελούνται. Τα υγρά έλαια τείνουν να είναι πλουσιότερα σε ακόρεστα λιπαρά οξέα, ενώ τα στερεά λίπη πλουσιότερα σε κορεσμένα. Τα κορεσμένα λιπαρά οξέα περιέχουν αποκλειστικά μονούς δεσμούς, ενώ τα ακόρεστα λιπαρά οξέα έχουν ένα ή περισσότερους διπλούς δεσμούς.
Το λίπος από τα βοοειδή και τα πρόβατα έχει μεγαλύτερη αναλογία κορεσμένων σε σχέση με το λίπος των χοιρινών και των πουλερικών. Σε όλα τα ζώα, το υποδόριο λίπος περιέχει μικρότερο ποσοστό κορεσμένων λιπαρών οξέων σε σχέση με το σπλαγχνικό.
Στην Ελλάδα, σύμφωνα με τα στοιχεία του 2009, η παροχή ζωικού λίπους υπολογίζεται στα 4,3 κιλά/άτομο/έτος και η κατανάλωση φυτικών ελαίων στα 25,9 κιλά/άτομο/έτος (http://faostat.fao.org/site/354/default.aspx).
Η διατροφική πρόσληψη κάποιων λιπαρών οξέων, όπως τα ω-6 πολυακόρεστα λιπαρά οξέα, είναι δυνατόν να πυροδοτήσει τη διαδικασία της φλεγμονής.
Έχει δειχθεί ότι σε υγιή άτομα ακόμα και 1 μόνο γεύμα πλούσιο σε λίπος προκαλεί διέγερση του ενδοθηλίου όπως αποδεικνύεται από την αύξηση των μορίων προσκόλλησης VCAM-1 (vascular cell adhesion molecule-1) και ICAM-1 (intercellular adhesion molecule-1) με ταυτόχρονη αύξηση της IL-6 και του TNF-a και με παράλληλη αύξηση της IL-18, μιας προφλεγμονώδους κυτταροκίνης που εμπλέκεται στο μηχανισμό αποσταθεροποίησης της αθηρωματικής πλάκας (13, 14).
Αντίθετα, η πρόσληψη άλλων λιπαρών οξέων, π.χ. ω-3 PUFA, μπορεί να αναστείλει τη φλεγμονώδη αντίδραση.
Τα κορεσμένα λίπη προσλαμβάνονται κυρίως από τις ζωικές τροφές (κρέας και γαλακτοκομικά προϊόντα), τα μονοακόρεστα κυρίως μέσω του ελαιόλαδου, ενώ τα πολυακόρεστα προσλαμβάνονται ως μη-εστεροποιημένα λιπαρά οξέα, ως τριακετυλ-γλυκερόλη και ως φωσφολιπίδια. Οι εστερικοί δεσμοί των λιπών υδρολύονται από τις λιπάσες του ΓΕΣ και παράγονται μη-εστεροποιημένα λιπαρά οξέα και μονοακετυλ-γλυκερόλη. Τα PUFA, από τα οποία κυρίως προέρχονται οι εκ του λίπους παραγόμενοι διαμεσολαβητές, είναι πολύ ευάλωτα στη μη-ενζυματική οξείδωση. Αυτός είναι και ο λόγος που η αντιφλεγμονώδης δράση των ω-3 λιπαρών οξέων αυξάνει αν προσλαμβάνονται μαζί με αντι-οξειδωτικά (15).
Η κατανάλωση ω-3 και ω-6 λιπαρών οξέων έχει υποστεί σημαντικές αλλαγές τα τελευταία χρόνια. Στις δυτικού τύπου κοινωνίες έχει αυξηθεί η κατανάλωση ω6-λιπαρών οξέων (σπορέλαια), ενώ σε περιοχές με αυξημένη κατανάλωση αλιευμάτων επικρατεί η πρόσληψη ω3-λιπαρών οξέων. Είναι από μακρού γνωστό ότι ο αυξημένος λόγος ω6/ω3 διαδραματίζει σημαντικό ρόλο στις προφλεγμονώδεις αντιδράσεις αλλά και σε νόσους όπως η αθηρωμάτωση, η σήψη, η μαστίτιδα και οι κακοήθεις νεοπλασίες. Ο ιδανικός λόγος είναι 4:1 έως 1:1 αν και στις ΗΠΑ σήμερα ο λόγος αυτός είναι περίπου 10-20:1. Πάντως, σε πρόσφατη μελέτη, δεν δείχτηκαν σημαντικές διαφορές στους δείκτες φλεγμονής όταν επιτεύχθηκε λόγος ω6/ω3 1:1 με την προσθήκη στη δίαιτα μόνο a-λινολενικού οξέος (ALA; C18:3) φυτικής όμως προέλευσης (16, εικόνα 5).
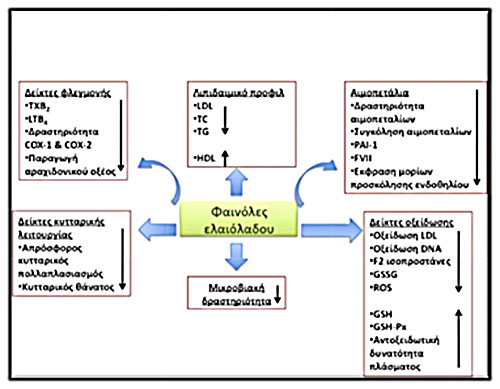
Εικόνα 5. Δράσεις των φαινολικών συστατικών του παρθένου ελαιόλαδου
Το είδος των λιπαρών οξέων των φωσφολιπιδίων της μεμβράνης των μακροφάγων και του ενδοθηλίου μπορεί να επηρεάσει τη μεταγευματική φλεγμονώδη αντίδραση. Τα κορεσμένα λιπαρά οξέα έχουν τη δυνατότητα άμεσης ενεργοποίησης προφλεγμονωδών αντιδράσεων μέσω των Toll-like υποδοχέων και προάγουν την έκφραση των προφλεγμονωδών γονιδίων στα μακροφάγα με μηχανισμό παρόμοιο με αυτόν των ενδοτοξινών (17).
Σημαντική είναι η αντιφλεγμονώδης δράση του ελαιόλαδου, αν και δεν είναι ακριβώς διευκρινισμένο αν αυτή οφείλεται στα μονοακόρεστα που περιέχει ή στα φαινολικά παράγωγα που υπάρχουν σ’ αυτό και ιδιαίτερα στο παρθένο και έξτρα παρθένο ελαιόλαδο.
Όλες οι μέχρι σήμερα μελέτες έχουν δείξει ότι αυτά τα φαινολικά παράγωγα ασκούν σημαντικές ευνοϊκές επιδράσεις σε μεγάλο αριθμό βιο δεικτών in vivo και in vitro (εικόνα 6, 18).
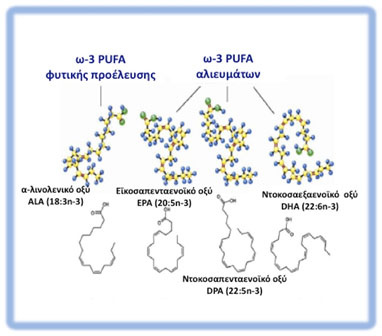
Εικόνα 6. Χημική δομή των ω-3 λιπαρών οξέων
Μέχρι σήμερα έχουν απομονωθεί 36 διαφορετικά είδη φαινολικών παραγώγων και όλα έχουν μεγάλη βιοδιαθεσιμότητα. Το είδος και η ποσότητα αυτών στο ελαιόλαδο εξαρτάται από:
- Την ποικιλία του ελαιόκαρπου
- Την περιοχή και τον τρόπο της καλλιέργειας
- Το βαθμό ωρίμανσης της ελιάς κατά τη συγκομιδή
- Το χρόνο από τη συγκομιδή μέχρι την εκχύλιση του ελαιόλαδου και τη μέθοδο που γίνεται αυτή
- Τον τρόπο μαγειρέματος
Συνοπτικά, οι δράσεις των φαινολικών παραγώγων στη χρόνια χαμηλής έντασης φλεγμονή είναι (19):
- Μείωση των επιπέδων στο πλάσμα των TXB2 (thromboxane B2) και LTB4 (leukotriene B4)
- Μείωση των επιπέδων της IL-6 και της CRP.
- Μείωση της σύνθεσης και έκκρισης του αραχιδονικού οξέος.
- Αναστολή της δραστηριότητας των COX-1 και COX-2 με απότοκο μείωση των εικοσανοειδών, των προσταγλανδινών και της θρομβοξάνης.
Το ερώτημα που υπάρχει σήμερα στη διεθνή βιβλιογραφία είναι το κατά πόσο είναι υπεύθυνα τα κορεσμένα λίπη για τη δημιουργία φλεγμονής και αθηρωμάτωσης και με πιο μηχανισμό (20). Η οξείδωση των PUFA και των υδατανθράκων προάγει την παραγωγή αλδεϋδών οι οποίες είναι γνωστό ότι προκαλούν ή επιβαρύνουν πολλά μη-μεταδοτικά νοσήματα (φλεγμονή, αθηρωμάτωση, καρκίνο, άσθμα, διαβήτη και δυσλειτουργία του ενδοθηλίου). Αντίθετα, τα κορεσμένα λίπη δεν έχουν αυτές τις ιδιότητες και πιθανότατα τα PUFA που συνυπάρχουν στις ίδιες τροφές προκαλούν τη νοσηρότητα που αποδίδεται σε αυτά. Μάλιστα, σε πρόσφατη μελέτη (21) σε παχύσαρκες γυναίκες με μεταβολικό σύνδρομο η χορήγηση δίαιτας υψηλή σε λιπαρά, αλλά με καλή ισορροπία SFA/MUFA/PUFA, είχε ως αποτέλεσμα τη μείωση του σωματικού λίπους, τη μείωση των δεικτών φλεγμονής (IL-1α, IL-1β, 1L-12, Il-17, IFNγ, TNFα, TNFβ) και βελτίωση της αγγειακής λειτουργίας (μείωση αρτ. πίεσης και PAI-1).
4. Υδατάνθρακες
Οι υδατάνθρακες καλύπτουν σήμερα παγκοσμίως το μεγαλύτερο ποσοστό των ενεργειακών αναγκών του ανθρώπου και σχεδόν το σύνολο των οργανισμών και σχεδόν όλες οι χώρες του κόσμου συστήνουν την πρόσληψη 4-11 μερίδων/ημερησίως δημητριακών και γενικά αμυλούχων τροφών (Ελλάδα: 8 μερίδες/ημ.), πάντα βέβαια μη-ραφιναρισμένα προϊόντα και ολικής άλεσης. Μία μερίδα ισοδυναμεί με 1 φέτα ψωμί (25 γρ.) ή ½ φλιτζάνι μαγειρεμένα ζυμαρικά ή ρύζι ή με 100 γρ. πατάτας. Αν στα παραπάνω προσθέσουμε και τους υδατάνθρακες των φρούτων, των λαχανικών, των οσπρίων, των γαλακτοκομικών, των γλυκών, των αναψυκτικών και το γλυκογόνο των πρωτεϊνούχων τροφών, θα δούμε ότι οι υδατάνθρακες καλύπτουν το 50-65% των ενεργειακών μας αναγκών.
Έχει δειχθεί ότι η αυξημένη πρόσληψη απλών σακχάρων έχει ως αποτέλεσμα την ενεργοποίηση φλεγμονωδών μεταβολικών οδών (22). Η χορήγηση γλυκόζης σε φυσιολογικά άτομα συνοδεύεται από αύξηση της παραγωγής υπεροξειδίων στα λευκοκύτταρα και στα μονοπύρηνα και αύξηση της δραστηριότητας του πυρηνικού παράγοντα kB (NF-kB) ο οποίος ελέγχει τη δραστηριότητα πολλών προφλεγμονωδών γονιδίων (23).
Αλλά και ο υψηλός γλυκαιμικός δείκτης των τροφών (ανάλογο στοιχείο με τα δεδομένα αυξημένης πρόσληψης απλών σακχάρων) και το αυξημένο γλυκαιμικό φορτίο (ΓΔ/ΓΦ) συνδέονται με αυξημένη θνησιμότητα, τόσο σε υγιή άτομα όσο και σε διαβητικούς, όπως έδειξαν μεγάλες προοπτικές μελέτες (24). Σε πρόσφατη μετα-ανάλυση, ενώ και πάλι αποδείχθηκε η αντιφλεγμονώδης δράση τροφών με χαμηλό ΓΔ/ΓΦ, δεν μπόρεσε να αποδειχθεί σαφής ευνοϊκή επίδραση από υδατανθρακούχες τροφές ολικής άλεσης (25).
Σήμερα υπάρχουν πολλοί και δικαιολογημένοι ενδοιασμοί για την κατανάλωση προϊόντων σίτου αλλά και άλλων δημητριακών ολικής άλεσης, όσον αφορά την ευνοϊκή τους επίδραση στη χρόνια χαμηλής έντασης φλεγμονή. Μάλιστα, πολλά βιβλιογραφικά δεδομένα σε πρόσφατη ανασκόπηση δείχνουν ότι αυτές οι τροφές αποτελούν συχνά και την αιτία του προβλήματος (26) και αναλυτικότερα:
Πολλές πρωτεΐνες που υπάρχουν στο σιτάρι και κυρίως η γλουτένη, αντιδρούν με τις IgE ανοσοσφαιρίνες και είναι δυνατόν να προκαλέσουν άσθμα του baker, ρινίτιδα, ουρτικάρια και αναφυλαξία μετά από άσκηση εξαρτώμενη από το σιτάρι (27). Επιπλέον, είναι γνωστή η αιτιολογική σχέση της γλουτένης με την κοιλιοκάκη και τη ερπητοειδή δερματίτιδα. Η στενή σχέση της δυσανεξίας στη γλουτένη με το διαβήτη 1 και η παρατήρηση ότι οι πάσχοντες από κοιλιοκάκη, καθώς και οι συγγενείς τους, πάσχουν συχνότερα από αυτοάνοσα νοσήματα, κάνουν ύποπτα πολλά δημητριακά για πρόκληση και πολλών άλλων συνδρόμων.
Τα ανοσο-τροποποιητικά πεπτίδια της γλιαδίνης ενεργοποιούν κάποια ειδικά Τ-λεμφοκύτταρα και προάγουν προφλεγμονώδεις αντιδράσεις, όχι μόνο σε πάσχοντες από δυσανεξία στη γλουτένη αλλά και σε υγιείς μάρτυρες. Για να επιδράσει η γλιαδίνη με τα κύτταρα του ανοσοποιητικού συστήματος θα πρέπει να διαπεράσει τον εντερικό φραγμό. Αυτό επιτυγχάνεται με παρακυτταρική μεταφορά, μια λειτουργία που μπορεί να γίνει μόνο όταν αυξηθεί η εντερική διαπερατότητα, κάτι που είναι δυνατόν να προκαλέσει η γλιαδίνη.
Μπορούμε λοιπόν να πούμε, όπως έδειξαν μελέτες in vivo και in vitro, ότι η γλιαδίνη και οι VGA’s (Wheat Germ Agglutinin) των δημητριακών αυξάνουν την εντερική διαπερατότητα και ενεργοποιούν το ανοσοποιητικό σύστημα. Οι μέχρι σήμερα επιδημιολογικές μελέτες, αλλά και μελέτες παρέμβασης, που εξέτασαν την επίδραση των δημητριακών ολικής άλεσης στην υγεία, είχαν σημαντικές επιδράσεις και από άλλους διατροφικούς παράγοντες αλλά και από το γενικότερο τρόπο ζωής των μελετηθέντων (26).
5. Προβιοτικά, πρεβιοτικά και αντιοξειδωτικά
5.1. Προβιοτικά
Ορισμός προβιοτικών: Ζωντανοί μικροοργανισμοί, οι οποίοι χορηγούμενοι σε θεραπευτικές δόσεις βελτιώνουν την υγεία του ξενιστή (28).
Τα κυρίως χρησιμοποιούμενα προβιοτικά είναι οι lactobacilli και τα bifidobacteria ανθρώπινης προέλευσης σε δόσεις 108 and 1010 cfu/ημέρα.
Οι δράσεις των προβιοτικών είναι άμεσες και έμμεσες, μέσω τροποποίησης της εντερικής χλωρίδας αλλά και της δραστηριότητας του ανοσοποιητικού συστήματος. Πολλά από τα προβιοτικά βακτηρίδια προσκολλώνται στο εντερικό επιθήλιο και εμποδίζουν την προσπέλαση παθογόνων μικρο-οργανισμών προς αυτό (29). Επίσης, τα προβιοτικά εμποδίζουν και την ανάπτυξη παθογόνων μικροοργανισμών μέσω της παραγωγής αντιμικροβιακών παραγόντων (30).
Η χορήγηση προβιοτικών έχει πολύ ικανοποιητικά αποτελέσματα στη θεραπεία των ιδιοπαθών φλεγμονωδών νόσων του εντέρου (31), αμφιλεγόμενα στη ρευματοειδή αρθρίτιδα (32), ικανοποιητικά στην ατοπική δερματίτιδα (33), και στους προδιαθεσικούς παράγοντες καρδιο-αγγειακών νόσων (34).
5.2. Πρεβιοτικά
Ορισμός πρεβιοτικών: Συστατικά των τροφών τα οποία δεν πέπτονται και έχουν θετική επίδραση στην ανάπτυξη ή στη δραστηριότητα κάποιων αποικιών της μικροβιακής εντερικής χλωρίδας με τελικό αποτέλεσμα τη βελτίωση της υγείας του ξενιστή. (35)
Τα απαραίτητα κριτήρια για το χαρακτηρισμό ενός διατροφικού συστατικού ως πρεβιοτικού είναι:
- Θα πρέπει να είναι ανθεκτικό στην επίδραση των γαστρικών υγρών και πεπτικών ενζύμων, ώστε να μη διασπάται και να μην απορροφάται, για να μπορεί να φτάσει ακέραιο και απόλυτα διαθέσιμο στη μικροβιακή χλωρίδα του παχέος εντέρου.
- Θα πρέπει να μπορεί να χρησιμοποιείται εκλεκτικά από κάποιες μόνο αποικίες (Bifidobacterium και Lactobacillus), ενώ αντίθετα θα πρέπει να μην επηρεάζει, ακόμα δε και να καταστέλλει την ανάπτυξη άλλων.
- Θα πρέπει να επιφέρει βελτίωση των δεικτών υγείας του ανθρώπου-ξενιστή.
Τα περισσότερο γνωστά, χρησιμοποιούμενα και δραστικά πρεβιοτικά είναι:
- Φρουκτάνες τύπου ινουλίνης. Βρίσκονται στο στάρι, στα κρεμμύδια, στο σκόρδο, στα χόρτα, στις αγκινάρες, στις μπανάνες και στις τομάτες (36). Η ινουλίνη και η παραγόμενη από αυτή ολιγοφρουκτόζη παράγονται σήμερα βιομηχανικά από τις ρίζες των ραδικιών και χρησιμοποιούνται ευρέως σε τρόφιμα όπως γαλακτοκομικά, κρεατοσκευάσματα, ποτά, αρτοσκευάσματα κτλ.
- Γαλακτο-ολιγοσακχαρίτες που συντίθενται ενζυματικά από τη λακτόζη.
- Άλλα υποψήφια μόρια με δράσεις πρεβιοτικών είναι: Η ισομαλτόζη, η λακτο-σακχαρόζη, οι ολιγοσακχαρίτες της σόγιας και οι ισομαλτο-ολιγοσακχαρίτες.
Εκτός από τα θετικά θεραπευτικά αποτελέσματα στα πειραματόζωα, τα πρεβιοτικά ασκούν και στον άνθρωπο σημαντική βελτίωση στις φλεγμονώδεις νόσους του εντέρου και στην ατοπική δερματίτιδα (37, 38, 39).
Τα πρεβιοτικά είναι πολύ χρήσιμοι βοηθητικοί παράγοντες στη θεραπεία της παχυσαρκίας αφού ευνοούν την πρόκληση κορεσμού (40), μειώνουν την έκκριση της ορεξιογόνου ορμόνης γκρελίνης και αυξάνουν την έκφραση του ανορεξιογόνου πεπτιδίου ΥΥ (41) και ταυτόχρονα τροποποιούν τη δραστηριότητα της λεπτίνης, που όπως είναι γνωστό ελέγχει το ενεργειακό ισοζύγιο (42).
Ευνοϊκή όμως είναι και η δράση τους στην πρόληψη ή και επιδείνωση του διαβήτη αφού επιβραδύνουν ή αναστέλλουν το σχηματισμό AGE’s (43).
5.3. Αντιοξειδωτικά
Τα αντιοξειδωτικά είναι χημικά μόρια τα οποία αναστέλλουν την οξείδωση άλλων χημικών μορίων. Τα οξειδωτικά μπορεί να προκαλέσουν βλάβη σε κυτταρικά στοιχεία του οργανισμού, π.χ. στα πολυακόρεστα λιπαρά οξέα της κυτταρικής μεμβράνης και στη συνέχεια τα οξειδωτικά μαζί με τους οξειδωμένους κυτταρικούς σχηματισμούς επιδρούν σε μεταγραφικές οδούς, όπως ο NF-kB, με τελικό αποτέλεσμα την παραγωγή φλεγμονωδών κυτταροκινών και εικοσανοειδών. Επομένως, ένας αποτελεσματικός μηχανισμός για τη μείωση της παραγωγής των διαμεσολαβητών της φλεγμονής είναι η πρόληψη του οξειδωτικού στρες.
Για να ελεγχθεί η αντι-οξειδωτική επάρκεια του οργανισμού μπορεί να γίνει μέτρηση στο αίμα των επιπέδων των βιταμινών, π.χ. βιταμίνη C, βιταμίνη Ε και η δραστηριότητα των αντι-οξειδωτικών ενζύμων. Επίσης, η δραστηριότητα του ενδογενούς μη-ενζυματικού αντι-οξειδωτικού συστήματος μπορεί να ελεγχθεί με τη μέτρηση της ολικής αντι-οξειδωτικής ικανότητας (Τotal antioxidant capacity – TAC), η οποία ορίζεται ως η ποσότητα σε moles των οξειδωτικών που αδρανοποιούνται από 1 λίτρο του υπό έλεγχο δείγματος (44). Έχει δειχθεί ότι η ενδογενής TAC επηρεάζεται ευνοϊκά από την κατανάλωση φυτικών τροφών (45), ενώ υπάρχει αντίστροφη συσχέτιση με τη θνησιμότητα από κάθε αιτία (46). Η διαπίστωση ότι η TAC έχει αρνητική και ανεξάρτητη συσχέτιση με τα επίπεδα της CRP σε μεγάλο αριθμό μη-διαβητικών ατόμων (47) αποδεικνύει τη σχέση του οξειδωτικού στρες με τη φλεγμονή και προφανώς, η διατροφική βελτίωση της TAC είναι μια πολύ καλή θεραπευτική προσέγγιση της χρόνιας φλεγμονής.
Οι κυριότερες αντι-οξειδωτικές ουσίες είναι:
- Βιταμίνες: Βιταμίνη Α και καροτινοειδή (α-καροτίνη, β-καροτίνη, καθαξανθίνη, λουτεΐνη, λυκοπένιο, ζεαξανθίνη), Βιταμίνη C, Βιταμίνη Ε
- Ορμόνες: Μελατονίνη
- Φαινόλες: Φλαβόνες, φλαβονόλες, φλαβονόνες, Στιλβενοειδή (ρεσβερατρόλη), ανθροκυανίνες
- Μη φλαβονοειδή φαινολικά παράγωγα: Κουρκουμίνη, φλαβονογλινάνες, ξανθόνες, ευγενόλη.
- Άλλα: καπσαϊσίνη, χολερυθρίνη, κιτρικό οξύ, οξαλικό οξύ, φυτικό οξύ, λιποϊκό οξύ, ουρικό οξύ.
Τροφές πλούσιες σε αντιοξειδωτικά είναι:
- Χορταρικά: Αγκινάρες, λάχανο, μπρόκολο, σπαράγγια, αβοκάντο, σπανάκι, τομάτες, παντζάρια, καρότα.
- Φρούτα: Πορτοκάλι, σύκα, δαμάσκηνα, φράουλες και όλα τα berries, κεράσια, μάνγκο, σταφύλια και ο χυμός τους καθώς και το κρασί, χυμός γκρέιπ-φρουτ
- Μπαχαρικά και μυρωδικά: Ρίγανη, κανέλα, θυμάρι, κύμινο, δυόσμος, βασιλικός, κάρι, πιπέρι, τζίντζερ, μουστάρδα, τσίλι, πάπρικα, σκόρδο, κρεμμύδι, κορίανδρος, κάρδαμο
- Αποξηραμένα φρούτα: Σταφίδες, σύκα, δαμάσκηνα, χουρμάδες, ροδάκινα, μήλα, αχλάδια, βερίκοκα.
- Ξηροί καρποί: Φιστίκια, αμύγδαλα, καρύδια, φουντούκια, κάσιους, μακαντέμια, φιστικοβούτυρο, κακάο και σοκολάτα.
6. Συμπεράσματα
Η σχέση της διατροφής με τη χρόνια χαμηλής έντασης φλεγμονή και τα γνωστά αλλά και άγνωστα νοσήματα που απορρέουν από αυτή είναι αναμφισβήτητη. Παρόλα αυτά, σπάνια χρησιμοποιούνται στην καθημερινή θεραπευτική διατροφικές προσεγγίσεις παρά τον τεράστιο όγκο των μέχρι σήμερα γνώσεων.
Από τα διατροφικά στοιχεία που αναφέρθηκαν παραπάνω, τα ω3-λιπαρά οξέα μακράς αλύσου, οι αντιοξειδωτικές βιταμίνες, τα φλαβονοειδή, τα προβιοτικά και τα πρεβιοτικά είναι δυνατόν να τροποποιήσουν την προδιάθεση στις χρόνιες φλεγμονώδεις νόσους, αλλά να έχουν και σημαντική συμμετοχή στη θεραπεία τους.
Από τα διατροφικά στοιχεία που η επιβαρυντική τους δράση είναι αναμφισβήτητη, τη πρώτη θέση έχει η αυξημένη κατανάλωση απλών σακχάρων και ω-6 λιπαρών οξέων. Τα κορεσμένα λίπη δε φαίνεται να έχουν την επιβαρυντική επίδραση που τους αποδίδεται μέχρι σήμερα, αν βέβαια καταναλώνονται σε σωστές αναλογίες, σε σχέση πάντα με τα άλλα είδη λίπους. Αλλά και η αυξημένη κατανάλωση σύνθετων υδατανθράκων και δημητριακών, ακόμα και ολικής άλεσης, δε φαίνεται να είναι τόσο “αθώα”, όσο πιστεύουμε.
Δεν πρέπει βέβαια να ξεχνάμε ότι οι παράγοντες που τροποποιούν το διατροφικό φλεγμονώδες ερέθισμα είναι πολλοί και έτσι πάντα χρειάζονται σύνθετοι υπολογισμοί πριν συστήσουμε κάποιο είδος διαιτητικής θεραπείας.
Βιβλιογραφία
- Wellen KE, Hotamisligil GS. Inflammation, stress, and diabetes. J.Clin.Invest. 2005;115:1111-19.
- Shoelson SE, Lee J, Goldfine AB. Inflammation and insulin resistance. J.Clin. Invest. 2006;116:1793-1801.
- ILSI Europe. A Consideration of Biomarkers to be used for Evaluation of Inflammation in Human Nutritional Studies. Br J Nutr, Januar 2013, Vol. 109 Suppl No. S1
- Calder P. C., Albers R, Antoine., J.-M., Blum S. et al. Br J Nutr, 2009, Vol. 101 Supplement No. S1
- Wooki Kim, Hyungjae Lee. Advances in Nutritional Research on Regulatory T-Cells. Nutrients 2013, 5, 4305-4315
- Hernández-Aguilera Α., Rull Α., Rodríguez-Gallego Ε. et al. Mitochondrial Dysfunction: A Basic Mechanism in Inflammation-Related Non-Communicable Diseases and Therapeutic Opportunities. Mediators of Inflammation, Volume 2013, Article ID 135698, 13 pages.
- Kontogianni MD, Panagiotakos DB, Pitsavos C et al. Relationship between meat intake and the development of acute coronary syndromes: the CARDIO2000 case-control study. Eur J Clin Nutr. 2008, 62(2):171-7.
- Feskens EJ, Sluik D, van Woudenbergh GJ. Meat consumption, diabetes, and its complications. Curr Diab Rep. 2013, 13(2):298-306.
- Pounis GD, Tyrovolas S, Antonopoulou M, et al. Long-term animal-protein consumption is associated with an increased prevalence of diabetes among the elderly: the Mediterranean Islands (MEDIS) study. Diabetes Metab. 2010, 36(6 Pt 1):484-90.
- Vallianou N.G, Bountziouka V.P, Georgousopoulou E. Influence of Protein Intake from Haem and Non-haem Animals and Plant Origin on Inflammatory Biomarkers among Apparently-healthy Adults in Greece. J HEALTH POPUL NUTR 2013, 31(4):446-454
- Montonen J , Boeing H, Fritsche A. et al. Consumption of red meat and whole-grain bread in relation to biomarkers of obesity, inflammation, glucose metabolism and oxidative stress. Eur J Nutr 2013, 52:337–345.
- Ley SH, Sun Q, Willett WC, Eliassen AH, et al. Associations between red meat intake and biomarkers of inflammation and glucose metabolism in women. Am J Clin Nutr. 2014, 99(2):352-60.
- Nappo F, Esposito K, Cioffi M, et al. Postprandial endothelial activation in healthy subjects and in type 2 diabetic patients: role of fat and carbohydrate meals. J Am Coll Cardiol 2002;39:1145–1450.
- Esposito K, Nappo F, Giugliano F, et al. Meal modulation of circulating interleukin 18 and adiponectin concentrations in healthy subjects and in patients with type 2 diabetes mellitus. Am J Clin Nutr 2003, 78:1135–1140.
- Trebble, T., Arden, N.K., Stroud, M.A. et al. Inhibition of tumour necrosis factor-α and interleukin 6 production by mononuclear cells following dietary fish-oil supplementation in healthy men and response to antioxidant co-supplementation. Br. J. Nutr. 2003, 90, 405–412.
- Enos R., Velazquez K., McClellan J. et al. Reducing the Dietary Omega-6:Omega-3 Utilizing a-Linolenic Acid; Not a Sufficient Therapy for AttenuatingHigh-Fat-Diet-Induced Obesity Development NorRelated Detrimental Metabolic and Adipose TissueInflammatory Outcomes. PLOS ONE , 2014 | Volume 9 | Issue 4
- Wong S.W.,Kwon M.J., Choi A.M. et al. Fatty acids modulate Toll-like receptor 4 activation through regulation of receptor dimerization and recruitment into lipid rafts in a reactive oxygen species-dependent manner. J. Biol. Chem. 2009, 284, 27384–27392.
- Cicerale, S., Conlan, X.A., Sinclair, A.J., Keast, R.S.J. Chemistry and health of olive oil phenolics. Crit. Rev. Food Sci. Nutr. 2009, 49, 218–236.
- Cicerale S, Lucas L, Keast R. Biological Activities of Phenolic Compounds Present in VirginOlive Oil. Int. J. Mol. Sci. 2010, 11, 458-479
- Glen D. Lawrence. Dietary Fats and Health: Dietary Recommendations in the Context of Scientific Evidence. Adv. Nutr. 2013, 4: 294–302
- Silver HJ, Kang H, Keil CD. et al. Consuming a balanced high fat diet for 16 weeks improves body composition, inflammation and vascular function parameters in obese premenopausal women. Metabolism. 2014, 63(4):562-73.
- Brown C.M., Dulloo,A.G., Montani, J.P. Sugary drinks in the pathogenesis of obesity and cardiovascular diseases. Int. J. Obes. (Lond.) 2008, 32, S28–S34.
- Dandona P, Aljada A, Chaudhuri A, Mohanty P, Garg R. Metabolic syndrome. A comprehensive perspective based on interactions between obesity, diabetes, and inflammation. Circulation 2005, 111:1448–1454.
- Burger KN, Beulens JW, van der Schouw YT, et al.Dietary fiber, carbohydrate quality and quantity, and mortality risk of individuals with diabetes mellitus.PLoS One. 2012, 7(8):e43127.
- Buyken AE, Goletzke J, Joslowski G et al .Association between carbohydrate quality and inflammatory markers: systematic review of observational and interventional studies. Am J Clin Nutr. 2014, 99(4):813-33.
- De Punder K. , Leo Pruimboom L. The Dietary Intake of Wheat and other Cereal Grains and Their Role in Inflammation. Nutrients 2013, 5, 771-787.
- Sapone A, Bai J.C, Ciacci C. et al. Spectrum of gluten-related disorders: Consensus on new nomenclature and classification. BMC Med. 2012, 10, doi:10.1186/1741-7015-10-13.
- FAO-WHO (2001) Joint FAO/WHO Expert Consultation on Health and Nutritional Properties of Probiotics in Food including Powder Milk with Live Lactic Acid Bacteria.
- Buck BL, Altermann E, Svingerud T, et al. Functional analysis of putative adhesion factors in Lactobacillus acidophilus NCFM. Appl Environ Microbiol 2005, 71, 8344–8351.
- Penner R, Fedorak RN & Madsen KL. Probiotics and nutraceuticals: non-medicinal treatments of gastrointestinal diseases. Curr Opin Pharmacol 2005, 5, 596–603.
- Furrie E, Macfarlane S, Kennedy A, et al. Synbiotic therapy (Bifidobacterium longum/Synergy 1) initiates resolution of inflammation in patients with active ulcerative colitis: a randomised controlled pilot trial. Gut 2005, 54, 242–249.
- Hatakka K, Martio J, Korpela M, et al. Effects of probiotic therapy on the activity and activation of mild rheumatoid arthritis – a pilot study. Scand J Rheumatol 2003, 32, 211–215.
- Rosenfeldt V, Benfeldt E, Nielsen SD, et al. Effect of probiotic Lactobacillus strains in children with atopic dermatitis. J Allergy Clin Immunol 2003, 111, 389–395.
- Naruszewicz M, Johansson ML, Zapolska-Downar D, et al. Effect of Lactobacillus plantarum 299v on cardiovascular disease risk factors in smokers. Am J Clin Nutr 2002, 76, 1249–1255.
- Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr 1995, 125, 1401–1412.
- Van Loo J, Coussement P, de Leenheer L, et al. On the presence of inulin and oligofructose as natural ingredients in the western diet. Crit Rev Food Sci Nutr 1995, 35, 525–552.
- Moro G, Arslanoglu S, Stahl B, et al. A mixture of prebiotic oligosaccharides reduces the incidence of atopic dermatitis during the first six months of age. Arch Dis Child 2006, 91, 814–819.
- Welters CF, Heineman E, Thunnissen FB, et al. Effect of dietary inulin supplementation on inflammation of pouch mucosa in patients with an ileal pouch-anal anastomosis. Dis Colon Rectum 2002, 45, 621–627.
- Casellas F, Borruel N, Torrejon A, et al. Oral oligofructose- enriched inulin supplementation in acute ulcerative colitis is well tolerated and associated with lowered faecal calprotectin. Aliment Pharmacol Ther 2007, 25, 1061–1067
- Cani PD, Joly E, Horsmans Y, Delzenne NM: Oligofructose promotes satiety in healthy human: a pilot study. Eur J Clin Nutr 2006, 60(5):567–572.
- Parnell JA, Reimer RA: Weight loss during oligofructose supplementation is associated with decreased ghrelin and increased peptide YY in overweight and obese adults. Am J Clin Nutr 2009, 89(6):1751–1759.
- Macfarlane GT, Macfarlane S: Fermentation in the human large intestine: its physiologic consequences and the potential contribution of prebiotics. J Clin Gastroenterol 2011, 45(Suppl):S120–S127.
- Kellow N.J, Melinda T Coughlan M.T, et al. BMC Endocrine Disorders 2014, 14:55
- Serafini M, Del RD. Understanding the association between dietary antioxidants, redox status and disease: is theTotal Antioxidant Capacity the right tool? Redox Rep 2004, 9,145–152.
- Serafini M, Bugianesi R, Maiani G, et al. Plasma antioxidants from chocolate. Nature 2003, 424, 1013.
- Agudo A, Cabrera L, Amiano P, et al. Fruit and vegetable intakes, dietary antioxidant nutrients, and total mortality in Spanish adults: findings from the Spanish cohort of the European Prospective Investigation into Cancer and Nutrition (EPIC-Spain). Am J Clin Nutr 2007, 85, 1634–1642.
- Brighenti F, Valtuena S, Pellegrini N, et al. Total antioxidant capacity of the diet is inversely and independently related to plasma concentration of high-sensitivity C-reactive protein in adult Italian subjects. Br J Nutr 2005, 93, 619–625.
Created: February 25, 2015
Last update: February 25, 2015