Βασιλάτου Ευαγγελίνα
Ενδοκρινολόγος, Επιμελήτρια Α΄, Ενδοκρινολογική Μονάδα,
Β΄ Προπαιδευτική Παθολογική Κλινική, Πανεπιστημιακό Νοσοκομείο «ΑΤΤΙΚΟΝ»
Ιωάννα Τζαβάρα
Ιωάννα Τζαβάρα, Διευθύντρια Ενδοκρινολογικού Τμήματος Γενικού Νοσοκομείου «Α. ΦΛΕΜΙΓΚ»
Εις μνήμην Ι. Τζαβάρα
1. Ορισμός
Ο όζος θυρεοειδούς αποτελεί μία εστιακή βλάβη του θυρεοειδικού παρεγχύματος, η οποία μπορεί να διαπιστωθεί κατά την κλινική εξέταση ή/και με απεικονιστικές μεθόδους. Η παρουσία μονήρους ή πολλαπλών όζων στο θυρεοειδικό παρέγχυμα χαρακτηρίζει την οζώδη θυρεοειδική νόσο. Οζώδης θυρεοειδική νόσος παρατηρείται είτε σε θυρεοειδή αδένα φυσιολογικού μεγέθους είτε σε διογκωμένο θυρεοειδή αδένα (βρογχοκήλη).
2. Επιδημιολογία
Η παρουσία εστιακών βλαβών στους ενδοκρινείς αδένες είναι συχνή, με πρώτο στην συχνότητα τον θυρεοειδή αδένα. Οι όζοι θυρεοειδούς που διαπιστώνονται κλινικά κατά την αντικειμενική εξέταση αποτελούν μικρό ποσοστό των υπαρχόντων όζων, όπως διαπιστώθηκε, αρχικά σε νεκροτομικές μελέτες και στην συνέχεια με απεικονιστικές μεθόδους (1) κατά την διάρκεια του εικοστού αιώνα. Αποτελούν επομένως συχνό εύρημα στην καθημερινή κλινική πράξη, κυρίως λόγω της αυξανόμενης χρήσης απεικονιστικών εξετάσεων και της συνεχούς τεχνολογικής βελτίωσης των απεικονιστικών μεθόδων.
Οι όζοι θυρεοειδούς είναι συχνότεροι στις γυναίκες και στους ηλικιωμένους (2). Επίσης, οι όζοι θυρεοειδούς είναι συχνότεροι σε γεωγραφικές περιοχές με ιωδοπενία (2). Επομένως υπάρχει μεγάλη διακύμανση στην συχνότητα των όζων θυρεοειδούς στις διάφορες μελέτες ανάλογα με τον πληθυσμό της μελέτης (ηλικία, φύλο, πρόσληψη ιωδίου) και την μέθοδο ανίχνευσης των όζων (ψηλάφηση, απεικονιστικές μέθοδοι). Σε γεωγραφικές περιοχές με επάρκεια ιωδίου η συχνότητα των όζων θυρεοειδούς ως ψηλαφητικό εύρημα κυμαίνεται σε ποσοστό 3-7%, ως εύρημα υπερηχογραφικού ελέγχου σε ποσοστό 19-67% σε μη επιλεγμένο πληθυσμό (3-7), ενώ ως νεκροτομικό εύρημα είναι περίπου 50% (2,8). Η δε ετήσια επίπτωση των όζων θυρεοειδούς στις Ηνωμένες Πολιτείες, περιοχή με επάρκεια ιωδίου, εκτιμάται στο 0,1 % (2,9).
3. Διαφορική διάγνωση
Η διαπίστωση ψηλαφητής τραχηλικής διόγκωσης στην ανατομική περιοχή του θυρεοειδούς συνήθως αφορά κολλοειδή όζο, θυρεοειδική κύστη, εστιακή φλεγμονή ή εστιακή θυρεοειδίτιδα (~80% των περιπτώσεων) (1,9). Σπανιώτερα μπορεί να αφορά ένα καλόηθες θυλακιοκυτταρικό νεόπλασμα. (10-15% των περιπτώσεων) (1,2,9). Σε ποσοστό ~5% των περιπτώσεων μπορεί να αφορά ένα πρωτοπαθές κακόηθες νεόπλασμα του θυρεοειδούς (1,2,9,10), συνήθως θυλακιοκυτταρικό καρκίνωμα και σπανιώτερα μυελοειδές καρκίνωμα, αναπλαστικό καρκίνωμα, πρωτοπαθές λέμφωμα θυρεοειδούς ή σάρκωμα (10). Σπανίως μπορεί να πρόκειται για μετάσταση στον θυρεοειδή αδένα, όπου στην πλειοψηφία των περιπτώσεων η πρωτοπαθής εστία έχει ήδη διαγνωστεί (10). Τέλος, έχουν περιγραφεί περιπτώσεις στις οποίες η τραχηλική διόγκωση μπορεί να αφορά διόγκωση του υπάρχοντος θυρεοειδικού λοβού σε περιπτώσεις ημιαγενεσίας του θυρεοειδούς ή να προέρχεται από τους παραθυρεοειδείς αδένες (αδένωμα παραθυρεοειδών ή κύστη και πολύ σπάνια καρκίνωμα παραθυρεοειδών) (11).
4. Κλινική εικόνα
Οι όζοι θυρεοειδούς συνήθως εκδηλώνονται ως ασυμπτωματική τραχηλική διόγκωση στην ανατομική περιοχή του θυρεοειδούς, η οποία μπορεί να γίνει αντιληπτή από τον ίδιο τον ασθενή ή/και να διαπιστωθεί από τον ιατρό κατά την αντικειμενική εξέταση (Εικόνα 1, Εικόνα 2). Ωστόσο, υπάρχει πληθώρα μελετών που έχουν δείξει ότι η κλινική εξέταση αποτελεί την λιγώτερο ευαίσθητη μέθοδο για την ανίχνευση των θυρεοειδικών όζων (1, 8, 9). Όζοι διαμέτρου μικρότεροι από 1,0cm καθώς και όζοι που προβάλλουν στην οπίσθια επιφάνεια του θυρεοειδούς δεν ψηλαφώνται (10). Επίσης, έχει δειχθεί ότι σε ποσοστό 20-48% των ασθενών με ψηλαφητούς όζους θυρεοειδούς διαπιστώνονται επιπλέον όζοι, συνήθως μικρότεροι, κατά τον υπερηχογραφικό έλεγχο (2, 6). Επιπλέον, έχει δειχθεί ότι υπάρχει μεγάλη διακύμανση στην ανίχνευση όζων με την ψηλάφηση μεταξύ των εξεταστών (13) αλλά και στον ίδιο εξεταστή σε διαφορετικές χρονικές στιγμές.

Εικόνα 1. Ευμεγέθης πολυοζώδης βρογχοκήλη σε γυναίκα μέσης ηλικίας (F + P).
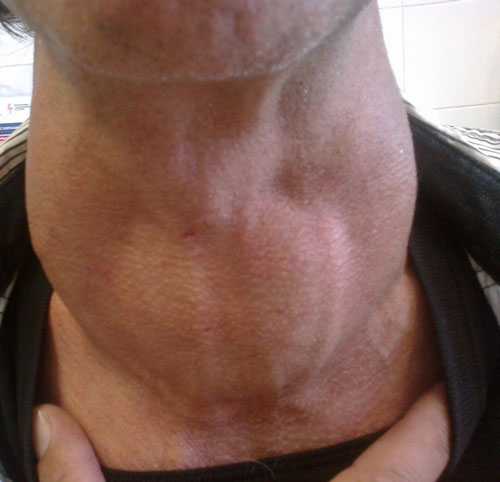
Εικόνα 2. Ευμεγέθης πολυοζώδης βρογχοκήλη σε άνδρα μέσης ηλικίας.
Η παρουσία επώδυνης τραχηλικής διόγκωσης θέτει την υπόνοια αιμορραγίας στο εσωτερικό κύστης θυρεοειδούς ή θυρεοειδίτιδος είτε θυρεοειδικού αποστήματος. Πιεστικά φαινόμενα από το ανώτερο αναπνευστικό, βράγχος φωνής ή/και δυσκαταποσία θέτουν την υπόνοια κακοήθους εξεργασίας, ιδίως αν συνδυάζονται με ταχεία αύξηση ανώδυνης συνήθως τραχηλικής διόγκωσης. Ωστόσο, πιεστικά φαινόμενα μπορεί να παρατηρηθούν και σε περιπτώσεις ευμεγέθους οζώδους βρογχοκήλης, ιδίως αν αυτή καταδύεται στην θωρακική κοιλότητα (10).
Η διαπίστωση τραχηλικής διόγκωσης μερικώς ή πλήρως καθηλωμένης στις γειτονικές ανατομικές δομές καθώς και η πολύ αυξημένη σύσταση ή σκληρία αυτής θέτουν την υπόνοια κακοήθους εξεργασίας. Επίσης, η διαπίστωση ψηλαφητών τραχηλικών λεμφαδενικών διογκώσεων, είτε ομόπλευρα με τον ψηλαφώμενο όζο είτε αμφοτερόπλευρα, αποτελεί έμμεση ένδειξη κακοήθους εξεργασίας (10).
Σε περίπτωση που οι όζοι θυρεοειδούς συνδυάζονται με διαταραχή της θυρεοειδικής λειτουργίας μπορεί ο ασθενής να αναφέρει συμπτώματα υπερ- ή υποθυρεοειδισμού και κατά την αντικειμενική εξέταση να διαπιστώνονται σημεία υπερ- ή υποθυρεοειδισμού, αντιστοίχως.
5. Θυρεοειδικά τυχαιώματα (incidentalomas)
Θυρεοειδικό τυχαίωμα αποτελεί κάθε μη ψηλαφητός όζος θυρεοειδούς, του οποίου η παρουσία αποκαλύπτεται σε απεικονιστικό έλεγχο θυρεοειδούς είτε στην ιστολογική εξέταση του παρακευάσματος θυρεοειδεκτομής ή σε νεκροτομικό υλικό (12).
Το υπερηχογράφημα αποτελεί την συχνότερη μέθοδο ανίχνευσης των τυχαίως διαπιστούμενων θυρεοειδικών όζων, δεδομένης της ολοένα αυξανόμενης εφαρμογής υπερηχογραφικού ελέγχου, της υψηλής ευαισθησίας και ειδικότητας της μεθόδου στην ανίχνευση θυρεοειδικών όζων και της συνεχούς τεχνολογικής εξέλιξης των υπερηχογράφων (14). Ακολουθούν από πλευράς συχνότητας άλλες απεικονιστικές μέθοδοι, με τελευταία την τομογραφία εκπομπής ποζιτρονίων (positron emission tomography, PET) με δεσοξυ-διφθορο-γλυκόζη (2-deoxy-2(18F)fluoro-D-glucose, 18FDG). Η συχνότητα ανεύρεσης θυρεοειδικών τυχαιωμάτων με PET-scan, ως εστιακή πρόσληψη στον θυρεοειδή, εκτιμάται σε ποσοστό ~2% των ασθενών που υποβάλλονται στην ανωτέρω εξέταση. Σημαντικό ποσοστό (27 – 42%) των τυχαιωμάτων αυτών αφορούν καρκίνο θυρεοειδούς, με συχνότερο ιστολογικό τύπο το θηλώδες καρκίνωμα (15,16).
6. Διαγνωστική διερεύνηση
Η διαπίστωση ενός ή περισσοτέρων όζων θυρεοειδούς σε έναν ασθενή είτε κατά την κλινική εξέταση είτε με απεικονιστικές μεθόδους, θέτει δύο ερωτήματα στον κλινικό ιατρό. Το ένα αφορά στην λειτουργική δραστηριότητα του ή των όζων και κατ’ επέκταση το ενδεχόμενο η παρουσία τους να επηρρεάζει την θυρεοειδική λειτουργία και το άλλο αφορά στο ενδεχόμενο κακοηθείας.
6.1. Διερεύνηση λειτουργικής δραστηριότητας
Ο έλεγχος της λειτουργικής δραστηριότητας των όζων θυρεοειδούς περιλαμβάνει αρχικά τον προσδιορισμό των θυρεοειδικών ορμονών και της θυρεοειδοτρόπου ορμόνης (TSH). Εφ’ όσον διαγνωστεί υπερθυρεοειδισμός ακολουθεί σπινθηρογράφημα θυρεοειδούς με Tc99 το οποίο μπορεί να αναδείξει την παρουσία τοξικού αδενώματος ή θερμού όζου ή οζώδους βρογχοκήλης με θερμές και ψυχρές περιοχές (Εικόνες 3 – 5). Η τελευταία περιπτώση συνήθως συνδιάζεται με υποκλινικό υπερθυρεοειδισμό. Το σπινθηρογράφημα θυρεοειδούς έχει επίσης ένδειξη σε περιπτώσεις ευθυρεοειδισμού επί παρουσίας ευμεγέθων όζων ή ευμεγέθους πολυοζώδους βρογχοκήλης, για την ανάδειξη αυτονομίας, κυρίως σε ιωδοπενικές περιοχές, καθώς και σε οζώδεις βρογχοκήλες με τάση «καταδύσεως» προς την θωρακική κοιλότητα (17,18). Στις περιπτώσεις αυτές λεπτομερέστερη εκτίμηση του μεγέθους της θυρεοειδικής διόγκωσης και του βαθμού καταδύσεως στην θωρακική κοιλότητα μπορεί να γίνει και με την αξονική τομογραφία τραχήλου και θώρακος (18) (Εικόνα 6).
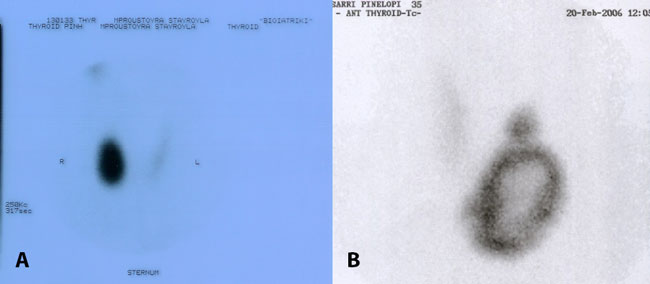
Εικόνα 3. α) Τοξικό αδένωμα και β) Τοξικό αδένωμα με κυστική εκφύλιση.
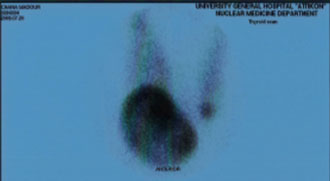
Εικόνα 4. Ευμεγέθης θερμός όζος στον ένα λοβό και μικρός θερμός όζος στον κάτω πόλο του άλλου λοβού.
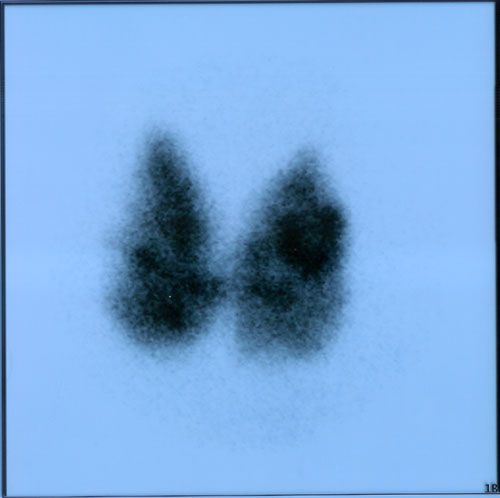
Εικόνα 5. Τοξική οζώδης βρογχοκήλη.
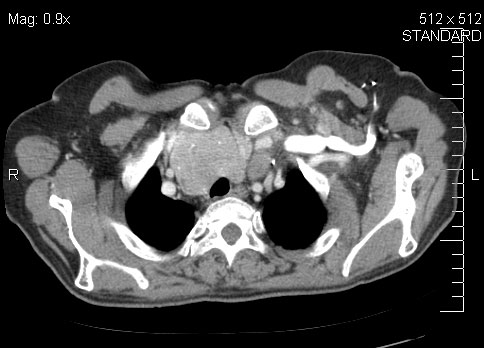
Εικόνα 6. Καταδυομένη στην θωρακική κοιλότητα βρογχοκήλη σε CT-θώρακος (εγκάρσια τομή).
6.2. Διερεύνηση πιθανής κακοηθείας
Η διερεύνηση πιθανής κακοηθείας των όζων θυρεοειδούς βασίζεται στα εξής: ατομικό και κληρονομικό ιστορικό ασθενούς, κλινική εξέταση, εργαστηριακός έλεγχος, απεικονιστικός έλεγχος και επιλεκτικά παρακέντηση με λεπτή βελόνα (FNA) (18). Πρέπει να σημειωθεί ότι τόσο οι όζοι που διαπιστώνονται μόνο υπερηχογραφικά όσο και οι ψηλαφητοί όζοι με παρόμοιο μέγεθος, έχουν την ίδια πιθανότητα κακοηθείας (10,18).
6.2.1. Ατομικό και κληρονομικό αναμνηστικό
Από το ατομικό αναμνηστικό πολύ σημαντικό στοιχείο αποτελεί το ιστορικό έκθεσης σε ιονίζουσα ακτινοβολία, ιδίως κατά την παιδική και εφηβική ηλικία, είτε από το περιβάλλον (κυρίως λόγω πυρηνικού ατυχήματος και σπανιώτερα λόγω πυρηνικών δοκιμών, ακόμη δε σπανιώτερα λόγω επαγγελματικής έκθεσης όταν δεν λαμβάνονται τα απαραίτητα μέτρα προστασίας) είτε λόγω θεραπευτικής χορήγησης (19). Λαμβάνεται επίσης υπ’ όψιν το ιστορικό κακοήθους νοσήματος. Συμπτώματα όπως ταχεία αύξηση μεγέθους ανώδυνης συνήθως τραχηλικής διόγκωσης, πιεστικά φαινόμενα από το ανώτερο αναπνευστικό, βράγχος φωνής ή/και δυσκαταποσία θέτουν την υπόνοια κακοήθους εξεργασίας, όπως αναφέρθηκε και προηγουμένως.
Από το κληρονομικό ιστορικό θα πρέπει να διευκρινίζεται η περίπτωση ύπαρξης συγγενούς με κακόηθες νόσημα θυρεοειδούς είτε ως μεμονωμένη εκδήλωση είτε στα πλαίσια νεοπλασματικών συνδρόμων. Το οικογενές θηλώδες καρκίνωμα θυρεοειδούς εκτιμάται σε ποσοστό 3 – 5% των ασθενών με θηλώδες καρκίνωμα και είναι συνήθως μεμονωμένο. Για να θεωρηθεί ως οικογενές θα πρέπει να υπάρχουν τουλάχιστον δύο συγγενείς με θηλώδες καρκίνωμα. Σπανίως, το οικογενές θυλακιοκυτταρικό καρκίνωμα αποτελεί εκδήλωση νεοπλασματικών συνδρόμων όπως πχ. η οικογενής πολύπωση παχέος εντέρου και το σύνδρομο Gardner που αποτελεί υπότυπο αυτής και οφείλονται σε αδρανοποιητικές μεταλλάξεις του ογκοκατασταλτικού γονιδίου APC (adenomatous polyposis coli), η νόσος Cowden που οφείλεται σε αδρανοποιητικές μεταλλάξεις του ογκοκατασταλτικού γονιδίου PTEN (phosphatase and tensin homologue) κλπ. (20). Αντιθέτως το οικογενές μυελοειδές καρκίνωμα θυρεοειδούς είναι πολύ συχνότερο καθώς εκτιμάται στο 20-25% των ασθενών με μυελοειδές καρκίνωμα, είτε στα πλαίσια νεοπλασματικών συνδρόμων (σύνδρομο πολλαπλής ενδοκρινικής νεοπλασίας τύπου 2 (ΜΕΝ 2Α & 2Β)), είτε ως μεμονωμένο οικογενές μυελοειδές (familial medullary thyroid cancer, FMTC), για το οποίο παραμένει αδιευκρίνιστο το ενδεχόμενο να αποτελεί κλινική παραλλαγή του συνδρόμου ΜΕΝ 2Α (χωρίς την εκδήλωση φαιοχρωμοκυττώματος ή / και πρωτοπαθούς υπερπαραθυρεοειδισμού (21).
6.2.2. Κλινική εικόνα
Από την κλινική εξέταση υπόνοια κακοηθείας τίθεται όταν η τραχηλική διόγκωση είναι μερικώς ή πλήρως καθηλωμένη στις γειτονικές ανατομικές δομές ή/και όταν παρουσιάζει πολύ αυξημένη σύσταση ή σκληρία ή/και όταν συνοδεύεται από την παρουσία ψηλαφητών τραχηλικών λεμφαδένων, όπως προαναφέρθηκε. Επίσης, πρέπει να σημειωθεί ότι το φύλο και η ηλικία έχουν σημασία, καθώς όζοι θυρεοειδούς στους άνδρες, σε παιδιά ή εφήβους καθώς και σε ηλικιωμένους έχουν αυξημένη πιθανότητα να είναι κακοήθεις (22). Ωστόσο, πρέπει να επισημανθεί ότι οι περισσότεροι ασθενείς με όζους θυρεοειδούς είναι ασυμπτωματικοί και με ελεύθερο ατομικό και κληρονομικό αναμνηστικό.
6.2.3. Εργαστηριακός έλεγχος
Ο εργαστηριακός έλεγχος έχει μικρή συμβολή στην διερεύνηση πιθανής κακοηθείας των όζων θυρεοειδούς. Υπάρχουν μελέτες που έχουν δείξει ότι τα επίπεδα TSH συχετίζονται με τον θυλακιοκυτταρικό καρκίνο σε ασθενείς με όζους θυρεοειδούς (23-25), ωστόσο τα δεδομένα δεν είναι επαρκή για να θεωρηθεί ως δείκτης για το συγκεκριμμένο νεόπλασμα. Επομένως, οι συστάσεις των Επιστημονικών Εταιρειών Θυρεοειδούς (Ευρωπαϊκή Ένωση Θυρεοειδούς (European Thyroid Association, ETA) (26), Αμερικανική Ένωση Θυρεοειδούς (American Thyroid Association, ATA) (27)) περιορίζονται στον προσδιορισμό TSH στα πλαίσια ελέγχου της λειτουργικής δραστηριότητας της οζώδους θυρεοειδικής νόσου. Ο προσδιορισμός της βασικής τιμής καλσιτονίνης ορού επιτρέπει την προεγχειρητική διάγνωση του μυελοειδούς καρκινώματος με μεγαλύτερη ακρίβεια από την παρακέντηση με λεπτή βελόνα (FNA) (28-30) και εφαρμόζεται στην καθημερινή κλινική πράξη για την διερεύνηση των όζων θυρεοειδούς σε αρκετά κέντρα. Ωστόσο δεν υπάρχει διεθνώς ομοφωνία για την σχέση κόστους / οφέλους για την συγκεκριμμένη πρακτική στην διάγνωση του μυελοειδούς καρκινώματος, γι’ αυτό και δεν έχει συμπεριληφθεί ως έλεγχος ρουτίνας για την διερεύνηση των όζων θυρεοειδούς στις συστάσεις της Αμερικανικής Ένωσης Θυρεοειδούς (27), ούτε της πλέον πρόσφατης διεταιρικής συνεργασίας τριών Επιστημονικών Εταιρειών (την Αμερικανική Ένωση Κλινικών Ενδοκρινολόγων (American Association of Clinical Endocrinologists, AACE), την Ιταλική Ένωση Κλινικών Ενδοκρινολόγων (Associazione Medici Endocrinologi, AME) και ETA (AACE/AME/ETA) (31). Αντιθέτως, στις συστάσεις όλων των Επιστημονικών Εταιρειών τονίζεται ότι ο προσδιορισμός της θυρεοσφαιρίνης ορού δεν έχει καμμία θέση στην διερεύνηση πιθανής κακοηθείας των όζων θυρεοειδούς, καθώς η θυρεοσφαιρίνη ορού αποτελεί δείκτη μετεγχειρητικής παρακολούθησης του θυλακιοκυτταρικού θυρεοειδικού καρκίνου (26,27,31).
6.2.4. Απεικονιστικός έλεγχος
Όλοι οι ασθενείς με γνωστή ή πιθανολογούμενη οζώδη θυρεοειδική νόσο θα πρέπει να υποβάλλονται σε υπερηχογάφημα θυρεοειδούς σύμφωνα με τις συστάσεις όλων των Επιστημονικών Εταιρειών (26,27,30), καθώς αποτελεί τον απεικονιστικό έλεγχο εκλογής για την διερεύνηση των όζων. Το υπερηχογράφημα χαρακτηρίζεται από υψηλή ευαισθησία και ειδικότητα στην διάγνωση των όζων, ευκολία εξέτασης και χαμηλό κόστος (5,10,18).
Το υπερηχογράφημα καθορίζει την θέση, το μέγεθος και τα υπόλοιπα χαρακτηριστικά (σχήμα, όρια, σύσταση, ηχογένεια, αγγείωση, παρουσία αποτιτανώσεων) του ή των όζων και του λοιπού θυρεοειδικού παρεγχύματος καθώς και τα χαρακτηριστικά των λεμφαδένων στην περίπτωση της τραχηλικής λεμφαδενοπάθειας (32). Οι όζοι διακρίνονται υπερηχογραφικά ως προς την σύσταση τους σε συμπαγείς (όταν το κυστικό στοιχείο απουσιάζει ή είναι ελάχιστο), σε μεικτούς (όταν συνυπάρχει κυστικό και συμπαγές στοιχείο) και σε κυστικούς (όταν κυριαρχεί το κυστικό στοιχείο). Οι αμιγώς κυστικοί όζοι και οι μικροί (διαμέτρου <2,0cm) σπογγόμορφοι όζοι (πολλαπλοί κυστικοί χώροι στο εσωτερικό του όζου, που χωρίζονται από λεπτά διαφραγμάτια) (Εικόνα 7) θεωρούνται καλοήθεις (32-34). Οι όζοι διακρίνονται ως προς την ηχογένεια σε υπερηχογενείς, ισόηχους, υπόηχους και άνηχους (λόγω παρουσίας υγρού – κυστικές βλάβες) συγκριτικά με το φυσιολογικό θυρεοειδικό παρέγχυμα (το οποίο είναι υπερηχογενές συγκριτικά με τους τραχηλικούς μυς) (32-34). Εναποθέσεις ασβεστίου παρατηρούνται στο ~30% των όζων και διακρίνονται σε μικροαποτιτανώσεις (Εικόνα 8), μακροαποτιτανώσεις και περιφερικές εναποθέσεις ασβεστίου εν είδη κελύφους αυγού (eggshell calcifications) (Εικόνα 9) (32-34). Η περιφερική άλως αποτελεί υπερηχογραφικό χαρακτηριστικό που παρατηρείται στους μισούς περίπου όζους, ως δακτυλιοειδής υποηχογένεια που μπορεί να περιβάλλει πλήρως ή ατελώς έναν όζο (Εικόνα 10) (32-34). Θεωρείται ότι προκύπτει από την συμπίεση των αιμοφόρων αγγείων γύρω από τον όζο και ενδεχομένως από την ανάπτυξη χρόνιας φλεγμονώδους διεργασίας και συνδετικού ιστού γύρω από τον όζο (34). Η παρουσία λεπτής, ομαλής άλω σε έναν όζο θεωρείται ενδεικτική καλοήθειας. Το υπερηχογράφημα δίνει πληροφορίες και για την αγγείωση των όζων με το έγχρωμο Doppler ροής, η οποία μπορεί να απουσιάζει σε κυστικούς όζους, να αφορά κυρίως την περιφέρεια του όζου ή να κυριαρχεί στο εσωτερικό του όζου (32,34). Υπερηχογραφικά χαρακτηριστικά του ή των όζων που συνηγορούν για κακοήθεια είναι τα εξής: υποηχογένεια, αυξημένη εσωτερική αγγείωση όζου, ανώμαλα και ασαφή όρια όζου, παρουσία μικροαποτιτανώσεων και απουσία περιφερικής άλω (32- 34). Επειδή κανένα υπερηχογραφικό χαρακτηριστικό δεν παρουσιάζει ικανοποιητική προγνωστική αξία για το ενδεχόμενο κακοηθείας, έχουν προταθεί συστήματα ταξινόμησης με βάση τον συνδυασμό υπερηχογραφικών χαρακτηριστικών των όζων για την καλύτερη εκτίμηση του κινδύνου κακοηθείας (35-37).
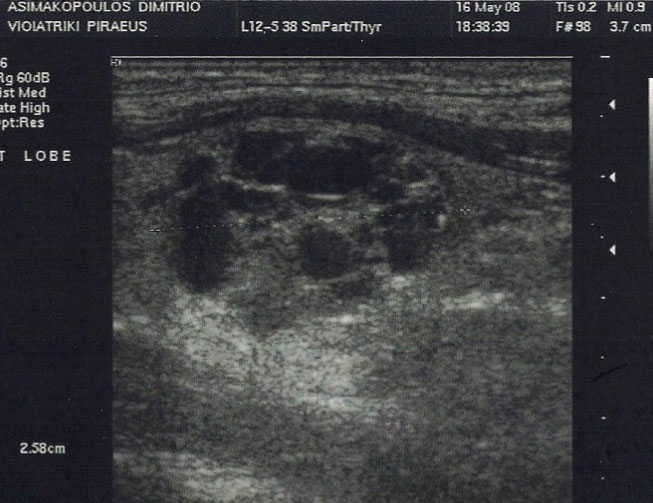
Εικόνα 7. Σπογγόμορφος όζος.
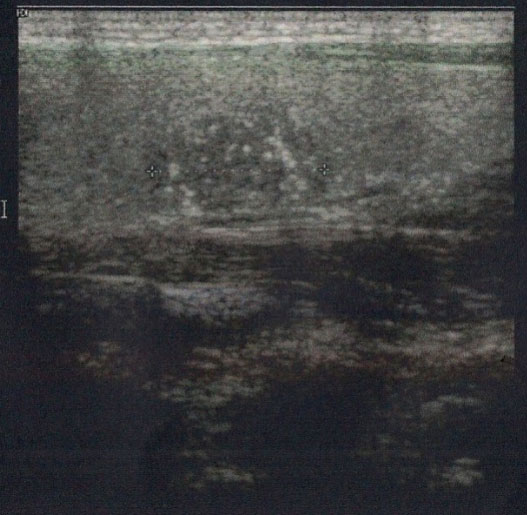
Εικόνα 8. Όζος με μικροαποτιτανώσεις.
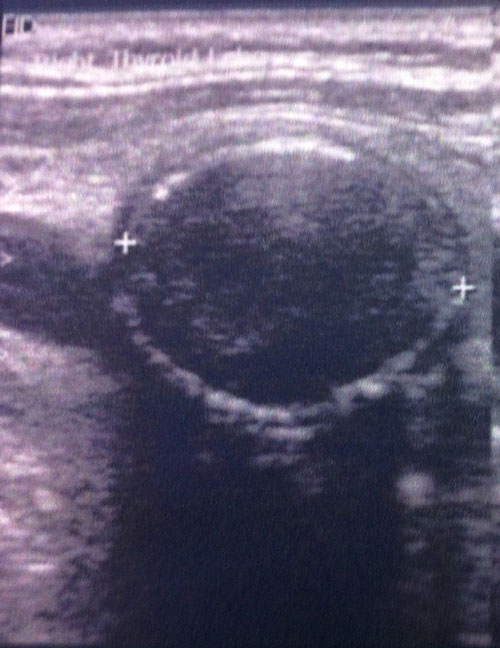
Εικόνα 9. Όζος με περιφερικές εναποθέσεις ασβεστίου εν είδη κελύφους αυγού (eggshell calcifications).

Εικόνα 10. α) Υπόηχη άλως περιβάλλουσα ατελώς έναν συμπαγή όζο και β) πλήρως έναν όζο μεικτής υφής (παρουσία μικροκυστικών στοιχείων).
Η ελαστογραφία, η οποία έχει αναπτυχθεί τελευταία, αποτελεί υπερηχογραφική τεχνική που επιτρέπει την εκτίμηση του βαθμού ακαμψίας ενός οργάνου ή ιστού (38). Δεδομένου ότι οι κακοήθεις εξεργασίες παρουσιάζουν σημαντικού βαθμού ακαμψία, η ελαστογραφία έχει θέση στην διάκριση μεταξύ καλοήθων και κακοήθων εξεργασιών σε διάφορα όργανα μεταξύ των οποίων συμπεριλαμβάνεται και ο θυρεοειδής (39,40). Χαρακτηρίζεται από υψηλή ευαισθησία και ειδικότητα για την εκτίμηση του κινδύνου κακοηθείας όζων θυρεοειδούς (41), με την προϋπόθεση ότι ο εξεταζόμενος όζος είναι συμπαγής και δεν παρουσιάζει αδρές αποτιτανώσεις (40).
Το σπινθηρογράφημα με Tc99 το οποίο κυριάρχησε ως απεικονιστική μέθοδος για την διερεύνηση των όζων θυρεοειδούς μέχρι την δεκαετία του ’80 έχει πλέον περιοριστεί σε ασθενείς με οζώδη θυρεοειδική νόσο και υποκλινικό ή κλινικό υπερθυρεοειδισμό (26,27), καθώς και για την ανάδειξη αυτονομίας (θερμών περιοχών) σε ευθυρεοειδικούς ασθενείς με πολυοζώδεις βρογχοκήλες, κυρίως σε ιωδοπενικές περιοχές (31). Όπως έχει δειχθεί σε πληθώρα παλαιοτέρων μελετών οι θερμοί όζοι σπανίως είναι κακοήθεις, σε αντίθεση με τους ψυχρούς όζους όπου η πιθανότητα κακοηθείας αναφέρεται σε ποσοστό 3%-16% (7,22,42). Η προγνωστική αξία του σπινθηρογραφήματος με Tc99 στην εκτίμηση της κακοηθείας είναι χαμηλή δεδομένου του μικρού ποσοστού κακοηθείας των ψυχρών όζων και της χαμηλής διακριτικής ικανότητας της μεθόδου (απεικονίσιμοι οι όζοι >1,0 cm) (31). Επίσης, όπως ήδη αναφέρθηκε έχει ένδειξη για την διερεύνηση οζώδους βρογχοκήλης με τάση «καταδύσεως» προς την θωρακική κοιλότητα.
Η αξονική και η μαγνητική τομογραφία τραχήλου ενδείκνυνται μόνο σε επιλεγμένες περιπτώσεις ασθενών με ευμεγέθεις οζώδεις βρογχοκήλες ή/και πιεστικά φαινόμενα προκειμένου να εκτιμηθεί η σχέση της θυρεοειδικής διόγκωσης με τις γειτονικές ανατομικές δομές και η πιθανότητα διήθησης αυτών, καθώς και για την διερεύνηση «καταδυομένης» στην θωρακική κοιλότητα (οπισθοστερνικής) βρογχοκήλης (31). Επίσης, με τις ανωτέρω απεικονιστικές μεθόδους ελέγχονται λεπτομερέστερα οι λεμφαδενικές διογκώσεις.
6.2.5. Παρακέντηση με λεπτή βελόνα (FNA)
Η παρακέντηση με λεπτή (διάμετρος 25-27 gauge) βελόνα (fine needle aspiration, FNA) αποτελεί την πλέον ακριβή και πλεονεκτική μέθοδο από πλευράς ωφέλους/κόστους για την διερεύνηση των όζων θυρεοειδούς. Εφαρμόζεται πλέον ευρύτατα στην καθημερινή κλινική πράξη και έχει οδηγήσει σε σημαντική μείωση των θυρεοειδεκτομών και αντίστοιχα σε αύξηση του ποσοστού κακοηθείας στις θυρεοειδεκτομές, λόγω καλύτερης επιλογής προς χειρουργική αντιμετώπιση των ασθενών με οζώδη θυρεοειδική νόσο και αυξημένο κίνδυνο ή βεβαιότητα κακοηθείας (1,9,10,17,18,43,44).
Σύμφωνα με τις κατευθυντήριες οδηγίες των Επιστημονικών Εταιρειών Θυρεοειδούς ένδειξη για παρακέντηση προκύπτει για κάθε όζο διαμέτρου ≥ 1,0 cm εκτός εκείνων που υπερλειτουργούν (τεκμηριωμένο σπινθηρογραφικά), εκείνων που χαρακτηρίζονται ως αμιγώς κυστικοί υπερηχογραφικά και των σπογγόμορφων όζων διαμέτρου < 2,0 cm (26,27,31). Επίσης, ένδειξη για παρακέντηση προκύπτει για κάθε όζο διαμέτρου < 1,0 cm με ύποπτα υπερηχογραφικά χαρακτηριστικά ή/και ιστορικό ασθενούς με υψηλό κίνδυνο (26,27,31), όπως έχουν προαναφερθεί. Επί παρουσίας πολλαπλών όζων θα πρέπει να εξετάζεται η ένδειξη για FNA για κάθε όζο ξεχωριστά (26,27,31). Σε οζώδεις βρογχοκήλες με θερμές και ψυχρές περιοχές στο σπινθηρογράφημα, η ένδειξη για παρακέντηση θα πρέπει να εξετάζεται για τους ψυχρούς και χλιαρούς όζους σε συνδυασμό με τα υπερηχογραφικά ευρήματα (26,27,31). Επίσης, επί παρουσίας υπόπτων διογκωμένων λεμφαδένων διαπιστωμένων ψηλαφητικά ή/και υπερηχογραφικά θα πρέπει να γίνεται FNA των λεμφαδένων (26,27,31). Η FNA μπορεί να γίνει είτε με ψηλαφητική καθοδήγηση, εφ’ όσον ο όζος είναι ψηλαφητός, είτε με υπερηχογραφική καθοδήγηση (45). Η υπερηχογραφικά καθοδηγούμενη FNA συνιστάται 1) σε αψηλάφητους όζους είτε λόγω μικρού μεγέθους ή/και λόγω θέσης (οπίσθια επιφάνεια λοβών) 2) σε καθ’υπεροχήν κυστικούς όζους, προκειμένου να ληφθεί υλικό από το συμπαγές στοιχείο και 3) σε επανάληψη FNA μετά από προηγούμενο μη διαγνωστικό αποτέλεσμα (27,31,45). Η μέθοδος είναι επεμβατική, είναι όμως ασφαλής με σπάνιες ανεπιθύμητες ενέργειες όπως πόνος στο σημείο της παρακέντησης, εμφάνιση εκχύμωσης ή αιματώματος, αντιδράσεις από το παρασυμπαθητικό, λοίμωξη και παροδική πάρεση λαρυγγικού, ενώ εξαιρετικά σπάνια είναι η διασπορά νεοπλασματικών κυττάρων κατά μήκος της διαδρομής της βελόνας (46). Η μέθοδος χαρακτηρίζεται από υψηλή ευαισθησία και ειδικότητα, εφ’ όσον γίνεται από έμπειρο ιατρό, το ληφθέν υλικό είναι επαρκές ποιοτικά και ποσοτικά και αξιολογείται από έμπειρο κυτταρολόγο (46).
Το αποτέλεσμα της κυτταρολογικής εξέτασης σύμφωνα με την πλέον πρόσφατη ταξινόμηση, όπως καθορίστηκε από την συνάντηση των ειδικών στο Εθνικό Ινστιτούτο Καρκίνου, στην Bethesda των ΗΠΑ (National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference) το 2007, μπορεί να είναι: υλικό μη διαγνωστικό (κατηγορία Ι), καλοήθεια (κατηγορία ΙΙ), θυλακιώδης αλλοίωση ακαθορίστου σημασίας / ατυπία (κατηγορία ΙΙΙ), θυλακιώδες νεόπλασμα (κατηγορία ΙV), υλικό ύποπτο για κακοήθεια (κατηγορία V), κακοήθεια (κατηγορία VI) (47). Η κυτταρολογική εξέταση μπορεί να δείξει μη διαγνωστικό υλικό λόγω υποκυτταρικότητας στο δείγμα όπως σε καθ’ υπεροχήν κυστικούς όζους, σε κακή ποιότητα δείγματος (απουσία θυλακιωδών κυττάρων) ή/και κακή τεχνική (επίστρωση, μονιμοποίηση). Επαρκές για την κυτταρολογική διάγνωση, θεωρείται το υλικό που αποτελείται από τουλάχιστον 6 ομάδες από 10-20 καλά διατηρημένα επιθηλιακά κύτταρα η κάθε μία, για τους συμπαγείς όζους (31, 46). Η πιθανότητα κακοηθείας ανάλογα με το αποτέλεσμα κατά Bethesda έχει ως εξής: καλοήθεια – 0-3% ποσοστό κακοήθειας (ψευδώς αρνητικά), θυλακιώδης αλλοίωση ακαθορίστου σημασίας / ατυπία – 5-15% ποσοστό κακοήθειας, θυλακιώδες νεόπλασμα – 20-30% ποσοστό κακοήθειας, υλικό ύποπτο για κακοήθεια – 50-75% ποσοστό κακοήθειας, κακοήθεια – 97-100% ποσοστό κακοήθειας (0-3% ψευδώς θετικά) (47,48). Επομένως, ανάλογα με το αποτέλεσμα της κυτταρολογικής εξέτασης είναι και η περαιτέρω αντιμετώπιση του ασθενούς, όπως θα αναφερθεί στην συνέχεια. Πρέπει να σημειωθεί ότι στις πλέον πρόσφατες κατευθυντήριες οδηγίες των Επιστημονικών Εταιριών (27,31) οι κατηγορίες ΙΙΙ & ΙV κατά Bethesda που αφορούν θυλακιώδεις βλάβες αναφέρονται ως αποτέλεσμα ακαθορίστου σημασίας (indeterminate cytology).
Παρακέντηση όζων θυρεοειδούς με μεγάλου εύρους βελόνα (διάμετρος ≤20 gauge) συνιστάται κυρίως για την εκκένωση κυστικών σχηματισμών που περιέχουν παχύρρευστο υγρό (31,46). Η χρήση μεγάλου εύρους βελόνας για την λήψη δείγματος ιστού (core needle biopsy, CNB) συνιστάται μόνο σε επιλεγμένες περιπτώσεις όζων όπου επανειλημμένες FNA είναι μη διαγνωστικές (31,46,49) ή σε περιπτώσεις ασυμφωνίας κλινικών ευρημάτων και αποτελέσματος FNA (31,46). Η CNB δεν ενδείκνυται για την διερεύνηση όζων που χαρακτηρίζονται ως θυλακιώδεις αλλοιώσεις μετά από FNA, καθώς δεν μπορεί να προσφέρει περισσότερες πληροφορίες για την διάκριση μεταξύ θυλακιώδους αδενώματος και καρκινώματος (31,46,50).
Σε περιπτώσεις FNA με αποτέλεσμα ακαθορίστου σημασίας (κατηγορία ΙΙΙ & ΙV κατά Bethesda) ο έλεγχος διαφόρων μοριακών δεικτών στο κυτταρολογικό υλικό (51) όπως έκφραση παραγόντων [κυτταροκερατίνη-19 (CK-19), Hector Battifora mesothelial-1 (HBME-1), galectin 3 (Gal-3)] (52) ή παρουσία σωματικών μεταλλάξεων (BRAF, RAS, RET/PTC, RAS, PAX8/PPARγ) (53) είτε η έκφραση mRNA πολλαπλών γονιδίων (gene expression classifier, GEC) (54) ή η διαταραχή έκφρασης microRNAs (55) μπορεί να βοηθήσει στην διάκριση μεταξύ θυλακιοκυτταρικού καρκινώματος και καλοήθους βλάβης. Ο έλεγχος αυτός σύμφωνα με τις κατευθυντήριες οδηγίες της ΑΤΑ (27) και των AACE/AME/ETA (31) συστήνεται σε επιλεγμένες περιπτώσεις.
Σε περιπτώσεις υποψίας μυελοειδούς καρκινώματος ο προσδιορισμός καλσιτονίνης στο υγρό μετά από έκπλυση της βελόνας παρακέντησης του όζου με φυσιολογικό ορό (needle washout), μπορεί να βοηθήσει την κυτταρολογική διάγνωση. Επίπεδα καλσιτονίνης >100 ng/ml στο υγρό έκπλυσης είναι ενδεικτικό μυελοειδούς καρκινώματος (31). Επί τραχηλικών λεμφαδενικών διογκώσεων και υποψίας μεταστατικού μυελοειδούς καρκινώματος επίπεδα καλσιτονίνης >100ng/ml στο υγρό έκπλυσης μετά από FNA των λεμφαδένων είναι σχεδόν διαγνωστικά (31). Αντιστοίχως, επί τραχηλικών λεμφαδενικών διογκώσεων και υποψίας μεταστατικού θυλακιοκυτταρικού καρκινώματος επίπεδα θυρεοσφαιρίνης >100ng/ml στο υγρό έκπλυσης είναι διαγνωστικά (31). Τέλος σε περιπτώσεις ασαφούς διάκρισης μεταξύ διηθημένων λεμφαδένων και παραθυρεοειδικών διογκώσεων ο προσδιορισμός παραθορμόνης στο υγρό έκπλυσης μετά από FNA μπορεί να βοηθήσει στην διαφορική διάγνωση (31).
7. Αντιμετώπιση
Η αντιμετώπιση της οζώδους θυρεοειδικής νόσου καθοδηγείται από τα ευρήματα του υπερηχογραφικού ελέγχου, από την παρουσία ή μη υπερθυρεοειδισμού, κυρίως όμως από το αποτέλεσμα της FNA (1,18,27,31).
Σε περίπτωση που το αποτέλεσμα της FNA είναι κακοήθεια (κατηγορία VI κατά Bethesda) και πρόκειται για διαφοροποιημένο θυλακιοκυτταρικό καρκίνωμα ή μυελοειδές καρκίνωμα, η θεραπεία εκλογής είναι η χειρουργική (26,27,31,56). Εφ’ όσον πρόκειται για αδιαφοροποίητο καρκίνωμα ή λέμφωμα, θα χρειαστεί περαιτέρω διερεύνηση προτού ληφθεί η απόφαση για χειρουργείο. Εφ’ όσον πρόκειται για μεταστατική νόσο θα πρέπει να αναζητηθεί η πρωτοπαθής εστία και η αντιμετώπιση θα διαμορφωθεί βάσει της αντιμετώπισης της πρωτοπαθούς νόσου (31).
Σε περίπτωση που το αποτέλεσμα της FNA είναι ύποπτο για κακοήθεια (κατηγορία V κατά Bethesda), δεδομένου ότι το ποσοστό ιστολογικά τεκμηριωμένης κακοηθείας ανέρχεται στο 50-75% (56, 57) συνιστάται επίσης χειρουργκή αντιμετώπιση (31, 56).
Σε περίπτωση που το αποτέλεσμα της FNA είναι θυλακιώδης βλάβη ακαθορίστου σημασίας (indeterminate cytology) (κατηγορίες ΙΙΙ & ΙV κατά Bethesda) συνιστάται χειρουργική αντιμετώπιση εφ’ όσον πρόκειται για θυλακιώδες αδένωμα (27,31,56) δεδομένου ότι έχει δειχθεί κακοήθεια σε ποσοστό 20-30%, ενώ εφ’ όσον πρόκειται για θυλακιώδης αλλοίωση ακαθορίστου σημασίας / ατυπία, για την οποία έχει δειχθεί κακοήθεια σε μικρότερο ποσοστό (5-15%), μπορεί να επαναληφθεί η FNA ή να συστηθεί εξ αρχής χειρουργική αντιμετώπιση αφού ληφθούν υπ’ όψιν κλινικά και απεικονιστικά δεδομένα (27,31). Ο έλεγχος μοριακών δεικτών μπορεί να πραγματοποιηθεί σε επιλεγμένες περιπτώσεις, αλλά δεν συνιστάται ως έλεγχος ρουτίνας (27,31).
Σε περίπτωση που το αποτέλεσμα της FNA είναι καλοήθεια, συνιστάται παρακολούθηση ανά διαστήματα 6-18 μηνών με κλινική εξέταση, προσδιορισμό TSH και υπερηχογραφικό έλεγχο, δεδομένου ότι ψευδώς αρνητικά αποτελέσματα αναφέρονται σε ποσοστό ~5% (27, 31). Η διάρκεια παρακολούθησης δεν έχει καθοριστεί. Εφ’ όσον κατά την παρακολούθηση διαπιστωθεί υπερηχογραφικά αύξηση της διαμέτρου του όζου κατά 20% σε συμπαγείς όζους τίθεται η ένδειξη για νέα FNA, καθώς αυτή η μεταβολή αντιστοιχεί σε μεταβολή όγκου κατά 50% (27,31). Σε όζους μεικτής σύστασης, θα πρέπει να αξιολογείται υπερηχογραφικά η αύξηση μεγέθους του/των συμπαγών στοιχείων (27). Εφ’ όσον κατά την παρακολούθηση διαπιστωθεί συνεχής αύξηση του μεγέθους του/των όζων ή/και εμφάνιση υπερηχογραφικών χαρακτηριστικών που θέτουν την υπόνοια κακοηθείας, παρά την επανάληψη αρνητικού αποτελέσματος FNA συνιστάται χειρουργκή αντιμετώπιση (31). Όσον αφορά στην χορήγηση αγωγής με θυροξίνη σε δόση αναστολής της TSH σε ασθενείς με καλοήθεις όζους με στόχο την συρρίκνωση των όζων, πρακτική που έχει εφαρμοστεί ευρύτατα και για πολλά χρόνια, σύμφωνα με τις κατευθυντήριες οδηγίες της ΑΤΑ (27) και των AACE/AME/ETA (31) έχει ένδειξη μόνο σε ασθενείς που βρίσκονται σε ιωδοπενικές περιοχές, νέας / μέσης ηλικίας και με μικρή βρογχοκήλη. Η χορήγηση αγωγής με θυροξίνη σε δόση αναστολής δεν συνιστάται σε ασθενείς που ζουν σε περιοχές με επάρκεια ιωδίου (27,31), καθώς οι μετα-αναλύσεις δεν έχουν δείξει κλινικά σημαντικό ώφελος με την ανωτέρω φαρμακευτική αγωγή (58,59). Επιπλέον, υπάρχουν επιφυλάξεις για την χορήγηση θυροξίνη σε δόση αναστολής για την καλοήθη οζώδη θυρεοειδική νόσο σε μετεμμηνοπαυσιακές γυναίκες, σε άνδρες άνω των 60 ετών, καθώς και σε ασθενείς με οστεοπόρωση, καρδιαγγειακά νοσήματα και συστηματικές παθήσεις (27,31).
Τα τελευταία χρόνια έχουν προταθεί ελάχιστα επεμβατικές τεχνικές υπό υπερηχογραφική καθοδήγηση, ως εναλλακτικές πρακτικές της χειρουργικής αντιμετώπισης των καλοήθων όζων, όπως είναι η διαδερμική έγχυση αιθανόλης (60) και η θερμική καταστροφή (ablation) με ραδιοσυχνότητες ή laser (61, 62). Η διαδερμική έγχυση αιθανόλης έχει δειχθεί αποτελεσματική κυρίως για την αντιμετώπιση θυρεοειδικών κύστεων που υποτροπιάζουν μετά από εκκενωτική παρακέντηση και όζων μεικτής σύστασης που κυριαρχεί το κυστικό στοιχείο (63, 64) και γι’ αυτό περιλαμβάνεται στις κατευθυντήριες οδηγίες της διεταιρικής συνεργασίας AACE/AME/ETA (31). Έχει επίσης δοκιμαστεί για την αντιμετώπιση αυτονόμων θυρεοειδικών όζων (65), ωστόσο δεν συνιστάται για την αντιμετώπιση των συμπαγών όζων, αυτονόμων ή μη, λόγω ανεπιθυμήτων ενεργειών και αυξημένου κινδύνου υποτροπής μακροχρονίως (31). Η θερμική καταστροφή των καλοήθων όζων έχει εισαχθεί την τελευταία δεκαετία για την αντιμετώπιση αυτονόμων ή μη όζων με ενθαρρυντικά αποτελέσματα (66,67). Ωστόσο, η μέθοδος δεν έχει αποτιμηθεί επαρκώς σε βάθος χρόνου, ως προς την αποτελεσματικότητα και την ασφάλεια, γι’ αυτό και συνιστάται να γίνεται σε επιλεγμένες περιπτώσεις όπου δεν είναι δυνατή η χειρουργική αντιμετώπιση, είτε λόγω αντενδείξεων είτε λόγω άρνησης των ασθενών και με την προϋπόθεση της εφαρμογής της σε εξειδικευμένα κέντρα (31,68).
Μία ακόμη μη χειρουργική θεραπευτική επιλογή για την αντιμετώπιση της μη τοξικής οζώδους βρογχοκήλης αποτελεί η χορήγηση θεραπευτικής δόσης ραδιενεργού ιωδίου Ι131 η οποία βασίζεται στην επερχόμενη σε ποικίλο βαθμό μεταθεραπευτική ρίκνωση του θυρεοειδικού ιστού. Με την αγωγή αυτή επιτυγχάνεται μείωση έως 50-60% στο μέγεθος του θυρεοειδούς σε σημαντικό ποσοστό ασθενών και σε διάστημα που κυμαίνεται από μήνες έως και 5 έτη (69,70), ωστόσο στις μισές περιπτώσεις των ασθενών που ανταποκρίνονται το αποτέλεσμα διαπιστώνεται μέσα στο πρώτο τρίμηνο από την λήψη (69, 70). Η μείωση του μεγέθους του θυρεοειδούς είναι ανάλογη της χορηγούμενης δόσης και αντιστρόφως ανάλογη του μεγέθους της βρογχοκήλης, ωστόσο ποσοστό 20% των ασθενών δεν παρουσιάζει καμμία ανταπόκριση (69,70). Η αποτελεσματικότητα της αγωγής επηρρεάζεται και από την ανομοιογενή πρόσληψη του Ι131 λόγω της παρουσίας όζων που υπολειτουργούν (ψυχρών), κυστικών περιοχών και ανάπτυξης συνδετικού ιστού (69). Δεύτερη θεραπευτική δόση ραδιενεργού ιωδίου Ι131 μπορεί να χορηγηθεί και επιτυγχάνονται συγκρίσιμα αποτελέσματα με την πρώτη χορήγηση (70). Πρώϊμες ανεπιθύμητες ενέργειες από την χορήγηση ραδιενεργού ιωδίου Ι131 είναι η μετακτινική θυρεοειδίτις, ο παροδικός υπερθυρεοειδισμός και η αύξηση του μεγέθους της βρογχοκήλης, οι οποίες δεν είναι συχνές, όμως απασχολούν σε ασθενείς με μεγάλες βρογχοκήλες (>100gr), στους οποίους έχει δοκιμαστεί η προφυλακτική αγωγή με γλυκοκορτικοειδή (πχ. πρεδνιζολόνη 20-30mg / 24ωρο για 2-4 εβδομάδες (70). Όψιμη ανεπιθύμητη ενέργεια είναι ο υποθυρεοειδισμός, ενώ ο κίνδυνος για εμφάνιση κακοηθείας θεωρείται αμελητέος (69,70). Η χορήγηση ανθρώπινης ανασυνδυασμένης TSH (recombinant human TSH, rhTSH) πριν την χορήγηση ραδιενεργού ιωδίου επιτυγχάνει βελτίωση του θεραπευτικού αποτελέσματος, καθώς αυξάνει την πρόσληψη του ραδιοϊσοτόπου από τον θυρεοειδικό ιστό (71) και αντίστοιχα περιορίζει την εξωθυρεοειδική πρόσληψη αυτού, ενώ παράλληλα επιτρέπει την μείωση της χορηγούμενης δόσης (72). Επίσης, μειώνει το ενδεχόμενο χορήγησης δεύτερης δόσης ραδιενεργού ιωδίου (73). Πρώϊμες ανεπιθύμητες ενέργειες από την προθεραπεία με rhTSH είναι ο παροδικός υπερθυρεοειδισμός και η παροδική διόγκωση του θυρεοειδούς, των οποίων η πιθανότητα εμφάνισης μειώνεται με την χορήγηση μικρών δόσεων rhTSH (≤ 0,1mg). Όψιμη ανεπιθύμητη ενέργεια είναι ο υποθυρεοειδισμός, με πενταπλάσια συχνότητα συγκριτικά με την κλασσική χορήγηση ραδιενεργού ιωδίου Ι131 (70).
Εφ’ όσον διαγνωστεί τοξικό αδένωμα ή τοξική οζώδης βρογχοκήλη η θεραπεία εκλογής είναι η χειρουργική, ιδίως αν πρόκειται για μεγάλο τοξικό αδένωμα ή μεγάλη τοξική οζώδη βρογχοκήλη και υπάρχουν συνοδές πιεστικές εκδηλώσεις ή αισθητικοί λόγοι (31). Προεγχειρητική προετοιμασία με αντιθυρεοειδικά φάρμακα μπορεί να χρειαστεί (70). Σε περίπτωση αντενδείξεων ή άρνησης της χειρουργικής αντιμετώπισης, καθώς και σε μικρό τοξικό αδένωμα ή μικρή τοξική βρογχοκήλη μπορεί να χορηγηθεί θεραπευτική δόση ραδιενεργού ιωδίου Ι131 (31). Το τοξικό αδένωμα είναι πιό ακτινοάντοχο από την τοξική οζώδη βρογχοκήλη και επομένως χρειάζονται υψηλότερες δόσεις ραδιενεργού ιωδίου Ι131 για την επίτευξη θεραπευτικού αποτελέσματος (31). Για τους περισσοτέρους ασθενείς η χορήγηση εφ’ άπαξ δόσης είναι αρκετή για την αντιμετώπιση της υπερλειτουργίας. Προετοιμασία με αντιθυρεοειδικά φάρμακα μπορεί να χρειαστεί και στην περίπτωση αυτή προτιμάται η χορήγηση μεθιμαζόλης ή καρβιμαζόλης, καθώς υπάρχουν δεδομένα ότι η προπυλθειουρακίλη ασκεί μία ακτινοπροστατευτική δράση, η οποία φαίνεται να είναι παρατεταμένη (70). Εφ’ όσον χορηγηθούν αντιθυρεοειδικά φάρμακα θα πρέπει να γίνει διακοπή αυτών πριν την λήψη του ραδιενεργού ιωδίου, ~5 μέρες για την μεθιμαζόλη ή καρβιμαζόλη και ~ 2 μήνες για την προπυλθειουρακίλη (70). Πριν την θεραπευτική χορήγηση ραδιενεργού ιωδίου θα πρέπει να αποφεύγεται η χρήση ιωδιούχων σκιαγραφικών και φαρμάκων που περιέχουν ιώδιο (προκειμένου να μην επηρρεαστεί η πρόσληψη ιωδίου από τον θυρεοειδή) και επίσης σε γυναίκες αναπαραγωγικής ηλικίας θα πρέπει να αποκλείεται το ενδεχόμενο εγκυμοσύνης. Εκτός από την εγκυμοσύνη, αντένδειξη για την θεραπεία με ραδιενεργό ιώδιο Ι131 αποτελεί και ο θηλασμός, δεδομένου ότι το ιώδιο απεκκρίνεται στο μητρικό γάλα (70). Σε γυναίκες αναπαραγωγικής ηλικίας συστήνεται επίσης να αποφεύγεται η εγκυμοσύνη τους πρώτους 6 μήνες μετά την θεραπεία με ραδιενεργό ιώδιο Ι131 (70). Η θεραπεία με ραδιενεργό ιώδιο Ι131, εκτός της αντιμετώπισης της υπερλειτουργίας με καταστροφή (ablation) του αυτονόμου λειτουργικού θυρεοειδικού ιστού, επιφέρει σημαντική μείωση στο μέγεθος του τοξικού αδενώματος ή της τοξικής οζώδους βρογχοκήλης (74). Ο μεταθεραπευτικός υποθυρεοειδισμός παρατηρείται σε ποσοστό που ποικίλλει ανάλογα κυρίως με την χορηγούμενη δόση και το μέγεθος του αδενώματος ή της βρογχοκήλης (31,70). Ο πρώτος έλεγχος θυρεοειδικής λειτουργίας μετά την λήψη θεραπευτικής δόσης ραδιενεργού ιωδίου γίνεται στους δύο μήνες. Το ποσοστό εμφάνισης μεταθεραπευτικού υποθυρεοειδισμού αυξάνει με την πάροδο του χρόνου, γι’ αυτό και οι ασθενείς αυτοί θα πρέπει να παρακολουθούνται σε τακτά χρονικά διαστήματα εφ’ όρου ζωής (70).
8. Ειδικά θέματα
8.1. Οζώδης θυρεοειδική νόσος στην εγκυμοσύνη
Η οζώδης θυρεοειδική νόσος στην εγκυμοσύνη αφορά στην πλειοψηφία των περιπτώσεων προϋπάρχουσα της εγκυμοσύνης νόσο, η οποία είναι συνήθως γνωστή. Η εγκυμοσύνη συσχετίζεται με αύξηση του μεγέθους των υπαρχόντων όζων και με εμφάνιση νέων όζων (75), πιθανώς λόγω του συχνά επερχομένου αρνητικού ισοζυγίου ιωδίου. Η χορήγηση όμως θυροξίνης σε δόση αναστολής για την αποφυγή εξέλιξης της νόσου δεν συνιστάται (31). Σε περίπτωση που κριθεί σκόπιμη η διερεύνηση του/των όζων, είναι ίδια με εκείνη εκτός εγκυμοσύνης (27,31), ωστόσο αντενδείκνυται η χρήση ραδιενεργού ιωδίου Ι131 για διαγνωστικούς σκοπούς, όπως άλλωστε και για θεραπευτικούς σκοπούς, όπως ήδη αναφέρθηκε. Σε ευθυρεοειδικές και υποθυρεοειδικές εγκύους, εφ’όσον υπάρχουν ενδείξεις για FNA, αυτή θα πρέπει να διενεργείται (27,31). Σε εγκύους με ανεσταλμένα επίπεδα TSH μετά το 1ο τρίμηνο της εγκυμοσύνης, η FNA μπορεί να αναβληθεί για μετά τον τοκετό και την διακοπή του θηλασμού, προκειμένου να ελεγχθεί σπινθηρογραφικά το ενδεχόμενο θερμού/θερμών όζου/όζων (27). Εφ’ όσον η FNA είναι διαγνωστική για διαφοροποιημένο θυλακιοκυτταρικό καρκίνωμα, μπορεί η χειρουργική αντιμετώπιση να προγραμματιστεί μετά τον τοκετό δεδομένου ότι 1) δεν έχει δειχθεί ότι πρόκειται για πιό επιθετική μορφή κατά την εγκυμοσύνη σε σύγκριση μη έγκυες γυναίκες παρόμοιας ηλικίας (76) 2) δεν έχει δειχθεί ότι η καθυστέρηση της θυρεοειδεκτομής για διάστημα μικρότερο του έτους επηρρεάζει την πορεία της νόσου ανεξαρτήτως εγκυμοσύνης (77) και 3) έχει δειχθεί αυξημένη συχνότητα επιπλοκών στις εγκύους που υποβάλλονται σε θυρεοειδεκτομή συγκριτικά μη έγκυες γυναίκες (78). Ωστόσο δεν υπάρχει ομοφωνία στην αντιμετώπιση και σε περίπτωση που κριθεί σκόπιμη η χειρουργική επέμβαση κατά την εγκυμοσύνη, συνιστάται να γίνεται κατά το 2ο τρίμηνο. Αναβολή της χειρουργικής αντιμετώπισης μετά τον τοκετό συνιστάται και στην περίπτωση που η FNA είναι είναι ύποπτη για κακοήθεια ή ενδεικτική θυλακιώδους βλάβης (κατηγορίες ΙΙΙ & ΙV κατά Bethesda) (31).
8.2. Οζώδης θυρεοειδική νόσος στην παιδική ηλικία
Παρά την απουσία επιδημιολογικών δεδομένων, η οζώδης θυρεοειδική νόσος σε παιδιά εκτιμάται σε ποσοστό 1,8% βάσει των υπαρχόντων μελετών (79-81). Όσον αφορά στην διερεύνηση της νόσου, είναι παρόμοια με των ενηλίκων (27,31). Το ποσοστό τεκμηριωμένης κακοηθείας σε χειρουργικές σειρές ανέρχεται στο 26% (81,83) και το ποσοστό κακοηθείας ή υλικού υπόπτου για κακοήθεια σε FNA ανέρχεται στο 9% και 18%, αντίστοιχα (81-83). Επίσης, φαίνεται ότι οι θερμοί όζοι στα παιδιά έχουν υψηλότερο ποσοστό κακοηθείας (83). Επομένως, λόγω της χαμηλώτερης συχνότητας οζώδους θυρεοειδικής νόσου στα παιδιά και του υψηλότερου ποσοστού κακοηθείας, έχει καταγραφεί και συχνότερη χειρουργική αντιμετώπιση της νόσου στα παιδιά συγκριτικά με τους ενήλικες.
Βιβλιογραφία
1. Hegedus L. The thyroid nodule. N Eng J Med 2004; 351: 1764-1771
2. Dean DS, Gharib H. Epidemiology of thyroid nodules. Best Pract Res Clin Endocrinol Metab 2008; 22(6): 901-911
3. Vander JB, Gaston EA, Dawber TR. The significance of nontoxic thyroid nodules: final report of a 15-year study of the incidence of thyroid malignancy. Ann Intern Med 1968; 69: 537-540
4. Tunbridge WM, Evered DC, Hall R, Appleton D, Brewis M, Clark F et al. The spectrum of thyroid disease in a community: the Whickham survey. Clin Endocrinol (Oxf) 1977; 7: 481–493
5. Brander A, Viikinkoski P, Tuuhea J, Voutilainen L, Kivisaari L. Clinical versus ultrasound examination of the thyroid gland in common clinical practice. J Clin Ultrasound 1992; 20: 37–42.
6. Ezzat S, Sarti DA, Cain DR, Braunstein GD. Thyroid incidentalomas: prevalence by palpation and ultrasonography. Arch Intern Med 1994; 154(16): 1838–40.
7. Knudsen N, Perrild H, Christiansen E, Rasmussen S, Dige-Petersen H, Jorgensen T. Thyroid structure and size and two year follow-up of solitary cold thyroid nodules in an unselected population with borderline iodine deficiency. Eur J Endocrinol 2000; 142: 224–230
8. Mortensen JD, Woolner LB, Bennett WA. Gross and microscopic findings in clinically normal thyroid glands. J Clin Endocrinol Metab 1955 15 1270–1280.
9. Gharib H. Changing trends in thyroid practice: understanding nodular thyroid disease. Endocr Pract. 2004;10:31-39
10. Schlumberger M, Pacini F. Thyroid nodule. In: Thyroid tumors. Nucleon Editions, Paris, 2006; pp: 11-31.
11. Wirowski D, Wicke C, Böhner H, Lammers BJ, Pohl P, Schwarz K, Goretzki PE. Presentation of 6 cases with parathyroid cysts and discussion of the literature. Exp Clin Endocrinol Diabetes. 2008; 116: 501-506
12. Burguera B, Gharib H. Thyroid incidentalomas: prevalence, diagnosis, significance, and management. Endocrinol Metab Clin North Am 2000; 29: 187–203.
13. Jarløv AE, Nygaard B, Hegedüs L, Hartling SG, Hansen JM. Observer variation in the clinical and laboratory evaluation of patients with thyroid dysfunction and goiter. Thyroid. 1998; 8(5): 393-398.
14. Gough J, Scott-Coombes D, Fausto Palazzo F. Thyroid incidentaloma: An evidence-based assessment of management strategy. World J Surg. 2008; 32: 1264-1268.
15. Kang KW, Kim SK, Kang HS, Lee ES, Sim JS, Lee IG, Jeong SY, Kim SW. Prevalence and risk of cancer of focal thyroid incidentaloma identified by 18F-fluorodeoxyglucose positron emission tomography for metastasis evaluation and cancer screening in healthy subjects. J Clin Endocrinol Metab 2003; 88: 4100–4104.
16. Soelberg KK, Bonnema SJ, Brix TH, Hegedüs L. Risk of malignancy in thyroid incidentalomas detected by 18F-fluorodeoxyglucose positron emission tomography: a systematic review. Thyroid 2012; 22(9): 918-925.
17. AACE/AME Task Force on Thyroid Nodules, American Association of Clinical Endocrinologists and Associazione Medici Endocrinologi. Medical Guidelines for clinical practice for the diagnosis and management of thyroid nodules. Endocr Pract 2006; 12: 65–102.
18. Bahn RS, Castro MR. Approach to the patient with nontoxic multinodular goiter. J Clin Endocrinol Metab 2011; 96: 1202–1212
19. Schlumberger M, Pacini F. Thyroid tumors after external irradiation to the neck. In: Thyroid tumors. Nucleon Editions, Paris, 2006; pp: 251-266.
20. Vriens MR, Suh I, Moses W, Kebebew E. Clinical features and genetic predisposition to hereditary nonmedullary thyroid cancer. Thyroid 2009; 19: 1343-1349
21. Pacini F, Castagna MG, Cipri C, Schlumberger M. Medullary thyroid carcinoma. Clin Oncol 2010; 22: 475-485.
22. Belfiore A, La Rosa GL, La Porta GA, Giuffrida D, Milazzo G, Lupo L, Regalbuto C, Vigneri R. Cancer risk in patients with cold thyroid nodules: relevance of iodine intake, sex, age and multinodularity. Am J Med 1992; 93: 363–369
23. Boelaert K, Horacek J, Holder RL, Watkinson JC, Sheppard MC, Franklyn JA. Serum thyrotropin concentration as a novel predictor of malignancy in thyroid nodules investigated by fine-needle aspiration. J Clin Endocrinol Metab 2006; 91: 4295–4301
24. Haymart MR, Repplinger DJ, Leverson GE, Elson DF, Sippel RS, Jaume JC, Chen H. Higher serum thyroid stimulating hormone level in thyroid nodule patients is associated with greater risks of differentiated thyroid cancer and advanced tumor stage. J Clin Endocrinol Metab 2008; 93: 809–814
25. Kim HK, Yoon JH, Kim SJ, Cho JS, Kweon SS, Kang HC. Higher TSH level is a risk factor for differentiated thyroid cancer. Clin Endocrinol 2013; 78: 472–477
26. Pacini F, Schlumberger M, Dralle H, Elisei R, Smit JW, Wiersinga W. European Thyroid Cancer Taskforce. European consensus for the management of patients with differentiated thyroid carcinoma of the follicular epithelium. Eur. J. Endocrinol 2006; 154: 787–803
27. Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, Mandel SJ, Mazzaferri EL, McIver B, Pacini F, Schlumberger M, Sherman SI, Steward DL, Tuttle RM. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer. Thyroid. 2009;19:1167-1214
28. Cheung K, Roman SA, Wang TS, Walker HD, Sosa JA. Calcitonin measurement in the evaluation of thyroid nodules in the United States: a cost-effectiveness and decision analysis. J Clin Endocrinol Metab 2008; 93: 2173–2180
29. Costante G, Durante C, Francis Z, Schlumberger M, Filetti S. Determination of calcitonin levels in C cell disease: clinical interest and potential pitfalls. Nat Clin Pract Endocrinol Metab 2009; 5: 35–44
30. Elisei R, Bottici V, Luchetti F, Di Coscio G, Romei C, Grasso L, Miccoli P, Iacconi P, Basolo F, Pinchera A, Pacini F. Impact of routine measurement of serum calcitonin on the diagnosis and outcome of medullary thyroid cancer: experience in 10,864 patients with nodular thyroid disorders. J Clin Endocrinol Metab 2004; 89: 163–168
31. Gharib, H. Papini E, Paschke R, Duick DS, Valcavi R, Hegedüs L, Vitti P. AACE/AME/ETA Task Force on Thyroid Nodules. American Association of Clinical Endocrinologists, Associazione Medici Endocrinologi and European Thyroid Association Medical guidelines for clinical practice for the diagnosis and management of thyroid nodules. Endocr Pract 2010; 16 (Suppl. 1): 1–43
32. Mandel SJ. Diagnostic use of ultrasonography in patients with nodular thyroid disease. Endocr Pract. 2004;10:246-252
33. Bonavita JA, Mayo J, Babb J, Bennett G, Oweity T, Macari M, Yee J. Pattern recognition of benign nodules at ultrasound of the thyroid: which nodules can be left alone? Am J Roentgenol 2009; 193: 207–213
34. Andrioli M, Carzaniga C, Persani L. Standardized ultrasound report for thyroid nodules: the endocrinologist’s viewpoint. Eur Thyroid J 2013; 2: 37–48
35. Horvath E, Majilis S, Rossi R, Franco C, Niedmann J, Castro A, Dominguez M. An ultrasonogram reporting system for thyroid nodules stratifying cancer risk for clinical management. J Clin Endocrinol Metab 2009; 90: 1748–1751
36. Park JY, Lee HJ, Jang HW, Kim HK, Yi JH, Lee W, Kim SH. A proposal for a thyroid imaging reporting and data system for ultrasound features of thyroid carcinoma. Thyroid 2009; 19: 1257–1264
37. Russ G, Royer B, Bigorgne C, Rouxel A, Bienvenu-Perrard M, Leenhardt L. Prospective evaluation of thyroid imaging reporting and data system on 4550 nodules with and without elastography. Eur J Endocrinol. 2013; 168(5): 649-655.
38. Ophir J, Alam SK, Garra B, Kallel F, Konofagou E, Krouskop T, Varghese T: Elastography: ultrasonic estimation and imaging of the elastic properties of tissues. Proc Inst Mech Eng H 1999; 213: 203–233.
39. Lyshchik A, Higashi T, Asato R, Tanaka S, Ito J, Mai JJ, Pellot-Barakat C, Insana MF, Brill AB, Saga T, Hiraoka M, Togashi K. Thyroid gland tumor diagnosis at US elastography. Radiology 2005; 237: 202–211.
40. Rago T, Santini F, Scutari M, Pinchera A, Vitti P: Elastography: new developments in ultrasound for predicting malignancy in thyroid nodules. J Clin Endocrinol Metab 2007; 92: 2917–2922.
41. Bojunga J, Herrmann E, Meyer G,Weber S, Zeuzem S & Mireen F-R. Real-time elastography for the differentiation of benign and malignant thyroid nodules: a meta-analysis. Thyroid 2010; 20: 1145–1150.
42. Ashcraft MW, Van Herle AJ. Management of thyroid nodules. II: Scanning techniques, thyroid suppressive therapy, and fine needle aspiration. Head Neck Surg 1981; 3: 297-322.
43. Zagorianakou P, Malamou-Mitsi V, Zagorianakou N, Stefanou D, Tsatsoulis A, Agnantis NJ. The role of fine-needle aspiration biopsy in the management of patients with thyroid nodules. In Vivo 2005; 19: 605–609.
44. Cappelli C, Rosei EA. Fine needle aspiration cytology of thyroid nodule. Thyroid 2006; 16: 819.
45. Cibas ES, Alexander EK, Benson CB, et al. Indications for Thyroid FNA and Pre-FNA Requirements: A synopsis of the National Cancer Institute Thyroid Fine Needle Aspiration State of the Science Conference. Diagn Cytopathol 2008; 36: 390–399.
46. Pitman ΜΒ, Abele J, Ali SZ, Duick D, Elsheikh TM, Jeffrey RB, Powers CN, Randolph G, Renshaw A, Scoutt L. Techniques for thyroid FNA: A synopsis of the National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference. Diagn Cytopathol 2008; 36: 407–424.
47. Baloch ZW, LiVolsi VA, Asa SL, Rosai J, Merino MJ, Randolph G, Vielh P, DeMay RM, Sidawy MK, Frable WJ. Diagnostic terminology and morphologic criteria for cytologic diagnosis of thyroid lesions: A synopsis of the National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference. Diagn Cytopathol 2008; 36: 425-437
48. Cibas ES, Ali SZ. The Bethesda system for reporting thyroid cytopathology. Thyroid 2009; 19: 1159-1165
49. Samir ΑΕ, Vij A, Seale MK, Desai G, Halpern E, Faquin WC, Parangi S, Hahn PF, Daniels GH. Ultrasound-guided percutaneous thyroid nodule core biopsy: clinical utility in patients with prior nondiagnostic fine-needle aspirate. Thyroid 2012; 22: 461-467
50. Elsheikh TM, Singh HK, Silverman JF. Fine-needle aspiration cytology versus core needle biopsy in the evaluation of thyroid and salivary gland lesions. Path Case Rev 2007; 12: 3-9
51. Duick DS. Overview of molecular biomarkers for enhancing the management of cytologically indeterminate thyroid nodules and thyroid cancer. Endocr Pract. 2012; 18: 611-615.
52. de Matos LL, Del Giglio AB, Matsubayashi CO, de Lima Farah M, Del Giglio A, da Silva Pinhal MA. Expression of CK-19, galectin-3 and HBME-1 in the differentiation of thyroid lesions: systematic review and diagnostic meta-analysis. Diagn Pathol 2012; 7: 97
53. Nikiforova MN, Nikiforov YE. Molecular diagnostics and predictors in thyroid cancer. Thyroid 2009;19: 1351-1361
54. Chudova D, Wilde JI, Wang ET, Wang H, Rabbee N, Egidio CM, Reynolds J, Tom E, Pagan M, Rigl CT, Friedman L, Wang CC, Lanman RB, Zeiger M, Kebebew E, Rosai J, Fellegara G, LiVolsi VA, Kennedy GC. Molecular classification of thyroid nodules using high-dimensionality genomic data. J Clin Endocrinol Metab. 2010; 95: 5296-5304
55. de la Chapelle A, Jazdzewski K. MicroRNAs in thyroid cancer. J Clin Endocrinol Metab. 2011; 96: 3326-3336
56. Layfield LJ, Abrams J, Cochand-Priollet B, Evans D, Gharib H, Greenspan F, Henry M, LiVolsi V, Merino M, Michael CW, Wang H, Wells SA. Post-thyroid FNA testing and treatment options: A synopsis of the National Cancer Institute Thyroid Fine-Needle Aspiration State of the Science Conference. Diagn Cytopathol 2008; 36: 442–448
57. Yang J, Schnadig V, Logrono R, Wasserman PG. Fine-needle aspiration of thyroid nodules: A study of 4703 patients with histologic and clinical correlations. Cancer 2007; 111: 306-315
58. Castro MR, Caraballo PJ, Morris JC. Effectiveness of thyroid hormone suppressive therapy in benign solitary thyroid nodules: a meta-analysis. J. Clin. Endocrinol. Metab 2002; 87: 4154–4159
59. Richter B, Neises G, Clar C. Pharmacotherapy for thyroid nodules. A systematic review and meta-analysis. Endocrinol. Metab. Clin. North Am. 2002; 31: 699–722
60. Bennedbæk FN, Hegedus L. Percutaneous ethanol injection therapy in benign solitary solid cold thyroid nodules: a randomized trial comparing one injection with three injections. Thyroid 1999 9 225–233.
61. Papini E, Guglielmi R, Bizzarri G, Pacella CM. Ultrasound-guided laser thermal ablation for treatment of benign thyroid nodules. Endocr Pract 2004; 10: 276-283
62. Baek JH, Kim YS, Lee D, Huh JY, Lee JH. Benign predominantly solid thyroid nodules: prospective study of efficacy of sonographically guided radiofrequency ablation versus control condition. AJR. American Journal of Roentgenology 2010; 194: 1137–1142
63. Guglielmi R, Pacella CM, Bianchini A, Bizzarri G, Rinaldi R, Graziano FM, Petrucci L, Toscano V, Palma E, Poggi M, Papini E. Percutaneous ethanol injection treatment in benign thyroid lesions: role and efficacy. Thyroid 2004; 14: 125-131
64. Valcavi R, Frasoldati A. Ultrasound-guided percutaneous ethanol injection therapy in thyroid cystic nodules. Endocr Pract 2004; 10: 269–275
65. Livraghi T, Paracchi A, Ferrari C, Bergonzi M, Garavaglia G, Raineri P, Vettori C. Treatment of autonomous thyroid nodules with percutaneous ethanol injection: 4‑year experience. Radiology 1990; 190: 529–533
66. Spiezia S, Garberoglio R, Milone F, Ramundo V, Caiazzo C, Assanti AP, Deandrea M, Limone PP, Macchia PE, Lombardi G, Colao A, Faggiano A. Thyroid nodules and related symptoms are stably controlled two years after radiofrequency thermal ablation. Thyroid 2009; 19: 219–225
67. Døssing H, Bennedbæk FN, Hegedüs L. Long-term outcome following interstitial laser photocoagulation of benign cold thyroid nodules. Eur J Endocrinol. 2011; 165: 123-128
68. Gharib H, Hegedüs L, Pacella CM, Baek JH, Papini E. Clinical review: Nonsurgical, image-guided, minimally invasive therapy for thyroid nodules. J Clin Endocrinol Metab 2013; 98: 3949-3957
69. Hegedüs L, Bonnema SJ, Bennedbaek FN. Management of simple nodular goiter: current status and future perspectives. Endocr Rev 2003; 24: 102-132
70. Weetman PA. Radioiodine treatment for benign thyroid diseases. Clin Endocrinol 2007; 66: 757-764
71. Huysmans DA, Nieuwlaat W, Erdtsieck J, Schellekens AP, Bus JW, Bravenboer B, Hermus AR. Administration of a single low dose of recombinant human thyrotropin significantly enhances thyroid radioiodine uptake in nontoxic nodular goiter. J Clin Endocrinol Metab 2000; 85: 3592–3596
72. Nieuwlaat WA, Huysmans DA, van den Bosch HC, et al. Pretreatment with a single, low dose of recombinant human thyrotropin allows dose reduction of radioiodine therapy in patients with nodular goiter. J Clin Endocrinol Metab 2003; 88: 3121-3129.
73. Fast S, Nielsen VE, Grupe P, Boel-Jørgensen H, Bastholt L, Andersen PB, Bonnema SJ, Hegedüs L. Prestimulation with recombinant human thyrotropin (rhTSH) improves the long-term outcome of radioiodine therapy for multinodular nontoxic goiter. J Clin Endocrinol Metab 2012; 97: 2653-60
74. Nygaard B, Hegedus L, Nielsen KG, Ulriksen P, Hansen JM. Long-term effect of radioactive iodine on thyroid function and size in patients with solitary autonomously functioning toxic thyroid nodules. Clin Endocrinol 1999; 50: 197-202
75. Kung AW, Chau MT, Lao TT, Tam SC, Low LC. The effect of pregnancy on thyroid nodule formation. J Clin Endocrinol Metab. 2002; 87: 1010-1014
76. Moosa M, Mazzaferri EL. Outcome of differentiated thyroid cancer diagnosed in pregnant women. J Clin Endocrinol Metab 1997; 82: 2862-2866
77. Mazzaferri EL, Jhiang SM. Long-term impact of initial surgical and medical therapy on papillary and follicular thyroid cancer. Am J Med 1994; 97: 418-428
78. Kuy S, Roman SA, Desai R, Sosa JA. Outcomes following thyroid and parathyroid surgery in pregnant women. Arch Surg 2009; 144: 399-406
79. Rallison ML, Dobyns BM, Keating FR Jr, Rall JE, Tyler FH. Thyroid nodularity in children. JAMA 1975; 233: 1069-1072
80. Hung W. Solitary thyroid nodules in 93 children and adolescents, a 35-years experience. Horm Res 1999; 52: 15-18
81. Raab SS, Silverman JF, Elsheikh TM, Thomas PA, Wakely PE. Pediatric thyroid nodules: Disease demographics and clinical management as determined by fine needle aspiration biopsy. Pediatrics. 1995; 95:46-49.
82. Amrikachi M, Ponder TB, Wheeler TM, Smith D, Ramzy I. Thyroid fine-needle aspiration biopsy in children and adolescents: experience with 218 aspirates. Diagn Cytopathol. 2005; 32: 189-192
83. Niedziela M. Pathogenesis, diagnosis and management of thyroid nodules in children. Endocr Relat Cancer 2006; 13: 427-453
Created: October 30, 2014
Last update: October 30, 2014