Νικόλαος Ποντικίδης
Ευαγγελία Κιντιράκη
Σπυρίδων Καρράς
Kλινική Ενδοκρινολογίας- Σακχαρώδη Διαβήτη και Μεταβολισμού
Γ.Ν Άγιος Παύλος ‘Παράρτημα Παναγία’
Εισαγωγή
Ο όρος υποκλινική θυρεοειδική δυσλειτουργία (ΥΘΔ) αναφέρεται στο πολύ πρώιμο (βιοχημικό, υπολινικό ή προκλινικό) στάδιο ανεπάρκειας (υποκλινικός υποθυρεοειδισμός – ΥΥΘ) ή παρουσίας αυξημένων ποσοτήτων θυρεοειδικών ορμονών (υποκλινική θυρεοτοξίκωση ή υπερθυρεοειδισμός- ΥΥπΘ). Χαρακτηρίζεται από την ανεύρεση παθολογικής τιμής θυρεοτρόπου ορμόνης (TSH), αυξημένης ή μειωμένης αντίστοιχα, και φυσιολογικών επιπέδων θυρεοειδικών ορμονών (free T4, free T3) στον ορό (1,2). Η δυνατότητά μας να ανιχνεύουμε διαρκώς πιο ήπιες διαβαθμίσεις ΥΘΔ έχει βελτιωθεί με την εισαγωγή στην εργαστηριακή πρακτική πιο ευαίσθητων μεθόδων, με συνέπεια τα ποσοστά ανίχνευσης ΥΘΔ διαφόρων διαβαθμίσεων να έχει αυξηθεί τις τελευταίες δεκαετίες. Σε αυτήν τη διαπίστωση συνέβαλε ασφαλώς και η αυξανόμενη συχνότητα αναγραφής εξετάσεων ελέγχου της θυρεοειδικής λειτουργίας ακόμη και χωρίς την παρουσία σημείων- συμπτωμάτων ενδεικτικών κάποιας αναγνωρίσιμης θυρεοειδικής πάθησης, ιδιαίτερα σε νεαρά και μέσης ηλικίας άτομα, σε έγκυες, αλλά και σε ηλικιωμένα άτομα. Ωστόσο, η πληθυσμιακή γενίκευση της αναζήτησης και ακόμη περισσότερο της αντιμετώπισης της ΥΘΔ είναι αμφιλεγόμενη παρά το υψηλό ποσοστό επίπτωσης της ΥΘΔ και της δυνητικής εξέλιξής της σε έκδηλη νόσο (3-5). Αυτό κατά κύριο λόγο διότι ο κίνδυνος εκδήλωσης ΥΘΔ δε μπορεί να προκαθορισθεί, τα δε οφέλη από τη θεραπευτική παρέμβαση είναι αβέβαια επίσης. Επιπλέον υπάρχει διάσταση απόψεων αναφορικά με την επίδραση της ΥΘΔ στους διαφόρους ιστούς και όργανα, τη συσχέτισή της με κλινικά σημεία και συμπτώματα και κυρίως την καρδιαγγειακή νοσηρότητα της ήπιας ΥΘΔ (3-7).
Τις τελευταίες δεκαετίες παρατηρείται μια προοδευτική μείωση των ανώτερων φυσιολογικών τιμών αναφοράς της TSH από 7,0 – 10,0 mU/L σε 4,0 – 5,0 mU/L. Ο υποκλινικός υποθυρεοειδισμός (ΥΥΘ) χαρακτηρίζεται από την ανεύρεση αυξημένων τιμών TSH ενώ τα επίπεδα των ελεύθερων θυρεοειδικών ορμονών βρίσκονται στα κατώτερα φυσιολογικά όρια (1,4,8,9). Είναι σημαντικό ωστόσο να διακριθούν οι ‘ασθενείς’ σε αυτούς με ήπιο ΥΥΘ (τιμές TSH μεταξύ 5,0 – 9,0 mU/L) και εκείνους με πιο υψηλές τιμές TSH (> 10,0 mU/L). Έχει διαπιστωθεί ότι η πλειονότητα (~ 75%) των ατόμων με ΥΥΘ ανήκουν στην πρώτη κατηγορία.
1. Επιδημιολογικά δεδομένα – επίπτωση
Επειδή η μόνη παράμετρος που χρησιμοποιείται για την ανίχνευση ΥΥΘ είναι η τιμή της TSH, είναι σημαντικό για τη διάγνωσή του να οριοθετηθούν οι τιμές αναφοράς της (9,10). Το θέμα δε των τιμών αναφοράς της TSH όπως αναφέρθηκε, έχει αποτελέσει σημείο αντιπαράθεσης (9-13). Ως γνωστόν οι τιμές της TSH εμφανίζουν αρνητική ευθύγραμμη συσχέτιση με τα επίπεδα της free T4. Ωστόσο ενώ η διακύμανση των τιμών της free T4 κινείται σε αριθμητική κλίμακα η διακύμανση των τιμών της TSH ακολουθεί λογαριθμική κλίμακα. Αυτό σημαίνει ότι και μικρές ακόμα μεταβολές στα επίπεδα της πρώτης (π.χ διπλασιασμός ή υποδιπλασιασμός) προκαλούν δυσανάλογη μεταβολή στα επίπεδα της TSH (100-πλάσια). Έτσι ο προσδιορισμός της TSH αποτελεί την απαραίτητη δοκιμασία για την πρώιμη διάγνωση του ήπιου ΥΥΘ, όταν οι τιμές των ΘΟ ανευρίσκονται εντός φυσιολογικών ορίων (14) (εικόνα 1). Η ενδοατομική διακύμανση των τιμών των θυρεοειδικών ορμονών είναι ‘στενότερη’ από τα πληθυσμιακά όρια αναφοράς. Συνεπώς ακόμα και μικρή μείωση των τιμών των ΘΟ εντός των ορίων αναφοράς επιφέρουν δυσανάλογη αύξηση στα επίπεδα της TSH, πάνω από τα φυσιολογικά όρια.
Η επίπτωση του ΥΥΘ υπολογίζεται μεταξύ 3 – 8% στον γενικό πληθυσμό (15, 16) και μεταξύ 4-20% στον ενήλικο πληθυσμό (1,8,17). Η συχνότητα ανίχνευσης ΥΥΘ βαίνει αυξανόμενη με την ηλικία και το φύλο μιας και ανευρίσκεται συχνότερα στις γυναίκες (15). Μετά τα 60 έτη η συχνότητα ανεύρεσης ΥΥΘ εξομοιώνεται στα δύο φύλα με μέση συχνότητα 10% (15). Το μεγάλο εύρος τω ποσοστών ανίχνευσης αντανακλά σημαντικές διαφορές στους πληθυσμούς που ελέγχθηκαν, από πλευράς φυλής και διαιτητικής πρόσληψης ιωδίου, ανομοιογένειας των επιμέρους χαρακτηριστικών (ηλικία, φύλο, δείκτης μάζας σώματος) όπως και τη διαφορετική μεθοδολογία προσδιορισμού της TSH και των ανώτερων ορίων αναφοράς της τελευταίας(1, 8, 18).
Η πλειονότητα των ασθενών (75 – 80%) εμφανίζει τιμές TSH ως 10 mU/L και σε ανάλογο ποσοστό των ασθενών με ήπιο ΥΥΘ ανιχνεύονται θετικοί τίτλοι αντιθυρεοειδικών αντισωμάτων (19).
2. Αιτιολογία
Η αυτοάνοση χρονία θυρεοειδίτιδα (θυρεοειδίτιδα Hashimoto) θεωρείται ως η πιο συχνή αιτία προϊούσας καταστροφής του θυρεοειδικού παρεγχύματος και υποθυρεοειδισμού στους ενήλικες (1,8,20). Σε ένα ποσοστό περίπου 15% των περιπτώσεων είναι δυνατόν να σχετίζεται και με άλλα συστηματικά αυτοάνοσα νοσήματα, όπως λεύκη, αλωπεκία, ψωρίαση, μεγαλοβλαστική αναιμία, ρευματικά νοσήματα κ.α. Η συχνότητά της είναι μεγαλύτερη στις γυναίκες αναπαραγωγικής- μέσης ηλικίας (30-50 έτη). Η επίπτωση της νόσου ωστόσο βαίνει αυξανόμενη με την αύξηση της ηλικίας και στα δύο φύλα φτάνοντας ως και το 20% την ένατη δεκαετία ζωής (1,8).
Άλλα αίτια επίκτητου υποθυρεοειδισμού αποτελούν η θυρεοειδεκτομή, η ακτινοβόληση, είτε εσωτερική (ραδιενεργό ιώδιο- RAI) είτε εξωτερική στην περιοχή κεφαλής – τραχήλου, φλεγμονώδη νοσήματα του θυρεοειδούς αδένα (υποξεία, ανώδυνη και θυρεοειδίτιδα της λοχείας) και διηθητικά νοσήμα. Διάφορα φάρμακα (ιωδιούχα, λίθιο) μπορούν επίσης να προκαλέσουν υποκλινικό ή κλινικό υποθυρεοειδισμό ιδιαίτερα όταν προϋπάρχει υποκείμενη θυρεοειδική νόσος (1,8,20). Τέλος πλημμελής συμμόρφωση, δυσαπορρόφηση ή φαρμακευτική ή άλλη επίδραση μπορεί να οδηγήσει σε ΥΥΘ ασθενείς με έκδηλο υποθυρεοειδισμό που λαμβάνουν ήδη θεραπεία υποκατάστασης με λεβοθυροξίνη (LT4) (21) (Πίνακας 1).
Πίνακας 1. Αίτια υποκλινικού υποθυρεοειδισμού [μεταφρασμένο από Biondi B et al (1)].
| Αίτια |
| Χρόνια αυτοάνοση θυρεοειδίτιδα(παράγοντες κινδύνου: θετικό οικογενειακό ιστορικό αυτοάνοσης θυρεοειδικής νόσου, θετικό οικογενειακό ή ατομικό ιστορικό αυτοάνοσης νόσου, σύνδρομο Down, σύνδρομο Turner) |
| Εμμένουσα αύξηση TSH σε υποξεία θυρεοειδίτιδα, θυρεοειδίτιδα μετά τον τοκετό, ανώδυνη θυρεοειδίτιδα |
| Τραυματικά αίτια: μερική θυρεοειδεκτομή ή άλλη χειρουργική παρέμβαση στην περιοχή του τραχήλου, εξωτερική ακτινοβόληση στις περιοχές της κεφαλής και του τραχήλου, θεραπεία με ραδιενεργό ιώδιο |
| Φάρμακα: ιώδιο ή που περιέχουν ιώδιο (αμιωδαρόνη, σκιαγραφικοί παράγοντες) λίθιο, κυτοκίνες, σουλφοναμίδες, σουλφονυλουρίες, αμινογλουταμίδη, εθειοναμίδη |
| Ανεπαρκής θεραπεία υποκατάστασης για κλινικό υποθυρεοειδισμό (ανεπαρκής δοσολογία, μη συμμόρφωση, αλληλεπίδραση με άλλα φάρμακα, αυξημένη clearance Τ4, δυσαπορρόφηση) |
| Διηθητικά νοσήματα (αμυλοείδωση, σαρκοείδωση, αιμοχρωμάτωση, θυρεοειδίτιδα Riedel, κυστίνωση, AIDS, πρωτοπαθές θυρεοειδικό λέμφωμα) |
| Κεντρικός υποθυρεοειδισμός με διαταραγμένη δραστικότητα TSH |
| Τοξικά παράγωγα, βιομηχανικοί και περιβαλλοντικοί παράγοντες |
| Μεταλλάξεις του υποδοχέα της TSH |
3. Διαφορική διάγνωση
Είναι σημαντικό να λαμβάνουμε υπόψη μας ορισμένες παραμέτρους που μπορεί να οδηγήσουν σε ελαφρά αύξηση των τιμών της TSH χωρίς αυτό να συνεπάγεται εξελισσόμενη θυρεοειδική λειτουργία όπως:
3.1. Κατανομή της TSH στο γενικό πληθυσμό
Στην επιδημιολογική μελέτη NHANES I I I (National Health and Nutrition Examination Survey) που διενεργήθηκε στις ΗΠΑ μεταξύ 1988-1994, σε δείγμα 17335 ατόμων (στατιστικά αντιπροσώπευε 200×106 άτομα ηλικίας άνω των 12 ετών) η διάμεση τιμή της TSH όσο και τα ανώτερα όρια αναφοράς της, τόσο στον ελεύθερο θυρεοειδικής νόσου πληθυσμό όσο και στον πληθυσμό αναφοράς, παρουσιάζουν σταδιακή άνοδο με την πρόοδο της ηλικίας (Πίνακας 2).
Πίνακας 2. Επίπεδα TSH ανάλογα με τις υποομάδες ηλικιών, σύμφωνα με τη μελέτη NHANES III [μεταφρασμένο από Hollowell JG et al (15)].
|
N |
TSH (mU/L) median |
P 2,5 – P 97,5 |
|
| 1. Συνολικός πληθυσμός >12 ετών |
17353 |
1,49 |
0,33-5,80 |
| 2. Ελεύθερος νόσου πληθυσμός (1) |
16533 |
1,49 |
0,44-5,52 |
| 3. Πληθυσμός αναφοράς (2) |
13344 |
1,39 |
0,45-4,12 |
| 12 – 19 ετών |
1,35 |
0,46-4,07 |
|
| 20 – 29 ετών |
1,26 |
0,40-3,56 |
|
| 30 – 39 ετών |
1,29 |
0,42-3,69 |
|
| 40 – 49 ετών |
1,40 |
0,50-3,82 |
|
| 50 – 59 ετών |
1,50 |
0,52-4,03 |
|
| 60 – 69 ετών |
1,67 |
0,49-4,33 |
|
| 70 – 79 ετών |
1,76 |
0,45-5,90 |
|
| > 80 ετών |
1,90 |
0,33-7,50 |
|
| (1) αποκλεισμός ασθενών που ανέφεραν θυρεοειδική νόσο, βρογχοκήλη ή λάμβαναν ήδη αγωγή(2) περαιτέρω αποκλεισμός λόγω κύησης, λήψης οιστρογόνων, ανδρογόνων, λιθίου, θετικών αντιθυρεοειδικών αντισωμάτων, χημικού υπο- και υπερθυρεοειδισμού | |||
Επίσης και το ποσοστό των ατόμων σε όλες τις υποομάδες που είχαν τιμή TSH άνω των 4,5 mU/L που θεωρούνταν γενικά ως οι ανώτερες τιμές αναφοράς παρουσίαζε προϊούσα αύξηση (Εικόνα 1).
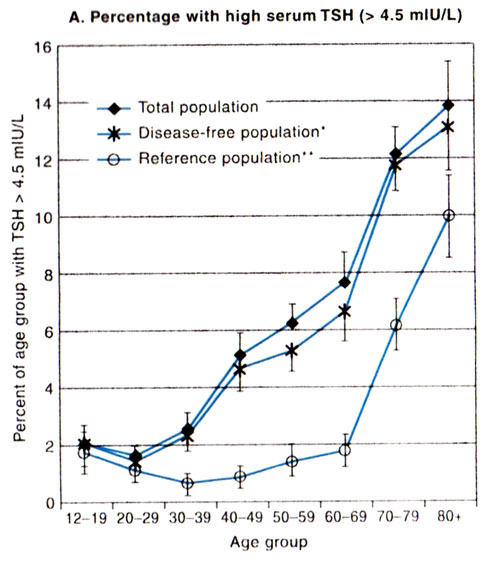
Εικόνα 1. Ποσοστά ατόμων ανάλογα με την ηλικία, που έχουν τιμή TSH > 4,5 mU/L, σύμφωνα με τη μελέτη NHANES III [Hollowell et al (15)].
Είναι ενδιαφέρον ότι οι γυναίκες έχουν σημαντικά υψηλότερες τιμές TSH από τους άνδρες σε όλες σχεδόν τις ηλικιακές υποομάδες άνω των 30 ετών (Εικόνα 2). Η κατανομή τόσο των αριθμητικών, όσο και των λογαριθμικών τιμών της TSH στον πληθυσμό αναφοράς (π.χ άτομα χωρίς ιστορικό θυρεοειδοπάθειας, λήψης φαρμάκων και χωρίς αντιθυρεοειδικά αντισώματα) στη συγκεκριμένη μελέτη ήταν μη κανονική (κωδωνοειδής) με απόκλιση στα ανώτερα όρια τιμών της TSH (Εικόνα 3). Παρόμοια απόκλιση των καμπυλών κατανομής της TSH όσο αυξάνεται η ηλικία παρατηρείται και στη νεότερη παρουσίαση των δεδομένων της ίδιας μελέτης (Εικόνα 4).

Εικόνα 2. Επίπεδα TSH σε ελεύθερο νόσου πληθυσμό, με ή χωρίς παράγοντες κινδύνου ανάλογα με το φύλο, σύμφωνα με τη μελέτη NHANES ΙΙΙ [Hollowell et al (15)].

Εικόνα 3. Ποσοστιαία κατανομή των αριθμητικών (α) και λογαριθμικών (β) τιμών της TSH σύφωνα με τη μελέτη NHANES III [Hollowell et al (15)].

Εικόνα 4. Ποσοστιαία κατανομή των τιμών της TSH ανάλογα με την ηλικία στην παλαιότερη εκδοχή της μελέτης NHANES III (15) και στη νεότερη (128). NHANES III vs NHANES 99-02 (A) ελεύθερος νόσου πληθυσμός (Β) πληθυσμός αναφορά Μεταφρασμένο από Hollowell et al (15), Surks et al (128)
Τα ευρήματα της μελέτης NHANES III σχετικά με τη συχνότητα του ΥΥΘ φαίνεται πως επιβεβαιώνονται και από αντίστοιχα δεδομένα άλλων μελετών από διαφορετικές χώρες. Σε μελέτες χρονικής στιγμής με διαφορετική προέλευση, αριθμό εξετασθέντων, φύλο, ηλικία, επάρκεια ιωδίου και κριτήρια ορισμού ΥΥΘ διαπιστώθηκαν ποσοστά ανεύρεσης αυξημένων τιμών TSH που κυμαίνονταν από 1,4-7,8% σε μικτό πληθυσμό, τα οποία αυξάνονται σε άτομα άνω των 60 ετών. Στις γυναίκες κυμαίνονται από 7,8-17,5% και στους άνδρες 2,2-15,4% (Πίνακας 3). Στη μελέτη Wichamm σε πληθυσμό 2779 Βρετανών τα ποσοστά ανεύρεσης τιμής TSH άνω των 6,0 mU/L στους μεν άνδρες παρέμειναν σχεδόν σταθερά με την πρόοδο της ηλικίας, στις δε γυναίκες παρατηρήθηκε σταθερή αύξηση των ποσοστών που έφτασε ως το 18% σε άτομα ηλικίας άνω των 74 ετών (22) (Εικόνα 5). Παρόμοια είναι και τα αποτελέσματα της μεγαλύτερης μελέτης χρονικής στιγμής Colorado όπου το μέσο ποσοστό ανεύρεσης αυξημένης TSH ήταν 9,5% στο σύνολο του πληθυσμού και στα άτομα άνω των 74 ετών ήταν 16 και 21% σε άνδρες και γυναίκες αντίστοιχα (17).
Πίνακας 3. Ποσοστά ανίχνευσης αυξημένης τιμής TSH σε άτομα >60 ετών (μελέτες χρονικής στιγμής).
| Βιβλιογραφία |
Έτος |
Προέλευση |
Ν ασθενών |
Ηλικία |
% αύξηση TSH |
|||
|
1 |
Falkenberg M et al (111) |
1983 |
Ryral Swedin |
1442 |
>60 |
1,4 |
♂+♀: 1,4-7,8 % | |
|
2 |
Sawin C et al (112) |
1985 |
Framinghan |
2139 |
>60 |
7,8 |
||
|
3 |
Bagchi N et al (113) |
1990 |
Michigan |
968 |
≥55 |
6,7 |
||
|
4 |
Mariotti S et al (114) |
1993 |
Italy |
41 |
>100 |
7,1 |
||
|
5 |
Manciet G et al (115) |
1995 |
France |
425 |
≥65 |
4,2 |
||
|
6 |
Luboshitzky R et al (116) |
1996 |
Israel |
751 |
≥65 |
4,9 |
||
|
♀ |
♂ |
|||||||
|
7 |
Sawin C et al (117) |
1979 |
Massachusetts |
344 |
≥65 |
16,9 |
8,2 |
♀: 7,8 – 17,5 %♂: 2,2 – 15,4 % |
|
8 |
Livingston E et al (118) | 1987 | California | >60 | 5,1 | |||
|
9 |
Rosenthal M et al (119) | 1987 | New Mexico | 258 | >60 | 16,2 | 9,5 | |
|
10 |
Brochmann H et al (120) | 1988 | Norway | 194 | >70 | 7,0 | 2,8 | |
| 11 | Drinka P et al (121) | 1990 | Wisconsin | 571 | ≥60 | 14,6 | 9,7 | |
| 12 | Parke J et al | 1990 | Great Britain | 194 | >70 | 9,5 | 2,2 | |
| 13 | Bemben D et al (122) | 1994 | Oklahoma | 283 | ≥60 | 14,6 | 15,4 | |
| 14 | Jayme J et al (123) | 1994 | Maryland | 3410 | >60 | 17,5 | 13,7 | |

Εικόνα 5. Ποσοστά ανεύρεσης τιμής TSH >6 mU/L σε γυναίκες και άντρες σύμφωνα με τη μελέτη Wickham Vanderpump MP et al (22).
Υπάρχουν επίσης 4 προοπτικές μελέτες για την επίπτωση του ΥΥΘ σε ηλικιωμένα άτομα τα οποία είχαν φυσιολογικές τιμές TSH στην έναρξη της μελέτης. Το χρονικό διάστημα παρακολούθησης κυμαινόταν από 4-20 έτη. Ευθυρεοειδικά άτομα με θετικό τίτλο αντιθυρεοειδικών αντισωμάτων (ΑΤΑ) εμφάνισαν ετήσιο ρυθμό μετάπτωσης σε υποκλινικό ή έκδηλο υποθυρεοειδισμό τουλάχιστον 20%, ενώ εκείνα με αρνητικά ΑΤΑ εμφάνισαν μικρότερο ρυθμό (πίνακας 4).
Πίνακας 4. Εμφάνιση υποκλινικού υποθυρεοειδισμού στους ηλικιωμένους ανάλογα με την εμφάνιση ή όχι αυτοαντισωμάτων (προοπτικές μελέτες).
|
|
Βιβλιογραφία |
Έτος |
Νο ασθενών |
Διάρκεια |
% αύξηση TSH |
|
|
+Abs |
-Abs |
|||||
|
1 |
Rosenthal M et al |
1987 |
1758 |
6 χρ. |
23 |
1,7 |
|
2 |
Hawkins B et al (124) |
1980 |
24 |
4 χρ. |
8,3 |
0 |
|
3 |
Geul K et al (125) |
1993 |
427 ♀ |
10 χρ. |
24 |
3 |
|
4 |
Vanderpump M et al (22) |
1995 |
942 ♀ |
20 χρ. |
2,1 |
0,3 |
Μελέτες χρονικής στιγμής δείχνουν ότι το ποσοστό ανίχνευσης θετικών ΑΤΑ κυμαίνεται από 15-20% στα ηλικιωμένα άτομα και 40-67% σε άτομα με ΥΥΘ (22, 23). Ενδιαφέρον παρουσιάζει επίσης η ποσοστιαία αύξηση των ΑΤΑ που βαίνει αυξανόμενη με την ηλικία, με την κλιμακωτή ωστόσο αύξηση της TSH να παραμένει εντός των φυσιολογικών ορίων (Πίνακας 5).
Πίνακας 5. Συχνότητα ανίχνευσης αυτοαντισωμάτων ανάλογα με την κλιμάκωση της τιμής της TSH [Vanderpump MP et al, Samuels MH et al (22, 23)].
|
TSH (mIU/L) |
|||||
|
Ηλικία (έτη) |
1 |
2 |
3 |
4 |
5 |
|
20 |
1 6 |
1 6 |
3 13 |
4 21 |
7 29 |
|
30 |
1 8 |
2 8 |
3 17 |
6 26 |
8 35 |
|
40 |
2 10 |
2 11 |
4 21 |
7 32 |
11 42 |
|
50 |
2 13 |
3 13 |
5 25 |
9 38 |
14 48 |
|
60 |
3 17 |
3 17 |
7 31 |
12 44 |
17 55 |
|
70 |
4 21 |
4 21 |
9 37 |
15 51 |
21 62 |
3.2. Η αξιοπιστία και η διακύμανση της TSH
Όπως συμβαίνει σε κάθε μεταβλητή, έτσι και στις παραμέτρους θυρεοειδικής λειτουργίας υπάρχει μια διακύμανση των τιμών που ποικίλλει ανάλογα με τη μεθοδολογία, το πρωτόκολλο, τις τεχνικές δυνατότητες κλπ. Έτσι η λεγόμενη διεργαστηριακή αναλυτική διακύμανση (interassay CV) για την TSH συγκεκριμένα ανέρχεται στο 10%, ενώ η ενδο-ατομική και δια-ατομική διακύμανση στο 30 και70% αντίστοιχα (σύμφωνα με το Νational Αcademy of Clinical Biochemistry).
Ο λόγος ενδο- προς δια-ατομική διακύμανση (θα μπορούσε να ονομασθεί και δείκτης ατομικότητας) μπορεί να χρησιμοποιηθεί προκειμένου να καθορίσει την χρησιμότητα πληθυσμιακών τιμών αναφοράς στην ανίχνευση μιας νόσου σε ένα συγκεκριμένο άτομο. Όταν ο λόγος είναι μικρότερος από 0,6 τα πληθυσμιακά όρια αναφοράς είμαι μη ευαίσθητη μέτρηση στην πλειονότητα των ατόμων.
Ο δείκτης αυτός σε 3 μελέτες κυμαινόταν από 0,36-0,5 (12,24,25). Σε ενδιαφέρουσα μελέτη των Andersen και συν οι οποίοι μέτρησαν τις μεταβολές των θυρεοειδικών ορμονών σε 16 υγιείς άνδρες κάθε μήνα μετρήσεις, για 12 μήνες, βρήκαν ότι η τιμή της TSH κάθε ατόμου κυμαινόταν στο 50% της διακύμανσης στο σύνολο των ατόμων (24). Έτσι με μέση τιμή TSH π.χ 1,4 mU/L οι επαναλαμβανόμενες στο ίδιο άτομο μπορεί να ποικίλλουν από 0,7-2,1 mU/L, ενώ αν ήταν 3,6 mU/L τα όρια διακύμανσης θα ήταν 1,8-5,4 mU/L. Γίνεται εμφανές από το δεύτερο παράδειγμα ότι οι τιμές αυτές θα μπορούσαν να ταξινομήσουν ασθενείς λανθασμένα ως πάσχοντες παρότι οι μέσες διαχρονικές συγκεντρώσεις στο ίδιο άτομο είναι εντελώς φυσιολογικές. Ένας επιπλέον παράγοντας που συμβάλλει σε ενδεχόμενη λανθασμένη εκτίμηση είναι και η ημερήσια διακύμανση των τιμών της TSH που ανέρχεται στο 26,5% με υψηλότερα τα πρωινά επίπεδα, καθώς και η επίδραση της λήψης φαγητού που μειώνει τα επίπεδά της (24). Συμπερασματικά όσο πιο στενό το παράθυρο των ορίων αναφοράς τόσο πιο μεγάλη η πιθανότητα παραπλανητικού αποτελέσματος.
3.3. Η φυσιολογία της λειτουργίας του υποθαλαμο-υποφυσιακού- θυρεοειδικού άξονα-περιφερικών ιστών στόχων και επίδραση της ηλικίας σε αυτόν
Έχει παρατηρηθεί ότι διάφοροι παράγοντες καθώς και η πρόοδος ηλικίας μπορεί να ασκήσουν δράση στα επιμέρους επίπεδα του άξονα, όπως φαίνεται στις εικόνες 6 και 7 αντίστοιχα, η οποία εκδηλώνεται ως εργαστηριακή διαταραχή ή ως ιστικός υποθυρεοειδισμός (26-29).

Εικόνα 6. Μεταβολές του Υ-Υ-Θ άξονα κατά το γήρας.

Εικόνα 7. Μεταβολές των παραμέτρων θυρεοειδικής οικονομίας με την ηλικία.
3.4. Επίδραση της μη θυρεοειδικής νόσησης στην θυρεοειδική οικονομία
Σε καταστάσεις σοβαρής μη θυρεοειδικής νόσησης είναι δυνατόν να εμφανισθούν σημαντικές συνέπειες στις παραμέτρους της θυρεοειδικής λειτουργίας και μάλιστα αυτές βαίνουν ανάλογα με τη βαρύτητα της νόσησης. Όσο βαρύτερη είναι αυτή τόσο πιο χαμηλά ανευρίσκονται τα επίπεδα των ΘΟ και ιδιαίτερα της Τ3 (low T3 syndrome) ενώ παράλληλα αυξάνονται τα επίπεδα της ανάστροφης Τ3 (30) (Εικόνα 8). Η παράλληλη πτώση και της Τ4 είναι κακός προγνωστικός δείκτης έκβασης της νόσου (31, 32).

Εικόνα 8. Μη – θυρεοειδική νόσηση και θυρεοειδική οικονομία.
3.5. Επίδραση φαρμάκων στον άξονα
Διάφορα φάρμακα ή ουσίες μπορούν να επηρεάσουν τη λειτουργικότητα του θυρεοειδικού άξονα σε πολλαπλά επίπεδα και να οδηγήσουν σε σημαντική μεταβολή των επιπέδων των ΘΟ και της TSH όπως φαίνεται στον πίνακα 6 (29).
Πίνακας 6. Επίδραση φαρμάκων στον θυρεοειδικό άξονα (μεταφρασμένο από Mooradian et al (29)].
| Φαρμακευτική ουσία |
Επίδραση στον θυρεοειδικό άξονα |
| Κορτικοστεροειδή, ντοπαμίνη, οκτρεοτίδη |
TSH |
| Αμιωδαρόνη, ιωδιούχα |
T4 |
| Λίθιο, αμιωδαρόνη, ιωδιούχα |
¯ T4 |
| Οιστρογόνα, ταμοξιφαίνη, μεθαδόνη, ηρωίνη, φλουοροουρακήλη |
TBG |
| Ανδρογόνα, αναβολικά, κορτικοστεροειδή, νιασίνη |
¯ TBG |
| Ηπαρίνη, φουροσεμίδη, σαλικυλικά, κ.α. |
¯ δέσμευσης TBG |
| Φαινυντοϊνη, βαρβυτουρικά, ριφαμπικίνη, καρβαμαζεπίνη |
Ηπατικός μεταβολισμός |
| Προπυθειουρακήλη, αμιοδαρόνη, β’-ανταγωνιστές, κορτικοστεροειδή |
¯ 5’ –TDI |
| Χολυστεραμίνη, χολεστυπόλη, Al, Fe |
¯ Απορρόφηση Τ4 |
| Ιντερφερόνη-α, ιντερλευκίνη-2 |
Τ4 ή ¯ Τ3,Τ4 |
3.6. Άλλα αίτια
Στον πίνακα 7 παρουσιάζονται διάφορα αίτια που μπορούν να οδηγήσουν στην ανεύρεση τιμών TSH στα όρια του ΥΥΘ (11).
Επιπλέον πρέπει να λαμβάνεται υπ’ όψιν ότι η ΤSH είναι υψηλότερη στα υπέρβαρα-παχύσαρκα άτομα σε σχέση με τα νορμοβαρή ή αδύνατα άτομα, ιδιαίτερα σε αυτά με αρνητικά ΑΤΑ. Η διαταραχή αυτή είναι αναστρέψιμη με την απώλεια βάρους (33).
Πίνακας 7. Aίτια αυξημένων τιμών TSH [μεταφρασμένο από Wartofsky et al (11)].
| Αίτια |
| Θυρεοειδίτιδα Hashimoto Φάρμακα (στεροειδή, ντοπαμίνη, ιωδιούχα, αμιωδαρόνη κ.α.) Οικ. ιστορικό υποθυρεοειδισμού σε μεγάλη ηλικία Μη-θυρεοειδική νόσηση Κύηση Φάση ανάνηψης από υποξεία θυρεοειδίτιδα Άλλα αυτοάνοσα νοσήματα Ετερόφυλα αντισώματα Βιολογικά μη-δραστική TSH, αντίσταση στην TSH Μεταλλάξεις υποδοχέα TSH Αντίσταση στις θυρεοειδικές ορμόνες Όγκοι υπόφυσης εκκρίνοντες TSH |
4. Εξέλιξη – φυσική πορεία νόσου
Ο ΥΥΘ μπορεί να είναι μια αναστρέψιμη ή μια προοδευτικά εξελισσόμενη κατάσταση προς τον έκδηλο υποθυρεοειδισμό. Η αυξημένη πρόσληψη ιωδίου σχετίζεται με αυξημένο κίνδυνο εξέλιξης σε έκδηλο υποθυρεοειδισμό (14). Άτομα χωρίς αυτοάνοση θυρεοειδίτιδα είναι δυνατόν να εμφανίζουν διαλείπουσα αύξηση των επιπέδων της TSH. Τα επίπεδα συνήθως επανέρχονται στα φυσιολογικά όρια ιδιαίτερα όταν οι τιμές της TSH βρίσκεται στο φάσμα τιμών 4,0-8,0 mU/L, ενώ η πιθανότητα αυτή μειώνεται όταν οι τιμές βρίσκονται μεταξύ 8,0-15,0 mU/L.
Ενδιαφέρον παρουσιάζουν 4 προοπτικές μελέτες στις οποίες ελέγχθηκε ο ρυθμός μετάπτωσης του ΥΥΘ σε κλινικό υποθυρεοειδισμό σε ηλικιωμένα. Ο χρόνος παρακολούθησης κυμαίνεται από 1-20 έτη, με μεγαλύτερο αυτόν της μελέτης Whickham. Οι παρατηρήσεις αυτών των μελετών υποδεικνύουν ότι άτομα με ΥΥΘ εμφανίζουν ετήσιο ρυθμό προόδου σε κλινικό υποθυρεοειδισμό 2-3% (Πίνακας 8). Ο ρυθμός αυτός είναι ιδιαίτερα αυξημένος (4,3%) στις γυναίκες με αυξημένη τιμή TSH και θετικά ΑΤΑ (14,34-36). Η αρχική τιμή της TSH φαίνεται ότι αποτελεί τον πιο ισχυρό προγνωστικό παράγοντα εξέλιξης σε έκδηλο υποθυρεοειδισμό. Άλλοι προγνωστικοί παράγοντες είναι η παρουσία συμπτωμάτων υποθυρεοειδισμού, η παρουσία βρογχοκήλης και θετικών ΑΤΑ καθώς και η χαμηλή (κατώτερα φυσιολογικά όρια) τιμή της FT4 (37). Ενδιαφέρον εύρημα είναι η αποκατάσταση των επιπέδων της TSH στα φυσιολογικά όρια σε ποσοστό 37% μετά από ένα μέσο χρονικό διάστημα παρακολούθησης 31,7 μηνών. Όπως έδειξαν επιπλέον τα ευρήματα της ίδιας μελέτης από τις 7 παραμέτρους κινδύνου που ελέγχθηκαν με βαθμιδωτή μονο- και πολυπαραγοντική συσχέτιση η μόνη παράμετρος που έχει σημαντική επίπτωση στην εξέλιξη του ΥΥΘ σε έκδηλο υποθυρεοειδισμό, ήταν η αρχική τιμή της TSH. Αντίθετα, πολύ μικρότερη επίδραση είχαν η τιμή της FT4, των αντι-TPO abs και η παρουσία βρογχοκήλης ή συμπτωμάτων (Εικόνα 9) (37).
Πίνακας 8. Μετάπτωση υποκλινικού υποθυρεοειδισμού σε κλινικό στους ηλικιωμένους (προοπτικές μελέτες).
| Βιβλιογραφία |
Έτος |
Προέλευση |
Νο ασθενών |
Διάρκεια |
Έκβαση ΥΠΟ – |
|
|
1 |
Gordin A et al (126) |
1981 |
Φινλανδία |
8 |
3 – 9 χρ. |
88% |
|
2 |
Parle J et al |
1991 |
Βρετανία |
73 |
≥ 1 χρ. |
18% |
|
3 |
Vanderpump M et al (22) |
1995 |
Βρετανία |
942 ♀ |
20 χρ. |
2,6% (- Abs), 4,3 (+ Abs) |
|
4 |
Huber G et al |
1997 |
Ελβετία |
154 ♀ |
10 χρ. |
4,3% |

Εικόνα 9. Εξέλιξη υποκλινικού υποθυρεοειδισμού σε έκδηλο ανάλογα με διάφορους παράγοντες Diez JJ et al (37).
5. Κλινική – βιολογική σημασία ΥΥΘ
5.1. Εξέλιξη σε έκδηλο-κλινικό υποθυρεοειδισμό
Όπως ήδη αναφέρθηκε σε ένα σημαντικό ποσοστό ασθενών ο ΥΥΘ εξελίσσεται σε έκδηλο υποθυρεοειδισμό. Ιδιαίτερα σε ασθενείς άνω των 55 ετών ο κίνδυνος υπολογίζεται ως και 8% ανά έτος (28).
5.2. Συστηματικά συμπτώματα ΥΥΘ
H απόφαση θεραπευτικής αντιμετώπισης του ΥΥΘ βασίζεται συχνά στην εκτίμηση της κλινικής συμπτωματολογίας της νόσου. Κατά καιρούς έχουν αναπτυχθεί και προταθεί διάφορες μέθοδοι εκτίμησης των σημείων-συμπτωμάτων του ΥΥΘ ή εκτίμησης της νοητικής και ψυχικής υγείας ή της ποιότητας ζωής αυτών των ασθενών. Ένα επιπλέον στοιχείο που έχει μεταβάλλει την κλινική εικόνα του υποθυρεοειδισμού είναι το γεγονός ότι τα τελευταία χρόνια διαγιγνώσκεται σε πολύ πρώιμο στάδιο, ενώ παλαιότερα η κλινική εκτίμηση βασιζόταν στις εκδηλώσεις της σοβαρής και μακροχρόνιας νόσου. Αυτό στην πράξη σημαίνει ότι οι παλιές κλινικές μέθοδοι εκτίμησης της νόσου είναι ατελέσφορες. Δύο επιπλέον στοιχεία που καθιστούν δυσχερή την κλινική εκτίμηση είναι πρώτον ότι σημεία και συμπτώματα υποθυρεοειδισμού ανευρίσκονται συχνά σε άτομα με φυσιολογική θυρεοειδική λειτουργία ή τοξικό αδένωμα (38-40) και δεύτερον η αλληλοεπικάλυψη συμπτωμάτων από την ψυχική σφαίρα (π.χ κατάθλιψη) με εκείνα του υποθυρεοειδισμού (41,42). Στην τελευταία δε περίπτωση η συχνότερη ανεύρεση αντιθυρεοειδικών αντισωμάτων (20 vs 5%) δυσχεραίνει επιπλέον τη διαφορική διάγνωση (43).
Χρησιμοποιώντας ένα άθροισμα 14 κλινικών συμπτωμάτων-σημείων εκτίμησης της θυρεοειδικής υπολειτουργίας οι Zulewski και συν. βρήκαν μια καλή συσχέτιση του ‘score’ με την FT4 και την TSH σε ασθενείς με ΥΥΘ (44). Σε νεότερη ωστόσο μελέτη μεταξύ 1423 γυναικών ηλικίας 16-75 ετών τόσο ο δείκτης ‘short form 36’ (SF-36) όσο και ο δείκτης καλής ψυχικής κατάστασης (psychological general well being index-PGWI) που χρησιμοποιήθηκαν ως δείκτες ποιότητας ζωής σχετιζόμενης με την καλή υγεία δε διαπίστωσαν σημαντικές διαφορές μεταξύ ατόμων με ή χωρίς ΥΥΘ (τιμή TSH>4,0 mU/L) (45).
Η παρουσία ή μη συμπτωμάτων σε ασθενείς με ΥΥΘ εκτιμήθηκε και σε δύο άλλες μελέτες με χρονική διαφορά 18 ετών. Στην πρώτη οι ασθενείς με ΥΥΘ εμφάνιζαν υψηλότερη συχνότητα υποθυρεοειδικών συμπτωμάτων συγκριτικά με τους ιδίου φύλου και ηλικίας ευθυρεοειδικούς μάρτυρες (46). Στη δεύτερη βρέθηκε ότι τα πιο συχνά συμπτώματα που εμφάνιζαν οι γυναίκες με ΥΥΘ ήταν το αίσθημα κόπωσης (83%) και η αύξηση του βάρους σώματος (80%) (47).
Σε μια πρόσφατη τέλος μελέτη, η οποία είναι μέχρι στιγμής η μεγαλύτερη προοπτική πληθυσμιακή μελέτη εξέλιξης του ΥΥΘ, μεταξύ 3996 ατόμων άνω των 65 ετών που παρακολουθήθηκαν για 4 έτη διαπιστώθηκαν τα ακόλουθα: επιμονή του ΥΥΘ σε ποσοστό 56% στα 2 και 4 έτη, η ύφεση του ΥΥΘ στα 2 έτη ήταν πιο συχνή στα άτομα με επίπεδα TSH μεταξύ 4,5-6,9 mU/L (46% vs 10% εκείνων με επίπεδα TSH 7,0-8,9 mU/L και 7% εκείνων που είχαν επίπεδα > 10,0 mU/L, p<0,001). Επιπλέον η απουσία TPOAbs συνοδεύονταν συχνότερα με υφέσεις του ΥΥΘ (48 vs 15% εκείνων με θετικά TPOAbs, p<0,001). Υψηλότερα επίπεδα της TSH και θετικά TPOAbs αποτελούν ανεξάρτητους παράγοντες μη ύφεσης (p<0,05) (17). Τιμές TSH=10,0 mU/L ή υψηλότερες ήταν επίσης ανεξάρτητος παράγοντας προόδου σε έκδηλο υποθυρεοειδισμό (p<0,05) (17). Η μετάπτωση σε ευθυρεοειδισμό ή υποκλινικό υποθυρεοεδισμό ήταν συχνή στα 2 και 4 έτη, ενώ τέλος η ηλικία και το φύλο δεν επηρέαζαν αυτή τη μετάπτωση (48).
Συμπερασματικά η παρουσία σημείων–συμπτωμάτων σε καταστάσεις ΥΥΘ παραμένει αμφιλεγόμενη. Είναι δύσκολη η κλινική διάκριση μεταξύ ευθυρεοειδικών και ασθενών με ΥΥΘ. Επιπλέον πολλά από τα συμπτώματα-σημεία είναι μη ειδικά και ανευρίσκονται συχνά σε άλλες καταστάσεις ιδιαίτερα σε άτομα μεγαλύτερης ηλικίας, στα οποία επιπλέον οι τυπικές εκδηλώσεις του υποθυρεοειδισμού ανευρίσκονται λιγότερο συχνά και όταν υπάρχουν αποδίδονται συνήθως σε συνοσηρότητα, κατάθλιψη, φαρμακευτική συνεπίδραση ή στη ίδια την ηλικία (49,50). Τέλος ένα σημείο που χρήζει ιδιαίτερης προσοχής είναι ότι οι ασθενείς που αναφέρουν περισσότερα συμπτώματα και ιδίως όταν εμφανίζονται σε βραχύ χρονικό διάστημα, έχουν μεγαλύτερη πιθανότητα να εμφανίσουν έκδηλη νόσο (17).
5.3. Μεταβολικές και καρδιαγγειακές επιπτώσεις ΥΥΘ
Όπως έχει φανεί από πολλές σχετικές μελέτες ο μακροχρόνιος μη θεραπευόμενος ΥΥΘ δυνατόν να σχετίζεται με σημαντικές μεταβολικές και καρδιαγγειακές επιπτώσεις (51-53) όπως φαίνεται παραστατικά στην εικόνα 10. Οι επιπτώσεις αυτές δυνατόν να αυξάνουν την καρδιαγγειακή νοσηρότητα και θνητότητα.
Στη γνωστή μελέτη Colorado οι ασθενείς με ΥΥΘ εμφανίζουν υψηλότερα επίπεδα ολικής χοληστερόλης σε σχέση με τους ευθυρεοειδικούς (224 έναντι 216 mg/dl) (17). Επιπλέον αρκετές τυχαιοποιημένες μελέτες έχουν δείξει μείωση των επιπέδων της LDL-χοληστερόλης μετά την χορήγηση LT4. Ωστόσο στις περισσότερες δεν έγινε κατηγοριοποίηση των αποτελεσμάτων ανάλογα με την τιμή της TSH στο φάσμα των τιμών τουΥΥΘ (5 – 10 mU/L). Σε σχετική μετα-ανάλυση που περιελάμβανε 13 μελέτες διαπιστώθηκε σχετικό όφελος στη μεταβολική εικόνα από τη χορήγηση LT4 (54). Σε γενικές γραμμές αυτό που εξάγεται ως μήνυμα από τις διάφορες μελέτες είναι ότι ο ΥΥΘ σχετίζεται με δυσλιπιδαιμία, ιδιαίτερα με αύξηση της ολικής και LDL-χοληστερόλης, ενώ τα δεδομένα αναφορικά με την HDL-χοληστερόλη, τα τριγλυκερίδια και την Lp(a) δε δείχνουν σαφή συσχέτιση με τον ΥΥΘ (53, 55, 56). Ενώ επιπλέον, σε σχετική ανασκόπηση του 2004 δε βρέθηκε όφελος από την χορήγηση LT4 (3). Αυτό ωστόσο που φαίνεται πιο σαφές είναι ότι η λιπιδαιμική εικόνα είναι πιο επηρεασμένη σε άτομα με σοβαρότερο ΥΥΘ (TSH > 10 mU/L), στους καπνιστές και στους ασθενείς που εμφανίζουν συγχρόνως ινσουλινοαντίσταση (53, 55, 56).

Εικόνα 10. Σχηματική απεικόνιση των παραγόντων καρδιαγγειακού κινδύνου σε ασθενείς με μακροχρόνιο μη-αντιμετωπιζόμενο ΥΥΘ.
Όσον αφορά σε άλλους ‘μη παραδοσιακούς’ παράγοντες κινδύνου για καρδιαγγειακή νόσο, όπως τα αυξημένα επίπεδα C-αντιδρώσας πρωτεϊνης (CRP), της ομοκυστεϊνης και της Lp(a) δε φαίνεται να υπάρχει συσχέτιση με τον ΥΥΘ (56,57). Όσον αφορά στη συσχέτιση του ΥΥΘ με την καρδιαγγειακή νόσο (ΚΑΝ) έχει εκτιμηθεί σε αρκετές επιδημιολογικές μελέτες. Στη μελέτη Rotterdam μεταξύ 1149 γυναικών άνω των 55 ετών διαπιστώθηκε συσχέτιση του ΥΥΘ και του εμφράγματος του μυοκαρδίου (διπλάσιος κίνδυνος) καθώς και της αποτιτάνωσης της αορτής (58). Σε μεγάλη νορβηγική μελέτη (25000 άτομα ηλικίας 60 ετών, διάρκεια παρακολούθησης 8,3 έτη), τα επίπεδα της TSH σχετίζονταν θετικά με την ολική καρδιαγγειακή θνητότητα στις γυναίκες αλλά όχι στους άνδρες (59). Η μελέτη NAHS (Nagasaki Adult Health Study -2856 μεσήλικες άνδρες επιβιώσαντες από την ατομική βόμβα) ωστόσο έδειξε αυξημένο κίνδυνο ΚΑΝ (60). Στη μελέτη Wickham δε διαπιστώθηκε αυξημένη θνητότητα από ΚΑΝ κατά τα 20 έτη παρατήρησης (61). Σε μια πρόσφατη επανεπεξεργασία των δεδομένων της ίδιας μελέτης (97 άτομα, μέσης ηλικίας 49 έτη) βρέθηκε σημαντικά υψηλότερη αρτηριακή πίεση στις γυναίκες με ΥΥΘ καθώς και επίπεδα ολικής, LDL-χοληστερόλης και ομοκυστεϊνης σε σχέση με τις γυναίκες με φυσιολογικές τιμές TSH. Διαπιστώθηκε επίσης θετική συσχέτιση μεταξύ ΥΥΘ και κινδύνου ισχαιμικής ΚΑΝ (62). Στη μελέτη Busseltron από την Αυστραλία (3447 άτομα, μέσης ηλικίας 49,8 έτη) βρέθηκε συσχέτιση των επιπέδων της TSH με αυξημένο κίνδυνο ΚΑΝ τόσο στην ανάλυση χρονικής στιγμής όσο και στην προοπτική ανάλυση (20 έτη) των δεδομένων (63). Άλλες μελέτες ωστόσο δεν έδειξαν αυξημένο σχετικό κίνδυνο ΚΑΝ (61,64-66). Η διακύμανση αυτή των αποτελεσμάτων των προαναφερθεισών μελετών αναφορικά με τον κίνδυνο ΚΑΝ προφανώς έγκειται στους διαφορετικούς προς μελέτη πληθυσμούς (αριθμός, ηλικία, φύλο, φυλή/εθνικότητα, τρόπος ζωής) καθώς και στα όρια ορισμού του ΥΥΘ, στα επίπεδα της TSH, στη μέθοδο εκτίμησης της ΚΑΝ, στη μη ομοιογενή συνεκτίμηση γνωστών παραγόντων κινδύνου και στη διάρκεια παρατήρησης. Επιπλέον αρκετές μελέτες δε συμπεριελάμβαναν παραμέτρους εκτίμησης θυρεοειδικής λειτουργίας κατά τον επανέλεγχο ή τη λήψη LT4. Δύο μετα-αναλύσεις επιχείρησαν να επαναξιολογήσουν τα ανωτέρω μεθοδολογικά προβλήματα. Το κύριο εύρημα της πρώτης είναι ότι ο κίνδυνος ΚΑΝ είναι σημαντικά αυξημένος σε ασθενείς με ΥΥΘ κάτω των 65 ετών αλλά όχι σε μεγαλύτερης ηλικίας άτομα (67). Η δεύτερη έδειξε ότι ο κίνδυνος ΚΑΝ αυξάνει ανάλογα με τη βαρύτητα του ΥΥΘ και είναι ιδιαίτερα υψηλός σε άτομα με TSH>10,0 mU/L (68). Τα ευρήματα αυτά δεν ισχύουν και για τα δύο φύλα αλλά έχουν στατιστική σημαντικότητα μόνο στις γυναίκες (67). Άλλη μετα-ανάλυση 11 προοπτικών μελετών με 55287 συνολικά άτομα επιβεβαιώνει τόσο τον αυξημένο κίνδυνο ΚΑΝ όσο και την θνητότητα από ΚΑΝ αλλά μόνο στα άτομα με TSH>10,0 mU/L, χωρίς σημαντική διαφορά ανάμεσα στα δύο φύλα (69). Τέλος, στη μελέτη PROSPER (Prospective Study of Pravastatin in the Elderly at Risk- ηλικία 70-82 έτη, θετικό ιστορικό ΚΑΝ) διαπιστώθηκε ότι ο ΥΥΘ σχετίζεται με αυξημένο κίνδυνο καρδιακής ανεπάρκειας μόνο όμως στα άτομα με TSH > 10 mU/L (HR 3,01, 95% CI 1,12 – 8,11, p=0,029) (70).
Συμπερασματικά όπως καταδεικνύεται από τα δεδομένα που προαναφέρθηκαν, φαίνεται ότι τα άτομα με ΥΥΘ και ιδιαίτερα αυτά με τιμές TSH>10,0 mU/L εμφανίζουν αυξημένο κίνδυνο ΚΑΝ. Ο ρόλος της ηλικίας είναι αμφιλεγόμενος και μάλλον λειτουργεί ευνοϊκά στα μεγάλης ηλικίας άτομα. Αμφιλεγόμενος είναι επίσης και ο ρόλος του φύλου.
5.4. Επίπτωση του ΥΥΘ σε καρδιαγγειακή και ολική θνητότητα
Τα δεδομένα αναφορικά με τον κίνδυνο καρδιαγγειακής και ολικής θνητότητας σε άτομα με ΥΥΘ είναι ποικίλα και σε μεγάλο βαθμό αντικρουόμενα (59-61, 63-66, 71-74). Υπάρχουν 3 μετα-αναλύσεις στις οποίες εκτιμήθηκε τόσο ο κίνδυνος της καρδιαγγειακής όσο και της ολικής θνητότητας σε άτομα με ΥΥΘ, που δημοσιεύθηκαν μεταξύ 2008 – 2010 (67-69).
Στην πρώτη μετα-ανάλυση διαπιστώθηκε ότι η θνητότητα από ΚΑΝ ήταν αυξημένη σε άτομα με ΥΥΘ νεότερα των 65 ετών, όχι όμως και σε μεγαλύτερης ηλικίας (67). Στη μετα-ανάλυση των Ochs και συν. επιβεβαιώθηκαν ο αυξημένος κίνδυνος τόσο από ΚΑΝ όσο και ολικής θνητότητας, στα άτομα με ΥΥΘ ηλικίας κάτω των 65 ετών (68). Στην τελευταία και πιο πρόσφατη ανάλυση ο ΥΥΘ βρέθηκε να σχετίζεται με αυξημένο κίνδυνο ΚΑΝ και θνητότητα από ΚΑΝ στα άτομα με υψηλότερες τιμές TSH και ιδιαίτερα με τιμές TSH > 10 mU/L. Στην ίδια μελέτη δε διαπιστώθηκε αυξημένος κίνδυνος ΚΑΝ και ολικής θνητότητας στην υπο-ομάδα των ατόμων > 80 ετών (69). Παρόμοια ευρήματα σχετικά με την ολική θνητότητα σε ηλικιωμένους πληθυσμούς έδειξε και νεότερη πληθυσμιακή προοπτική μελέτη (74). Τα ως άνω αποτελέσματα είναι ενδεικτικά του ότι οι ‘παραδοσιακοί’ σχετικοί παράγοντες κινδύνου σε νεότερης ηλικίας πληθυσμούς όπως π.χ η υπερχοληστερολαιμία, η διαστολική υπέρταση, η ενδοθηλιακή δυσλειτουργία, η παχυσαρκία και η ινσουλινοαντίσταση ίσως να ενέχουν μικρότερο σχετικό κίνδυνο στα ηλικιωμένα άτομα ή ενδεχομένως τα επίπεδα της TSH στα όρια του ΥΥΘ να λειτουργούν προστατευτικά σε αυτά τα άτομα (2). Σε σχετική μελέτη σε πληθυσμό ηλικιωμένων ανδρών που ζούσαν μόνοι τους, τα χαμηλότερα επίπεδα FT4 και τα υψηλότερα της TSH, στα όρια του ΥΥΘ, σχετίζονταν με καλύτερη τετραετή επιβίωση (75). Προς την κατεύθυνση αυτή επίσης λειτουργούν υποστηρικτικά και τα αποτελέσματα άλλης μελέτης στην οποία διαπιστώθηκε ότι η γενετική προδιάθεση για υψηλότερα επίπεδα TSH (φορείς των SNPs rs12050077 και rs10149689 για τον υποδοχέα της TSH) σχετίζεται με ασυνήθιστη μακροζωία ενδεχομένως λόγω μειωμένης θυρεοειδικής λειτουργίας (76).
Στα άτομα με γνωστή ΚΑΝ, ο ΥΥΘ φαίνεται να σχετίζεται με αυξημένη καρδιαγγειακή θνητότητα (73). Σε μετα-ανάλυση βρέθηκε επίσης αυξημένος κίνδυνος ολικής θνητότητας σε άτομα με ΥΥΘ και συνοσηρότητα συγκριτικά με ευθυρεοειδικούς μάρτυρες (77).
Ως συμπέρασμα θα λέγαμε ότι ο ΥΥΘ σχετίζεται με καρδιαγγειακή νοσηρότητα και θνητότητα από ΚΑΝ σε άτομα ηλικίας κάτω των 65 ετών με υψηλότερα επίπεδα TSH, ιδιαίτερα όταν αυτά υπερβαίνουν την τιμή των 10,0 mU/L.
5.5. Επίπτωση ΥΥΘ σε νευρομυική, ψυχική και νοητική λειτουργία
Ο ΥΥΘ έχει συσχετισθεί με την επιδείνωση ενός μεγάλου φάσματος νευρομυικής και μυικής δυσλειτουργίας η παθογενετική βάση των οποίων δεν έχει κατανοηθεί πλήρως (1). Μεταξύ των παθογενετικών μηχανισμών που πιθανόν εμπλέκονται περιλαμβάνονται η διαταραχή της γλυκογονόλυσης (78,79), της παραγωγής μυοσίνης (80), και της λειτουργίας των μιτοχονδρίων (81,82). Το εύρος του αχίλλειου αντανακλαστικού, το οποίο αποτελεί μια βιολογική παράμετρο εκτίμησης της νευρομυικής λειτουργίας, έχει βρεθεί παθολογικό σε ασθενείς τόσο με έκδηλο όσο και με ΥΥΘ (83). Αντίθετα, δεν έχουν διαπιστωθεί διαταραχές της αγωγιμότητας στο εύρος της κινητικής- αισθητικής νευρικής δραστηριότητας, καθώς και στην ταχύτητα αγωγής του ερεθίσματος των περιφερικών νεύρων των ασθενών με ΥΥΘ (84). Ανάλογα ευρήματα από τα περιφερικά νεύρα καθώς και απουσία διαταραχών στα προκλητά δυναμικά του ακουστικού νεύρου διαπιστώθηκαν σε ασθενείς με ΥΥΘ και σε άλλη ανάλογη μελέτη (85).
Αντίθετα, όσον αφορά στα επίπεδα της κρεατινικής φωσφοκινάσης και της μυοσφαιρίνης, τα δεδομένα είναι αλληλοαναιρούμενα (84, 86-88) , παρότι έχει διαπιστωθεί θετική συσχέτιση μεταξύ των επιπέδων της πρώτης και εκείνων της TSH τόσο στον έκδηλο όσο και στον ΥΥΘ (84).
Σε ασθενείς με ΥΥΘ και νευρομυικά συμπτώματα προσδιορίστηκαν επίσης η παραγωγή γαλακτικού και πυρουβικού οξέος από τους μύες τόσο σε ηρεμία όσο και μετά από άσκηση, η οποία δε διέφερε από αυτή των μαρτύρων. Ωστόσο τα μέσα επίπεδα γαλακτικού καθώς και η μέση αύξησή τους ήταν μεγαλύτερη στους ασθενείς με ΥΥΘ στη διάρκεια της άσκησης κάτι που υποδηλώνει διαταραχές στην οξειδωτική λειτουργία των μιτοχονδρίων (89). Σε άλλη μελέτη της ίδιας ομάδας διαπιστώθηκε επιπλέον διαταραγμένος μεταβολισμός των μυών αλλά και της ανταπόκρισής τους σε συγκεκριμένο φορτίο άσκησης στους ασθενείς με ΥΥΘ (90).
Συμπερασματικά τα ως άνω ευρήματα υποστηρίζουν ότι η νευρομυική δυσλειτουργία είναι συχνή στον ΥΥΘ και επιπλέον τα αποτελέσματα των μελετών παρέμβασης υποδεικνύουν ότι οι εκδηλώσεις της δυσλειτουργίας αυτής είναι αναστρέψιμες με την χορήγηση LT4 (91). Αυτό που δεν προκύπτει με σαφήνεια και για το λόγο αυτόν απαιτούνται περαιτέρω μελέτες, είναι εάν οι όποιες εκδηλώσεις διαφοροποιούνται ανάλογα με τα επίπεδα της TSH.
Αναφορικά τέλος με τις πιθανές ψυχικές και νοητικές επιπτώσεις του ΥΥΘ υπάρχουν δεδομένα που υποστηρίζουν επιδείνωση προϋπαρχουσών διαταραχών όπως η κατάθλιψη, οι διπολικές διαταραχές καθώς και αυτής καθεαυτής της νοητικής λειτουργίας με την παρουσία του (92). Σχετική μελέτη έδειξε συσχέτιση του ΥΥΘ με αγχώδεις διαταραχές, κατάθλιψη και εκδηλώσεις νοητικής δυσλειτουργίας σε ηλικιωμένους ασθενείς (93).
5.6. Επίπτωση ΥΥΘ σε γονιμότητα, κύημα και εξέλιξη της κύησης
Τόσο οι διαταραχές της θυρεοειδικής λειτουργίας (κλινικές και υποκλινικές), όσο και τα αυτοάνοσα θυρεοειδικά νοσήματα είναι ιδιαίτερα συχνά στις γυναίκες και μάλιστα στην αναπαραγωγική ηλικία τους (0,5 – 5,0%), η παρουσία τους δε έχει συσχετισθεί με αρνητικές επιδράσεις στην κύηση (1,8,94,95). Επιπλέον, η αυτοάνοση θυρεοειδίτιδα αποτελεί τη συχνότερη αιτία ανεπάρκειας ή πλημμελώς αντιμετωπιζόμενου υποθυρεοειδισμού κατά τη διάρκεια της κύησης (1,94,96). Όπως προκύπτει από τα δεδομένα δύο ανασκοπήσεων / μετα-αναλύσεων σχετικών μελετών για την κλινική σημασία της θυρεοειδικής δυσλειτουργίας και της αυτοανοσίας στην εξέλιξη της κύησης, διαπιστώθηκε ότι ο ΥΥΘ στην πρώιμη φάση της κύησης σχετίζεται με προεκλαμψία και αυξημένη περιγεννητική θνησιμότητα σε σχέση με ευθυρεοειδικές γυναίκες. Επιπλέον, η παρουσία θυρεοειδικής αυτοανοσίας συσχετίσθηκε με αυξημένο κίνδυνο υπογονιμότητας, καθ’ έξιν αποβολών, πρόωρων τοκετών και θυρεοειδίτιδας κατά τη λοχεία σε σχέση με μάρτυρες χωρίς αυτοανοσία (97). Επίσης καταδείχθηκε ότι οι έγκυες με ΥΥΘ έχουν τριπλάσιο κίνδυνο αποβολής και διπλάσιο κίνδυνο πρόωρου τοκετού όταν συνυπάρχει αυτοανοσία (98).
Τέλος υποστηρίζεται ότι η παρουσία αθεράπευτου ΥΥΘ στη μητέρα σχετίζεται με το δείκτη ευφυΐας του παιδιού (1,8,96). Παιδιά που γεννήθηκαν από μητέρες με ΥΥΘ, υποθυροξιναιμία και θετικά αντιθυρεοειδικά αντισώματα εμφάνιζαν χαμηλότερο δείκτη ευφυΐας και κινητικής ανταπόκρισης σε σύγκριση με αυτά που γεννήθηκαν από μητέρες χωρίς θυρεοειδοπάθεια ή επαρκώς θεραπευόμενες (96,99).
Αναφορικά τέλος με την θέση της θεραπείας υποκατάστασης με LT4 φαίνεται να λειτουργεί προληπτικά και ευνοϊκά (1,8,94,96).
6. Θεραπευτική αντιμετώπιση ΥΥΘ
Υπάρχει ακόμα και σήμερα σημαντική διχογνωμία σχετικά με το ποιοι ασθενείς με ΥΥΘ θα πρέπει να αντιμετωπίζονται θεραπευτικά (3,4). Οι υπάρχουσες μελέτες παρατήρησης δε μπορούν να δώσουν σαφείς κατευθύνσεις για το θέμα της αντιμετώπισης, ιδιαίτερα στα ηλικιωμένα άτομα όπου ο ΥΥΘ συναντάται συχνότερα.
Οπωσδήποτε απαιτούνται τυχαιοποιημένες και ελεγχόμενες με μάρτυρες μελέτες, για παράδειγμα για να δειχθούν τα οφέλη χορήγησης LT4 σε σχέση με εικονικό φάρμακο σε ασθενείς με ΥΥΘ και ΚΑΝ με τελικό στόχο τη νοσηρότητα και θνητότητα από ΚΑΝ ιδιαίτερα σε ηλικιωμένα άτομα, προκειμένου να εξαχθούν ασφαλή συμπεράσματα και να τεθούν σαφείς θεραπευτικές ενδείξεις. Προς το παρόν υπάρχει μόνο μια ανάλυση που δείχνει ότι η χορήγηση LT4 μειώνει το ποσοστό καρδιαγγειακής θνησιμότητας σε 10% από 31% στην ομάδα που δεν χορηγήθηκε (62). Ωστόσο η συγκεκριμένη μελέτη επιδέχεται κριτικής λόγω του μικρού αριθμού ασθενών που έλαβαν LT4.
Επειδή όπως αναφέρθηκε, παρεμβαίνουν διάφοροι παράγοντες στην τιμή της TSH μεταξύ των οποίων και η βιολογική της διακύμανση, πριν αποφασισθεί η θεραπευτική ή μη αντιμετώπιση θα πρέπει να επιβεβαιώνεται η διάγνωση του επιμένοντος ΥΥΘ (100). Η απόφαση για θεραπευτική αντιμετώπιση εξαρτάται σε μεγάλο ποσοστό από την τιμή της TSH, εάν βρίσκεται δηλαδή μεταξύ 3 – 5 mU/L, 5,1 – 10 mU/L ή >10 mU/L.
6.1. Υποομάδα ασθενών με τιμή TSH>10,0 mU/L
H πλειονότητα των θυρεοειδολόγων-ενδοκρινολόγων συστήνει θεραπευτική αντιμετώπιση όλων των ασθενών αυτής της κατηγορίας (1,4,6-8). Όπως ήδη αναφέρθηκε οι αρνητικές επιδράσεις του ΥΥΘ είναι πιο σοβαρές σε αυτήν την υπο-ομάδα και συγκεκριμένα υπάρχει μεγαλύτερος κίνδυνος εξέλιξης του ΥΥΘ σε έκδηλο υποθυρεοειδισμό (14,34-36), είναι οι ασθενείς πιο συχνά συμπτωματικοί (101), εμφανίζουν συχνότερα δυσλιπιδαιμία (54), όπως και καρδιαγγειακή δυσλειτουργία με αυξημένο κίνδυνο ΚΑΝ (67-69) και καρδιακής ανεπάρκειας (64, 102). Τα αποτελέσματα σχετικών μελετών δείχνουν ότι η θεραπεία με LT4 έχει ως αποτέλεσμα μείωση ως 8 mg της LDL-χοληστερόλης (54, 101). Μεταξύ των παραγόντων που προδιαγράφουν όφελος στο λιπιδαιμικό ‘προφίλ’ από την χορήγηση LT4 περιλαμβάνονται τα υψηλότερα επίπεδα TSH, η ινσουλινοαντίσταση, τα υψηλότερα αρχικά επίπεδα ολικής χοληστερόλης καθώς και η υπερτριγλυκεριδαιμία τύπου I I I.
Η θεραπεία με LT4 κρίνεται μάλλον αναγκαία σε νεαρότερης ηλικίας άτομα (<65 έτη) με σκοπό την πρόληψη έκδηλου υποθυρεοεδισμού, την εξάλειψη των συμπτωμάτων, τη βελτίωση της ποιότητας ζωής και την πρόληψη εμφάνισης ΚΑΝ και θνητότητας (62, 102). Όπως φαίνεται και από την επαναξιολόγηση των δεδομένων της μελέτης Wickham η χορήγηση LT4 σε ασθενείς με ΥΥΘ μειώνει σημαντικά την ολική θνησιμότητα (62).
Τέλος υπάρχουν δεδομένα που δείχνουν ότι η χορήγηση LT4 συνοδεύεται από βελτίωση νευρομυικών, ψυχικών και νοητικών δυσλειτουργιών που επιδεινώνουν τον ΥΥΘ (46,51,87,101,103).
6.2. Υπο-ομάδα ασθενών με τιμή TSH μεταξύ 5,1-10 mU/L
Σε αντίθεση με την προηγούμενη πιο ‘σοβαρή’ υποκατηγορία ΥΥΘ, δεν υπάρχει ομοφωνία τόσο στις κλινικές επιπτώσεις όσο και στο ενδεχόμενο όφελος από την χορήγηση LT4 σε αυτή την ομάδα ‘ήπιου’ ΥΥΘ (1,3,4,8). Η θεραπευτική ή μη αντιμετώπιση εξατομικεύεται ανάλογα με διάφορους παράγοντες ‘κινδύνου’ όπως η ηλικία, η πιθανότητα εξέλιξης σε έκδηλη νόσο, η ποιότητα ζωής η συνοσηρότητα και άλλοι νοητικοί, καρδιαγγειακοί και μεταβολικοί παράγοντες (1,8). Νεαρές γυναίκες αναπαραγωγικής ηλικίας με συνύπαρξη βρογχοκήλης και παρουσία αντι-TPO αντισωμάτων αντιμετωπίζονται συχνότερα από ότι ηλικιωμένοι ασθενείς (1,8,104). Τα υπάρχοντα βιβλιογραφικά δεδομένα, παρά τα αντικρουόμενα και επαμφοτερίζοντα ευρήματά τους, δείχνουν ενδεχόμενο όφελος από την χορήγηση LT4 σε ορισμένες κατηγορίες συμπτωμάτων που συνοψίζονται στον πίνακα 9 (1,8,19,46,47,87,101,103-110). Με το δεδομένο ότι παιδιά που γεννήθηκαν από μητέρες με ΥΥΘ κατά τη διάρκεια της κύησης εμφανίζουν χαμηλότερο δείκτη ευφυΐας (99) και της αρνητικής επίδρασης του ήπιου ΥΥΘ στην έκβαση της κύησης η θεραπεία με LT4 κρίνεται αναγκαία σε έγκυες ή γυναίκες που επιθυμούν να τεκνοποιήσουν άμεσα. Ανάλογη αντιμετώπιση θα πρέπει να έχουν και τα παιδιά ή οι έφηβοι με ΥΥΘ δεδομένης της επίδρασης των θυρεοειδικών ορμομών στην ανάπτυξη. Τέλος, στην υποομάδα ασθενών με TSH > 8 mU/L υπάρχει μεγάλη πιθανότητα εξέλιξης σε πιο σοβαρό ΥΥΘ τα επόμενα 4 έτη και ως εκ τούτου θα είχε ενδεχομένως και εδώ ένδειξη η χορήγηση LT4 (19).
Πίνακας 9. Κατηγορίες ασθενών στις οποίες παρατηρήθηκε όφελος από την χορήγηση LT4.
| Εγκυμοσύνη ή αναπαραγωγική ηλικία |
| Βρογχοκήλη |
| Trial για πιθανά υποθυρεοειδικά συμπτώματα |
| Προτίμηση ασθενούς |
| Παιδική ηλικία ή εφηβεία |
| TSH > 8 mIU/L |
| Διπολικές διαταραχές/ κατάθλιψη |
| Υπογονιμότητα |
| Παρουσία αντιθυρεοειδικών αντισωμάτων |
| Προοδευτική αύξηση της TSH |
| Διαταραχές ωοθυλακιορηξίας |
| Υπερλιπιδαιμία |
6.3. Υπο-ομάδα ασθενών με τιμή TSH μεταξύ 3 – 5 mU/L
Επίπεδα TSH σε αυτά τα όρια είναι μάλλον απίθανο να υποδηλώνουν θυρεοειδική δυσλειτουργία και επιπλέον, το όφελος από την θεραπεία με LT4 προκειμένου να μειωθούν τα επίπεδά της δεν είναι τεκμηριωμένο. Η μείωση των ανωτέρω επιπέδων στα όρια των 3 mU/L θα είχε τεράστιο κόστος εργαστηριακών εξετάσεων και κλινικού ελέγχου με αμφίβολα αποτελέσματα (12) .
Στην εικόνα 11 παρουσιάζονται σχηματικά τα προτεινόμενα βήματα διαγνωστικής και θεραπευτικής αντιμετώπισης ασθενών με ΥΥΘ και ιδιαίτερα της υπο-ομάδας ‘πολύ ήπιου’ ΥΥΘ. Ως κύριο κριτήριο χρησιμοποιείται η ύπαρξη θεραπευτικού οφέλους και η αποφυγή παρενεργειών ή ανεπιθύμητων ενεργειών. Συνοψίζοντας θα μπορούσε να λεχθεί ότι η αντιμετώπιση του ΥΥΘ γίνεται με LT4 και υπάρχει ομοφωνία σχετικά με την υποομάδα ασθενών με τιμή TSH > 10 mU/L. Στην υπο-ομάδα ασθενών με τιμή TSH μεταξύ 3 – 5 mU/L προτείνεται εξατομίκευση. Η συνήθης συνιστώμενη δοσολογία κυμαίνεται από 25 – 75 μg ημερησίως με τις μικρότερες δοσολογίες να προτείνονται κυρίως σε μεγαλύτερης ηλικίας ασθενείς με συνοσηρότητα. Ο επανακαθορισμός της προτεινόμενης δοσολογίας γίνεται σε μεσοδιαστήματα επανελέγχου δύο μηνών και εφόσον τα επίπεδα της TSH σταθεροποιηθούν ο επανέλεγχος γίνεται σε 6μηνιαία βάση. Σε νεαρότερης ηλικίας τα επίπεδα της TSH πρέπει να κυμαίνονται από 0,3 ως 3 mU/L, ενώ στα μεγαλύτερης ηλικίας άτομα σε υψηλότερα επίπεδα. Η θεραπευτική στόχευση οφείλει να λαμβάνει υπόψη πιθανές εκδηλώσεις φαρμακευτικής θυρεοτοξίκωσης. Η στάθμιση των επιπτώσεων του αθεράπευτου ήπιου ΥΥΘ και της φαρμακευτικής θυρεοτοξίκωσης επαφίεται στην κρίση του θεράποντος ιατρού.

Εικόνα 11. Διαγνωστικός και θεραπευτικός αλγόριθμος αντιμετώπισης ασθενών με ΥΥΘ και ιδιαίτερα της υπο-ομάδας ‘πολύ ήπιου’ ΥΥΘ.
Βιβλιογραφία
- Biondi B, Cooper D. S. The clinical significance of subclinical thyroid dysfunction. Endocr Rev 2008; 29:76-131
- Biondi B.Natural history, diagnosis and management of subclinical thyroid dysfunction. Best Pract Res Clin Endocrinol Metab 2012; 26:431-446
- Gharib H, Tuttle RM, Baskin HJ, Fish LH, Singer PA, McDermott MT. Subclinical thyroid dysfunction: a joint statement on management from the American Association of Clinical Endocrinologists, the American Thyroid Association, and the Endocrine Society. J Clin Endocrinol Metab 2005; 90:581-585
- Surks MI, Ortiz E, Daniels GH, Sawin CT, Col NF, Cobin RH, et al. Subclinical thyroid disease: scientific review and guidelines for diagnosis and management. JAMA 2004; 291:228-238
- Helfand M. Screening for subclinical thyroid dysfunction in nonpregnant adults: a summary of the evidence for the U.S. Preventive Services Task Force. Ann Intern Med 2004; 140:128-141
- McDermott MT, Ridgway EC. Subclinical hypothyroidism is mild thyroid failure and should be treated. J Clin Endocrinol Metab 2001; 86:4585-4590
- Chu JW, Crapo LM.The treatment of subclinical hypothyroidism is seldom necessary. J Clin Endocrinol Metab 2001; 86:4591-4599
- Cooper DS, Biondi B.Subclinical thyroid disease. Lancet 2012; 379:1142-1154
- Baloch Z, Carayon P, Conte-Devolx B, Demers LM, Feldt-Rasmussen U, Henry JF, et al. Laboratory medicine practice guidelines. Laboratory support for the diagnosis and monitoring of thyroid disease. Thyroid 2003; 13:3-126
- Dayan CM, Saravanan P, Bayly G. Whose normal thyroid function is better–yours or mine? Lancet 2002;360:353
- Wartofsky L, Dickey RA. The evidence for a narrower thyrotropin reference range is compelling. J Clin Endocrinol Metab 2005; 90:5483-5488
- Surks MI, Goswami G, Daniels GH. The thyrotropin reference range should remain unchanged. J Clin Endocrinol Metab 2005; 90:5489-5496
- Brabant G, Beck-Peccoz P, Jarzab B, Laurberg P, Orgiazzi J, Szabolcs I, et al. Is there a need to redefine the upper normal limit of TSH? Eur J Endocrinol 2006; 154:633-637
- Imaizumi M, Sera N, Ueki I, Horie I, Ando T, Usa T, et al. Risk for progression to overt hypothyroidism in an elderly Japanese population with subclinical hypothyroidism. Thyroid 2011; 21:1177-1182
- Hollowell JG, Staehling NW, Flanders WD, Hannon WH, Gunter EW, Spencer CA, et al. Serum TSH, T(4), and thyroid antibodies in the United States population (1988 to 1994): National Health and Nutrition Examination Survey (NHANES III). J Clin Endocrinol Metab 2002; 87:489-499
- Karmisholt J, Andersen S, Laurberg P. Variation in thyroid function tests in patients with stable untreated subclinical hypothyroidism. Thyroid 2008;18:303-308
- Canaris GJ, Manowitz NR, Mayor G, Ridgway E. C. The Colorado thyroid disease prevalence study. Arch Intern Med 2000;160:526-534
- Surks MI, Boucai L. Age- and race-based serum thyrotropin reference limits. J Clin Endocrinol Metab 2010; 95:496-502
- Fatourechi V. Subclinical hypothyroidism: an update for primary care physicians. Mayo Clin Proc 2009; 84:65-71
- Roberts CG, Ladenson PW. Hypothyroidism. Lancet 2004; 363:793-803
- Somwaru LL, Arnold AM, Joshi N, Fried LP, Cappola AR. High frequency of and factors associated with thyroid hormone over-replacement and under-replacement in men and women aged 65 and over. J Clin Endocrinol Metab 2009; 94:1342-1345
- Vanderpump MP, Tunbridge WM, French JM, Appleton D, Bates D, Clark F, et al. . The incidence of thyroid disorders in the community: a twenty-year follow-up of the Whickham Survey. Clin Endocrinol (Oxf) 1995;43:55-68
- Samuels MH. Subclinical thyroid disease in the elderly. Thyroid 1998; 8:803-813
- Andersen S, Pedersen KM, Bruun NH, Laurberg P. Narrow individual variations in serum T(4) and T(3) in normal subjects: a clue to the understanding of subclinical thyroid disease. J Clin Endocrinol Metab 2002;87:1068-1072
- Baskin HJ, Cobin RH, Duick DS, Gharib H, Guttler RB, Kaplan MM, et al. American Association of Clinical Endocrinologists medical guidelines for clinical practice for the evaluation and treatment of hyperthyroidism and hypothyroidism. Endocr Pract 2002;8:457-469
- Weissel M. Disturbances of thyroid function in the elderly. Wien Klin Wochenschr 118:16-20
- da Costa VM, Rosenthal D Effects of aging on thyroidal function and proliferation. Curr Aging Sci 1:101-104
- Peeters RP. Thyroid hormones and aging. Hormones (Athens) 2008 7:28-35
- Mooradian AD. Asymptomatic hyperthyroidism in older adults: is it a distinct clinical and laboratory entity? Drugs Aging 2008;25:371-80
- Kaptein EM. Thyroxine kinetics in nonthyroidal illnesses. J Endocrinol Invest 1986;9 (Suppl 4):37-46
- Wiersingha WM, Van Den Berghe, G. Nonthyroidal illness syndrome. In: Braverman L, Utiger, R. ed. Werner and Ingbar The thyroid. 10th ed. Philadelphia: Lippincott Williams & Wilkins; Chapter 11C. 203-216
- Bello G, Ceaichisciuc I, Silva S, Antonelli M. The role of thyroid dysfunction in the critically ill: a review of the literature. Minerva Anestesiol 2010;76:919-28
- Biondi B.Thyroid and obesity: an intriguing relationship. J Clin Endocrinol Metab 2010; 95:3614-3617
- Li Y, Teng D, Shan Z, Teng X, Guan H, Yu X, et al. Antithyroperoxidase and antithyroglobulin antibodies in a five-year follow-up survey of populations with different iodine intakes. J Clin Endocrinol Metab 2008; 93:1751-1757
- Walsh JP, Bremner AP, Feddema P, Leedman PJ, Brown SJ, O’Leary P. Thyrotropin and thyroid antibodies as predictors of hypothyroidism: a 13-year, longitudinal study of a community-based cohort using current immunoassay techniques. J Clin Endocrinol Metab 2010; 95:1095-1104
- Huber G, Staub JJ, Meier C, Mitrache C, Guglielmetti M, Huber P, et al. Prospective study of the spontaneous course of subclinical hypothyroidism: prognostic value of thyrotropin, thyroid reserve, and thyroid antibodies. J Clin Endocrinol Metab 2002; 87:3221-3226
- Diez JJ, Iglesias P. Spontaneous subclinical hypothyroidism in patients older than 55 years: an analysis of natural course and risk factors for the development of overt thyroid failure. J Clin Endocrinol Metab 2004; 89:4890-4897
- Grabe HJ, Volzke H, Ludemann J, Wolff B, Schwahn C, John U, et al. Mental and physical complaints in thyroid disorders in the general population. Acta Psychiatr Scand 2005; 112:286-293
- Pollock MA, Sturrock A, Marshall K, Davidson KM, Kelly CJ, McMahon AD, et al. Thyroxine treatment in patients with symptoms of hypothyroidism but thyroid function tests within the reference range: randomised double blind placebo controlled crossover trial. BMJ 2001; 323:891-895
- Bianchi GP, Zaccheroni V, Solaroli E, Vescini F, Cerutti R, Zoli M, et al. Health-related quality of life in patients with thyroid disorders. Qual Life Res 2004; 13:45-54
- Carta M, Loviselli A, Hardoy M, Massa S, Cadeddu M, Sardu C, et al. The link between thyroid autoimmunity (antithyroid peroxidase autoantibodies) with anxiety and mood disorders in the community: a field of interest for public health in the future. BMC Psychiatry 2004; 4:25
- Pop VJ, Maartens LH, Leusink G, Van Son MJ, Knottnerus AA, Ward AM, et al. Are autoimmune thyroid dysfunction and depression related? J Clin Endocrinol Metab 1998; 83:3194-3197
- Nemeroff CB, Simon JS, Haggerty JJ, Jr., Evans DL. Antithyroid antibodies in depressed patients. Am J Psychiatry 1985 142:840-843
- Zulewski H, Muller B, Exer P, Miserez AR, Staub JJ. Estimation of tissue hypothyroidism by a new clinical score: evaluation of patients with various grades of hypothyroidism and controls. J Clin Endocrinol Metab 1997; 82:771-776
- Bell RJ, Rivera-Woll L, Davison SL, Topliss DJ, Donath S, Davis, S. R. Well-being, health-related quality of life and cardiovascular disease risk profile in women with subclinical thyroid disease – a community-based study. Clin Endocrinol (Oxf) 2007; 66:548-556
- Cooper DS, Halpern R, Wood LC, Levin AA, Ridgway EC.L-Thyroxine therapy in subclinical hypothyroidism. A double-blind, placebo-controlled trial. Ann Intern Med 1984; 101:18-24
- Kong WM, Sheikh MH, Lumb PJ, Naoumova RP, Freedman DB, Crook M, et al. A 6-month randomized trial of thyroxine treatment in women with mild subclinical hypothyroidism. Am J Med 2002; 112:348-354
- Somwaru LL, Rariy CM, Arnold AM, Cappola AR. The natural history of subclinical hypothyroidism in the elderly: the cardiovascular health study. J Clin Endocrinol Metab 2012; 97:1962-1969
- Zhu DF, Wang ZX, Zhang DR, Pan ZL, He S, Hu XP, et al. fMRI revealed neural substrate for reversible working memory dysfunction in subclinical hypothyroidism. Brain 2006; 129:2923-2930
- Billewicz WZ, Chapman RS, Crooks J, Day ME, Gossage J, Wayne E, et al. Statistical methods applied to the diagnosis of hypothyroidism. Q J Med 1969; 38:255-266
- Biondi B, Palmieri EA, Lombardi G, Fazio S. Effects of subclinical thyroid dysfunction on the heart. Ann Intern Med 2002; 137:904-914
- Biondi B.Cardiovascular effects of mild hypothyroidism. Thyroid 2007; 17:625-630
- Cappola AR, Ladenson P. W. Hypothyroidism and atherosclerosis. J Clin Endocrinol Metab 2003; 88:2438-2444
- Danese MD, Ladenson PW, Meinert CL, Powe NR. Clinical review 115: effect of thyroxine therapy on serum lipoproteins in patients with mild thyroid failure: a quantitative review of the literature. J Clin Endocrinol Metab 2000; 85:2993-3001
- Palmieri EA, Fazio S, Lombardi G, Biondi B. Subclinical hypothyroidism and cardiovascular risk: a reason to treat? Treat Endocrinol 2004; 3:233-244
- Duntas LH, Wartofsky L. Cardiovascular risk and subclinical hypothyroidism: focus on lipids and new emerging risk factors. What is the evidence? Thyroid 2007; 17:1075-1084
- Hueston WJ, King DE, Geesey ME. Serum biomarkers for cardiovascular inflammation in subclinical hypothyroidism. Clin Endocrinol (Oxf) 2005; 63:582-587
- Hak AE, Pols HA, Visser TJ, Drexhage HA, Hofman A, Witteman JC. Subclinical hypothyroidism is an independent risk factor for atherosclerosis and myocardial infarction in elderly women: the Rotterdam Study. Ann Intern Med 2000; 132:270-278
- Asvold BO, Bjoro T, Nilsen TI, Gunnell D, Vatten L. J. Thyrotropin levels and risk of fatal coronary heart disease: the HUNT study. Arch Intern Med 2008;168:855-860
- Imaizumi M, Akahoshi M, Ichimaru S, Nakashima E, Hida A, Soda M, et al. Risk for ischemic heart disease and all-cause mortality in subclinical hypothyroidism. J Clin Endocrinol Metab 2004; 89:3365-3370
- Vanderpump MP, Tunbridge WM, French JM, Appleton D, Bates D, Clark F, et al. The development of ischemic heart disease in relation to autoimmune thyroid disease in a 20-year follow-up study of an English community. Thyroid 1996; 6:155-160
- Razvi S, Weaver JU, Vanderpump MP, Pearce SH. The incidence of ischemic heart disease and mortality in people with subclinical hypothyroidism: reanalysis of the Whickham Survey cohort. J Clin Endocrinol Metab 2010; 95:1734-1740
- Walsh JP, Bremner AP, Bulsara MK, O’Leary P, Leedman PJ, Feddema P, et al. Subclinical thyroid dysfunction as a risk factor for cardiovascular disease. Arch Intern Med 2005; 165:2467-2472
- Rodondi N, Newman AB, Vittinghoff E, de Rekeneire N, Satterfield S, Harris TB, et al. Subclinical hypothyroidism and the risk of heart failure, other cardiovascular events, and death. Arch Intern Med 2005; 165:2460-2466
- Cappola AR, Fried LP, Arnold AM, Danese MD, Kuller LH, Burke GL, et al. Thyroid status, cardiovascular risk, and mortality in older adults. JAMA 2006; 295:1033-1041
- Parle JV, Maisonneuve P, Sheppard MC, Boyle P, Franklyn JA. Prediction of all-cause and cardiovascular mortality in elderly people from one low serum thyrotropin result: a 10-year cohort study. Lancet 2001; 358:861-865
- Razvi S, Shakoor A, Vanderpump M, Weaver JU, Pearce SH. The influence of age on the relationship between subclinical hypothyroidism and ischemic heart disease: a metaanalysis. J Clin Endocrinol Metab 2008; 93:2998-3007
- Ochs N, Auer R, Bauer DC, Nanchen D, Gussekloo J, Cornuz J, et al. Meta-analysis: subclinical thyroid dysfunction and the risk for coronary heart disease and mortality. Ann Intern Med 2008; 148:832-845
- Rodondi N, den Elzen WP, Bauer DC, Cappola AR, Razvi S, Walsh JP, et al. Subclinical hypothyroidism and the risk of coronary heart disease and mortality. JAMA 2010; 304:1365-1374
- Nanchen D, Gussekloo J, Westendorp RG, Stott DJ, Jukema JW, Trompet S, et al. Subclinical thyroid dysfunction and the risk of heart failure in older persons at high cardiovascular risk. J Clin Endocrinol Metab 2012; 97:852-861
- Gussekloo J, van Exel E, de Craen AJ, Meinders AE, Frolich M, Westendorp RG. Thyroid status, disability and cognitive function, and survival in old age. JAMA 292:2591-2599
- Sgarbi JA, Matsumura LK, Kasamatsu TS, Ferreira SR, Maciel RM Subclinical thyroid dysfunctions are independent risk factors for mortality in a 7.5-year follow-up: the Japanese-Brazilian thyroid study. Eur J Endocrinol 162:569-577
- Iervasi G, Molinaro S, Landi P, Taddei MC, Galli E, Mariani F, et al. Association between increased mortality and mild thyroid dysfunction in cardiac patients. Arch Intern Med 2007;167:1526-1532
- De Jongh RT, Lips P, Van Schoor NM, Rijs KJ, Deeg DJ, Comijs HC, et al. Endogenous subclinical thyroid disorders, physical and cognitive function, depression, and mortality in older individuals. Eur J Endocrinol 2011;165:545-554
- Van den Beld AW, Visser TJ, Feelders RA, Grobbee DE, Lamberts SW. Thyroid hormone concentrations, disease, physical function, and mortality in elderly men. J Clin Endocrinol Metab 2005;90:6403-6409
- Atzmon G, Barzilai N, Surks MI, Gabriely I. Genetic predisposition to elevated serum thyrotropin is associated with exceptional longevity. J Clin Endocrinol Metab 2009;94:4768-4775
- Haentjens P, Van Meerhaeghe A, Poppe K, Velkeniers B. Subclinical thyroid dysfunction and mortality: an estimate of relative and absolute excess all-cause mortality based on time-to-event data from cohort studies. Eur J Endocrinol 2008;159:329-341
- McDaniel HG, Pittman CS, Oh SJ, DiMauro S. Carbohydrate metabolism in hypothyroid myopathy. Metabolism 1977;26:867-873
- Taylor DJ, Rajagopalan B, Radda GK. Cellular energetics in hypothyroid muscle. Eur J Clin Invest 1992;22:358-365
- Caiozzo VJ, Baker MJ, Baldwin K. M. Novel transitions in MHC isoforms: separate and combined effects of thyroid hormone and mechanical unloading. J Appl Physiol 1998;85:2237-2248
- Kaminsky P, Robin-Lherbier B, Brunotte F, Escanye JM, Walker P, Klein M, et al. Energetic metabolism in hypothyroid skeletal muscle, as studied by phosphorus magnetic resonance spectroscopy. J Clin Endocrinol Metab 1992;74:124-129
- Argov Z, Renshaw PF, Boden B, Winokur A, Bank W. J. Effects of thyroid hormones on skeletal muscle bioenergetics. In vivo phosphorus-31 magnetic resonance spectroscopy study of humans and rats. J Clin Invest 1988;81:1695-1701
- Goulis DG, Tsimpiris N, Delaroudis S, Maltas B, Tzoiti M, Dagilas A, et al. Stapedial reflex: a biological index found to be abnormal in clinical and subclinical hypothyroidism. Thyroid 1998;8:583-587
- Hekimsoy Z, Oktem IK. Serum creatine kinase levels in overt and subclinical hypothyroidism. Endocr Res 2005;31:171-175
- Ozata M, Ozkardes A, Corakci A, Gundogan MA. Subclinical hypothyroidism does not lead to alterations either in peripheral nerves or in brainstem auditory evoked potentials (BAEPs). Thyroid 1995;5:201-205
- Beyer IW, Karmali R, Demeester-Mirkine N, Cogan E, Fuss, M. J. Serum creatine kinase levels in overt and subclinical hypothyroidism. Thyroid 1998;8:1029-1031
- Nystrom E, Caidahl K, Fager G, Wikkelso C, Lundberg PA, Lindstedt G. A double-blind cross-over 12-month study of L-thyroxine treatment of women with ‘subclinical’ hypothyroidism. Clin Endocrinol (Oxf) 1988;29:63-75
- Staub JJ, Althaus BU, Engler H, Ryff AS, Trabucco P, Marquardt K, et al. Spectrum of subclinical and overt hypothyroidism: effect on thyrotropin, prolactin, and thyroid reserve, and metabolic impact on peripheral target tissues. Am J Med 1992;92:631-642
- Monzani F, Caraccio N, Siciliano G, Manca L, Murri L, Ferrannini E. Clinical and biochemical features of muscle dysfunction in subclinical hypothyroidism. J Clin Endocrinol Metab 1997;82:3315-3318
- Caraccio N, Natali A, Sironi A, Baldi S, Frascerra S, Dardano A, et al. Muscle metabolism and exercise tolerance in subclinical hypothyroidism: a controlled trial of levothyroxine. J Clin Endocrinol Metab 2005;90:4057-4062
- Christ-Crain M, et al Effect of l-Thyroxine Replacement Therapy on Surrogate Markers of Skeletal and Cardiac Function in Subclinical Hypothyroidism. Endocrinologist 2004;14:161-166
- Haggerty JJ, Jr., Garbutt JC, Evans DL, Golden RN, Pedersen C, Simon JS, et al. Subclinical hypothyroidism: a review of neuropsychiatric aspects. Int J Psychiatry Med 1990;20:193-208
- Roberts LM, Pattison H, Roalfe A, Franklyn J, Wilson S, Hobbs FD, et al. Is subclinical thyroid dysfunction in the elderly associated with depression or cognitive dysfunction? Ann Intern Med 2006;145:573-581
- Krassas GE, Poppe K, Glinoer D. Thyroid function and human reproductive health. Endocr Rev 2010;31:702-575
- Krassas GE, Pontikidis, N.E. The male and Female Reproductive System in Hypothyroidism. In: Braverman L, Utiger, R. ed. Werner and Ingbar The thyroid .10th ed. Philadelphia: Lippincot Williams & Wilkins; Chapter 41. 582-589
- Abalovich M, Amino N, Barbour LA, Cobin RH, De Groot LJ, Glinoer D, et al. Management of thyroid dysfunction during pregnancy and postpartum: an Endocrine Society Clinical Practice Guideline. J Clin Endocrinol Metab 2007;92(8 Suppl):S1-47
- Van den Boogaard E, Vissenberg R, Land JA, van Wely M, van der Post JA, Goddijn M, Bisschop PH. Significance of (sub)clinical thyroid dysfunction and thyroid autoimmunity before conception and in early pregnancy: a systematic review. Hum Reprod Update 2011;17:605-619
- Thangaratinam S, Tan A, Knox E, Kilby MD, Franklyn J, Coomarasamy A. Association between thyroid autoantibodies and miscarriage and preterm birth: meta-analysis of evidence. BMJ 2011;342:d2616
- Haddow JE, Palomaki GE, Allan WC, Williams JR, Knight GJ, Gagnon J, et al. Maternal thyroid deficiency during pregnancy and subsequent neuropsychological development of the child. N Engl J Med 1999;341:549-555
- Karmisholt J, Andersen S, Laurberg P. Variation in thyroid function in subclinical hypothyroidism: importance of clinical follow-up and therapy. Eur J Endocrinol 2011;164:317-323
- Meier C, Staub JJ, Roth CB, Guglielmetti M, Kunz M, Miserez AR, et al. TSH-controlled L-thyroxine therapy reduces cholesterol levels and clinical symptoms in subclinical hypothyroidism: a double blind, placebo-controlled trial (Basel Thyroid Study). J Clin Endocrinol Metab 2001;86:4860-4866
- Rodondi N, Bauer DC, Cappola AR, Cornuz J, Robbins J, Fried LP, et al. Subclinical thyroid dysfunction, cardiac function, and the risk of heart failure. The Cardiovascular Health study. J Am Coll Cardiol 2008;52:1152-1159
- Jaeschke R, Guyatt G, Gerstein H, Patterson C, Molloy W, Cook D, et al. Does treatment with L-thyroxine influence health status in middle-aged and older adults with subclinical hypothyroidism? J Gen Intern Med 1996;11:744-749
- Fatourechi V, Lankarani M, Schryver PG, Vanness DJ, Long KH, Klee GG. Factors influencing clinical decisions to initiate thyroxine therapy for patients with mildly increased serum thyrotropin (5.1-10.0 mIU/L). Mayo Clin Proc 2003;78:554-560
- Monzani F, Caraccio N, Kozakowa M, Dardano A, Vittone F, Virdis A, et al. Effect of levothyroxine replacement on lipid profile and intima-media thickness in subclinical hypothyroidism: a double-blind, placebo- controlled study. J Clin Endocrinol Metab 2004;89:2099-2106
- Monzani F, Di Bello V, Caraccio N, Bertini A, Giorgi D, Giusti C, et al. Effect of levothyroxine on cardiac function and structure in subclinical hypothyroidism: a double blind, placebo-controlled study. J Clin Endocrinol Metab 2001;86:1110-1115
- Jorde R, Waterloo K, Storhaug H, Nyrnes A, Sundsfjord J, Jenssen TG. Neuropsychological function and symptoms in subjects with subclinical hypothyroidism and the effect of thyroxine treatment. J Clin Endocrinol Metab 2006;91:145-153
- Razvi S, Ingoe L, Keeka G, Oates C, McMillan C, Weaver JU. The beneficial effect of L-thyroxine on cardiovascular risk factors, endothelial function, and quality of life in subclinical hypothyroidism: randomized, crossover trial. J Clin Endocrinol Metab 2007;92:1715-1723
- Yazici M, Gorgulu S, Sertbas Y, Erbilen E, Albayrak S, Yildiz O, et al. Effects of thyroxin therapy on cardiac function in patients with subclinical hypothyroidism: index of myocardial performance in the evaluation of left ventricular function. Int J Cardiol 2004;95:135-143
- Caraccio N, Ferrannini E, Monzani F. Lipoprotein profile in subclinical hypothyroidism: response to levothyroxine replacement, a randomized placebo-controlled study. J Clin Endocrinol Metab 2002;87:1533-1538
- Falkenberg M, Kagedal B, Norr A. Screening of an elderly female population for hypo- and hyperthyroidism by use of a thyroid hormone panel. Acta Med Scand 1983;214:361-365
- Sawin CT, Castelli WP, Hershman JM, McNamara P, Bacharach P. The aging thyroid. Thyroid deficiency in the Framingham Study. Arch Intern Med 1985;145:1386-1388
- Bagchi N, Brown TR, Parish RF. Thyroid dysfunction in adults over age 55 years. A study in an urban US community. Arch Intern Med 1990;150:785-787
- Mariotti S, Barbesino G, Caturegli P, Bartalena L, Sansoni P, Fagnoni F, et al. Complex alteration of thyroid function in healthy centenarians. J Clin Endocrinol Metab 1993;77:1130-4
- Manciet G, Dartigues JF, Decamps A, Barberger-Gateau P, Letenneur L, Latapie MJ, et al. The PAQUID survey and correlates of subclinical hypothyroidism in elderly community residents in the southwest of France. Age Ageing 1995;24:235-241
- Luboshitzky R, Oberman AS, Kaufman N, Reichman N, Flatau E. Prevalence of cognitive dysfunction and hypothyroidism in an elderly community population. Isr J Med Sci 1996;32:60-65
- Sawin CT, Chopra D, Azizi F, Mannix JE, Bacharach P. The aging thyroid. Increased prevalence of elevated serum thyrotropin levels in the elderly. JAMA 1979;242:247-250
- Livingston EH, Hershman JM, Sawin CT, Yoshikawa TT. Prevalence of thyroid disease and abnormal thyroid tests in older hospitalized and ambulatory persons. J Am Geriatr Soc 1987;35:109-114
- Rosenthal MJ, Hunt WC, Garry PJ, Goodwin JS. Thyroid failure in the elderly. Microsomal antibodies as discriminant for therapy. JAMA 1987;258:209-213
- Brochmann H, Bjoro T, Gaarder PI, Hanson F, Frey HM. Prevalence of thyroid dysfunction in elderly subjects. A randomized study in a Norwegian rural community (Naeroy). Acta Endocrinol (Copenh) 1988;117:7-12
- Drinka PJ, Nolten WE. Prevalence of previously undiagnosed hypothyroidism in residents of a midwestern nursing home. South Med J 1990;83:1259-1261
- Bemben DA, Winn P, Hamm RM, Morgan L, Davis A, Barton E. Thyroid disease in the elderly. Part 1. Prevalence of undiagnosed hypothyroidism. J Fam Pract 1994;38:577-582
- Jayme JJ, Ladenson PW. Subclinical thyroid dysfunction in the elderly. Trends Endocrinol Metab 1994;5:79-86
- Hawkins BR, Cheah PS, Dawkins RL, Whittingham S, Burger HG, Patel Y, et al. Diagnostic significance of thyroid microsomal antibodies in randomly selected population. Lancet 1980;2:1057-1059
- Geul KW, van Sluisveld IL, Grobbee DE, Docter R, de Bruyn AM, Hooykaas H, et al. The importance of thyroid microsomal antibodies in the development of elevated serum TSH in middle-aged women: associations with serum lipids. Clin Endocrinol (Oxf) 1993;39:275-280
- Gordin A, Lamberg BA. Spontaneous hypothyroidism in symptomless autoimmune thyroiditis. A long-term follow-up study. Clin Endocrinol (Oxf) 1981;15:537-543
- Wiershinga W Hypothyroidism and myxedema coma. In: De Groot LJ, Jameson J.L. ed. Endocrinology. 4th ed. Philadelphia: Saunders W. B; 2001; 1491-1506
- Surks MI, Hollowell JG Age-specific distribution of serum thyrotropin and antithyroid antibodies in the US population: implications for the prevalence of subclinical hypothyroidism. J Clin Endocrinol Metab 92:4575-4582
Created: February 25, 2015
Last update: February 25, 2015